
 .
.分析 由常温下,0.05mol/LA溶液的pH=13,则A为二元强碱,所以A为Ba(OH)2;
D、E的溶液显酸性,E溶液与其余四种的浓溶液反应均有沉淀生成,则E为AgNO3;
A与D的溶液混合时有白色沉淀生成,当A过量时沉淀部分溶解,则D为铝盐,再根据溶液中的阴离子分析,D为Al2(SO4)3;
A与B的浓溶液混合时有刺激性气味的气体产生,同时有白色沉淀生成,且B显酸性,则B为(NH4)2CO3;
剩余离子为Na+和Cl-,C溶液显中性,所以C为NaCl,以此来解答.
解答 解:由常温下,0.05mol/LA溶液的pH=13,则A为二元强碱,所以A为Ba(OH)2;
D、E的溶液显酸性,E溶液与其余四种的浓溶液反应均有沉淀生成,则E为AgNO3;
A与D的溶液混合时有白色沉淀生成,当A过量时沉淀部分溶解,则D为铝盐,再根据溶液中的阴离子分析,D为Al2(SO4)3;
A与B的浓溶液混合时有刺激性气味的气体产生,同时有白色沉淀生成,且B显酸性,则B为(NH4)2CO3;
剩余离子为Na+和Cl-,C溶液显中性,所以C为NaCl,
综上可知:A为Ba(OH)2,B为(NH4)2CO3,C为NaCl,D为Al2(SO4)3,E为AgNO3;
(1)由上述分析可知D为Al2(SO4)3,A为Ba(OH)2,A中阴离子的电子式是 ,
,
故答案为:Al2(SO4)3; ;
;
(2)E为AgNO3,见光易分解,所以实验室保存在棕色试剂瓶中,置于冷暗处,
故答案为:保存在棕色试剂瓶中,置于冷暗处;
(3)B为(NH4)2CO3,实验测得B的溶液显碱性,则碳酸根离子水解程度大于铵根离子,所以(NH4)2CO3电离产生的阳离子与阴离子的物质的量浓度的比值大于2,
故答案为:大于;
(4)D为Al2(SO4)3,A为Ba(OH)2,1mol D与A反应生成沉淀的质量最大时,则反应为1molAl2(SO4)3与3molBa(OH)2反应生成沉淀为3molBaSO4和2molAl(OH)3,其质量为233×3g+78×2g=855g,
故答案为:855.
点评 本题考查无机物的推断,利用离子共存和离子反应推断物质为解答的关键,是高考的热点和难点,注意把握有特征的物质,然后结合推出的物质推导剩余的物质,最后进行验证即可,题目难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
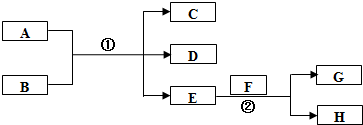
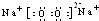 ;在反应②中,当生成2.24L的G(标准状况)时,反应转移的电子数目为0.2NA或1.024×1023.
;在反应②中,当生成2.24L的G(标准状况)时,反应转移的电子数目为0.2NA或1.024×1023.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
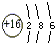 ;
; ;CO2的电子式
;CO2的电子式 ;NH4Cl的电子式
;NH4Cl的电子式 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如下:
合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如下:| 温 度(℃) | 360 | 440 | 520 |
| K值 | 0.036 | 0.010 | 0.0038 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该病毒主要通过血液向他人传染 | |
| B. | 该病毒在浓盐溶液中一定会发生变性 | |
| C. | 通常将病毒样本保存在福尔马林中 | |
| D. | 该病毒在一定条件下水解最终会生成氨基酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 溶液 | CH3COONa | Na2CO3 | Na2CO3 | HClO | C6H5ONa |
| PH | 8.8 | 9.7 | 11.6 | 10.3 | 11.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | B元素的最高化合价为+4价时,其负化合价也可能为-3价 | |
| B. | A(OH)n与HnEOm不能反应 | |
| C. | HnCOm为强酸时,HxDOy一定为强酸 | |
| D. | HnDOm为强酸时,E的非金属性一定很强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com