
 Cu2+ (aq) + 2Ag (s)��Ƴ�ԭ��أ�ijһʱ�̵ĵ����������ƣ�G��ָ��ƫת������ͼ��ʾ���й�������ȷ����
Cu2+ (aq) + 2Ag (s)��Ƴ�ԭ��أ�ijһʱ�̵ĵ����������ƣ�G��ָ��ƫת������ͼ��ʾ���й�������ȷ����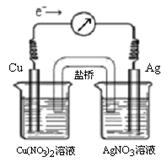
| A��KNO3�����е�K+����Cu(NO3)2��Һ |
| B����������ָ��Ϊ0ʱ���÷�Ӧ��ƽ�⣬ƽ�ⳣ��K=0 |
| C������ʱ��AgNO3��Һ�м���NaCl���壬����NaCl�������ӣ�������ָ������ƫת���ȼ�С��ָ��ָ��0������ƫת |
| D������ʱ��Cu(NO3)2��Һ�м���NaOH���壬����NaOH�������ӵ�����ָ������ƫת���ȼ�С��ָ��ָ��0������ƫת |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
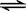 2HI(g)��K��50���ɴ��Ʋ���450��ʱ����Ӧ2HI(g)
2HI(g)��K��50���ɴ��Ʋ���450��ʱ����Ӧ2HI(g) 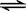 H2(g)��I2(g)�Ļ�ѧƽ�ⳣ��Ϊ
H2(g)��I2(g)�Ļ�ѧƽ�ⳣ��Ϊ| A��50 | B��0.02 | C��100 | D����ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A��H2(g)��I2(g)  2HI(g) ��H<0 2HI(g) ��H<0 |
B��4NH3(g)��5O2(g) 4NO(g)��6H2O(g) ��H<0 4NO(g)��6H2O(g) ��H<0 |
C��N2(g)��3H2(g)  2NH3(g)��H<0 2NH3(g)��H<0 |
D��2SO3(g) 2SO2(g)��O2(g) ��H>0 2SO2(g)��O2(g) ��H>0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 cZ(g) ��H��0����ƽ���������������ʱ������˵����ȷ����
cZ(g) ��H��0����ƽ���������������ʱ������˵����ȷ����| A�������¶ȣ�����Ӧ���������淴Ӧ���ʼ�С, ƽ�ⳣ������ |
| B����ͨ��ϡ������ƽ�ⲻ�ƶ�����a+b=c |
| C���������������Ӧ���ʸı䣬��ƽ�ⲻ�ƶ� |
| D��������X������ƽ�������ƶ���X��ת�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2SO3(g)�ﵽƽ��״̬�ı�־��______��
2SO3(g)�ﵽƽ��״̬�ı�־��______��| A����(O2)��=2��(SO2)�� |
| B�����������������������ʱ����仯 |
| C���������������ɫ����ʱ����仯 |
| D�������������ѹǿ����ʱ����仯 |
 2SO3(g) ��H<0������ͼ���в���ȷ����______ (����ĸ��ţ���
2SO3(g) ��H<0������ͼ���в���ȷ����______ (����ĸ��ţ���
 O2(g)
O2(g)  SO3(g) ��H=-98KJ/mol
SO3(g) ��H=-98KJ/mol�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
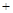 2H2(g)
2H2(g)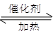 CH3OH(g)
CH3OH(g)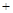 Q
Q| �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.270 | 0.012 |
 ����������Ҫ���COת���ʣ��ɲ�ȡ�Ĵ�ʩ
����������Ҫ���COת���ʣ��ɲ�ȡ�Ĵ�ʩ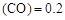 mol��L������CH3OH��ʾ�ķ�Ӧ����v
mol��L������CH3OH��ʾ�ķ�Ӧ����v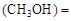 mol /(L��min)��
mol /(L��min)��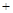 CO2(g)
CO2(g)  2CO(g) ƽ�ⳣ��K1
2CO(g) ƽ�ⳣ��K1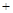 H2O(g)
H2O(g)  CO(g)
CO(g)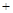 H2(g) ƽ�ⳣ��K2
H2(g) ƽ�ⳣ��K2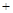 H2O(g)
H2O(g)  H2(g)
H2(g)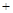 CO2(g) ƽ�ⳣ��K3
CO2(g) ƽ�ⳣ��K3�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
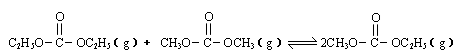 ��̼��������Ĺ�ҵ����ԭ������ͼ��Ͷ�ϱ�[
��̼��������Ĺ�ҵ����ԭ������ͼ��Ͷ�ϱ�[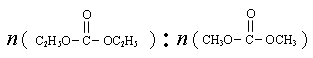 ]�ֱ�Ϊ3�U1��1�U1����Ӧ��������ʵ�����ͬʱ��
]�ֱ�Ϊ3�U1��1�U1����Ӧ��������ʵ�����ͬʱ�� ��ƽ��ת�������¶ȵĹ�ϵ���ߡ�����˵����ȷ����
��ƽ��ת�������¶ȵĹ�ϵ���ߡ�����˵����ȷ����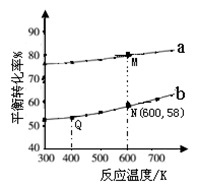
| A������b����Ӧ��Ͷ�ϱ�Ϊ3�U1 |
| B��M���Ӧ��ƽ�ⳣ��С��Q�� |
| C��N���Ӧ��ƽ��������̼������������ʵ�������Ϊ0.58 |
| D��M���Q���Ӧ��ƽ��������������ʵ���֮��Ϊ2�U1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 xC(g)��H=-192kJ��mol-1,��M��N�ж�ͨ��1molA��2molB�Ļ�����壬��ʼM��N�ݻ���ͬ�������¶Ȳ��䡣����˵����ȷ���� ( )
xC(g)��H=-192kJ��mol-1,��M��N�ж�ͨ��1molA��2molB�Ļ�����壬��ʼM��N�ݻ���ͬ�������¶Ȳ��䡣����˵����ȷ���� ( )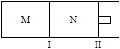
| A����x=3���ﵽƽ���A�����������ϵΪ����(M)>��(N) |
| B����x>3���ﵽƽ���B��ת���ʹ�ϵΪ����(M)>��(N) |
| C����x<3��C��ƽ��Ũ�ȹ�ϵΪ��c(M)>c(N) |
| D��x����Ϊ��ֵ����ʼʱ��N�����г�������ֵ��C��ƽ���N������A��Ũ�Ⱦ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2C(g) �ﵽƽ��ģ� ��
2C(g) �ﵽƽ��ģ� ��A��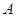 �� ��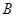 �� ��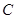 ��Ũ��֮��Ϊ1:2:2 ��Ũ��֮��Ϊ1:2:2 |
B����λʱ�������� ��ͬʱ����2a mol C ��ͬʱ����2a mol C |
C��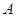 ��Ũ�Ȳ��ٱ仯 ��Ũ�Ȳ��ٱ仯 |
| D��������������ʵ���Ϊ2a mol |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com