
【题目】检验某溶液中是否含有Na+、K+、Fe3+、Mg2+、Cl-、I-、CO32-、SO42-,限用试剂有:盐酸、硫酸、硝酸钡溶液、硝酸银溶液。设计如下实验步骤,并记录相关现象:
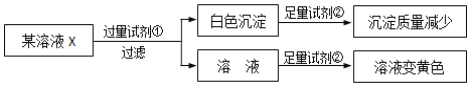
(已知,NO3-在酸性条件下具有强氧化性)
下列叙述不正确的是
A. 试剂①为硝酸钡
B. 试剂②一定为盐酸
C. 该溶被中一定有I-、CO32-、SO42-;Na+、K+至少含有一种
D. 通过在黄色溶液中加入硝酸银可以检验原溶液中是否存在C1-
【答案】D
【解析】
由实验可知,加试剂①为硝酸钡溶液,生成白色沉淀为碳酸钡和硫酸钡,则加试剂②为盐酸,沉淀减少,硫酸钡不溶于酸;加试剂①过滤后的滤液中,再加试剂②为盐酸,氢离子,硝酸根离子、I-发生氧化还原反应生成碘,溶液为黄色,以此来解答。
由实验可知,加试剂①为硝酸钡溶液,生成白色沉淀为碳酸钡和硫酸钡,则加试剂②为盐酸,沉淀减少,硫酸钡不溶于酸,则原溶液中一定存在CO32-、SO42-,则不含Fe3+、Mg2+;加试剂①过滤后的滤液中,再加试剂②为盐酸,氢离子,硝酸根离子、I-发生氧化还原反应生成碘,溶液为黄色,溶液为电中性,则一定含阳离子为K+,A.由上述分析可知,试剂①为硝酸钡,选项A正确;B.由上述分析可知,试剂②一定为盐酸,因碳酸钡与硫酸反应生成硫酸钡使沉淀量增加,选项B正确;C.由上述分析可知,该溶液中一定有I-、CO32-、SO42- 、Na+、K+至少含有一种,选项C正确;D.黄色溶液中加入硝酸银可生成AgI沉淀,试剂②加盐酸引入氯离子,不能检验原溶液中是否存在Cl-,选项D不正确;答案选D。


 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:
【题目】钠离子电池开始成为下一轮电池研究的重点,下图是一种可充电钠离子电池(电解质溶液为Na2SO3溶液) 工作时的示意图。下列说法正确的是
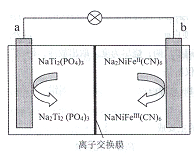
A. 电池放电时,Na+从a极区移动到b极区
B. 电池充电时,b极区发生的反应是:NaNiFeIII(CN)6+ e—+Na+=Na2NiFeII(CN)6
C. 金属钠可以作为该电池的负极材料
D. 若用该电池电解饱和食盐水,理论上每生成1molCl2,电池内有,1molNa+通过间子交换膜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气(主要成分为NOx和CO)已成为主要的空气污染物来源之一,有发生光化学烟雾污染的潜在危险。
(1)某小组同学为研究光化学烟雾的形成进行了模拟实验。测得烟雾的主要成分为CxHy(烃)、NO、NO2、O3、PAN (CH3COOONO2),各种物质的相对浓度随时间的变化如右图。根据图中数据,下列推论最不合理的是_____。(填选项序号字母)

a.NO的消失的速率比CxHy快 b.NO生成NO2
c.CxHy及NO2可以生成PAN及O3 d.O3生成PAN
(2)一定条件下,将2 mol NO与2 mol O2置于恒容密闭容器中发生反应2NO(g)+O2(g) ![]() 2NO2(g),下列可判断反应达平衡的是_____。(填选项序号字母)
2NO2(g),下列可判断反应达平衡的是_____。(填选项序号字母)
a.体系压强保持不变 b.混合气体密度保持不变
c.NO和O2的物质的量之比保持不变 d.每消耗2 mol NO同时生成2 mol NO2
(3)高温下N2和O2发生N2(g)+O2(g)![]() 2NO(g)反应,是导致汽车尾气中含有NO的原因之一。
2NO(g)反应,是导致汽车尾气中含有NO的原因之一。
①右图是T1、T2两种不同温度下,一定量的NO发生分解过程中N2的体积分数随时间变化的图像,据此判断反应N2(g)+O2(g)![]() 2NO(g)为_____(填“吸热”或“放热”)反应。
2NO(g)为_____(填“吸热”或“放热”)反应。

②2000℃时,向容积为2 L的密闭容器中充入10 mol N2与5 mol O2,达到平衡后NO的物质的量为2 mol,则此刻反应的平衡常数K=_____。该温度下,若开始时向上述容器中充入N2与O2均为1 mol,则达到平衡后N2的转化率为_____。

③汽车净化装置里装有含Pd化合物的催化剂,气体在催化剂表面吸附与解吸作用的机理如右图所示。写出其变化的总化学反应方程式:_____。
(4)为减少汽车尾气中NOx的排放,常采用CxHy(烃)催化还原NOx消除氮氧化物的污染。
例如:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ/mol
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH2
若16 g CH4还原NO2至N2,共放出热量867 kJ,则ΔH2=_____。若用标准状况下4.48 L CH4还原NO2至N2,共转移的电子总数为_____(阿伏加德罗常数的值用NA表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于胶体和溶液的说法中,正确的是( )
A.胶体粒子的直径大于100nm
B.用过滤的方法可以分离胶体和溶液
C.光线通过时,胶体产生丁达尔效应,溶液则无丁达尔效应
D.将饱和氯化铁溶液滴入稀氢氧化钠溶液中加热,可得氢氧化铁胶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NaHSO3溶液显酸性,溶液中存在以下平衡:①HSO3-+ H2O![]() H2SO3+OH- ;②HSO3-
H2SO3+OH- ;②HSO3-![]() H++SO32-
H++SO32-
向0.1mol·L-1的NaHSO3溶液中分别加入以下物质,下列有关说法正确的是
A. 加入少量金属Na,平衡①左移,平衡②右移,溶液中[HSO3-]增大
B. 加入少量Na2SO3固体,则[H+]+[Na+]=[HSO3-]+[OH-]+![]() [SO32-]
[SO32-]
C. 加入少量NaOH溶液,  、
、 的值均增大
的值均增大
D. 加入氨水至中性,则2[Na+]=[SO32-]>[H+]=[OH-]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色透明溶液,在酸性环境下能大量共存的离子组是( )
A.Na+、SO42-、CO32-、Cl-
B.Mg2+、Cl-、Na+、NO3-
C.K+、MnO4-、NO3-、Fe2+
D.Cu2+、Cl-、H+、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中水既不是氧化剂,又不是还原剂的氧化还原反应是( )
A.SO3+H2O=H2SO4
B.2Na2O2+2H2O=4NaOH+O2↑
C.2F2+2H2O=4HF+O2
D.NaH+H2O=NaOH+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,下列有关两种溶液的说法不正确的是
序号 | ① | ② |
pH | 12 | 12 |
溶液 | 氨水 | 氢氧化钠溶液 |
A.①②两溶液中c(OH-)相等
B.①溶液的物质的量浓度为0.01mol·L-1
C.①②两溶液分别加水稀释10倍,稀释后溶液的pH:①>②
D.等体积的①②两溶液分别与0.01 mol·L-1的盐酸完全中和,消耗盐酸的体积:①>②
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com