
【题目】酸、碱、盐都是电解质,在水中都能电离出离子。根据下列化合物:①NaOH ②CH3COOH ③NH4Cl ④NH3·H2O ⑤CH3COONa,请回答下列问题:
(1)上述几种电解质中属于弱电解质的是______________
(2)常温下pH=2的CH3COOH溶液中由水电离产生的 c(OH-) =_____________________
(3)写出CH3COOH的电离方程式_______________________
(4)将等pH等体积的NaOH和NH3·H2O分别稀释m倍和n倍,稀释后两溶液的pH仍相等,则m ___________n (填“大于、等于或小于”)
(5)pH=12的NaOH溶液100mL,要使它的pH为11,如果加0.01mol/L HCl,应加_______mL。(体积变化忽略不计)
【答案】②④ 10-12mo1/L CH3 COOH![]() CH3COO—+H+ 小于 81.8
CH3COO—+H+ 小于 81.8
【解析】
(1)弱电解质是在水溶液中不能完全电离的电解质,包括弱酸、弱碱、水等,所以②CH3COOH、④NH3H2O是弱电解质;
答案为:②④;
(2)常温下pH=2的CH3COOH溶液中c(H+)=1.0×10-2mol/L,醋酸溶液中的氢氧根离子来自于水的电离,由水电离产生的 c(OH-) = mol/L;
mol/L;
答案为:10-12mo1/L
(3) CH3COOH为弱电解质,部分电离,电离方程式![]() ;
;
答案为:![]()
(4)氨水是弱电解质,氢氧化钠是强电解质,氨水存在电离平衡,氢氧化钠不存在电离平衡,将等pH等体积的NaOH和NH3·H2O分别稀释m倍和n倍,稀释后两溶液的pH仍相等,则氢氧化钠的稀释倍数小于氨水,
答案为:小于;
(5) 盐酸的浓度是0.01mol/L,设加入盐酸的体积是V,c(OH)= =
=![]() =0.001mol/L,解得:V=81.8mL,
=0.001mol/L,解得:V=81.8mL,
故答案为:81.8;


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】已知AG=lg![]() ,电离度α=
,电离度α=![]() ×100%。常温下,向10mL0.1mol/LHX溶液中滴加0.1mol/LNaOH溶液,混合溶液中AG与滴加NaOH溶液体积的关系如图所示。
×100%。常温下,向10mL0.1mol/LHX溶液中滴加0.1mol/LNaOH溶液,混合溶液中AG与滴加NaOH溶液体积的关系如图所示。
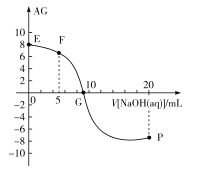
下列说法错误的是( )
A.F点溶液pH<7
B.G点溶液中c(Na+)=c(X-)>c(H+)=c(OH-)
C.V=10时,溶液中c(OH-)<c(HX)
D.常温下,HX的电离度约为1%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cu、Zn及其化合物在生产、生活中有着重要作用。请回答:
(1)Cu、Zn在周期表中________区,焰色反应时Cu的4s电子会跃迁至4p轨道,写出Cu的激发态电子排布式___________。
(2)分别向CuSO4、MgSO4溶液加氨水至过量,前者为深蓝色溶液,后者为白色沉淀。
①NH3与Cu2+形成配合物的能力大于Mg2+的原因为_________________。
②溶液中的水存在H3O+、![]() 等微粒形式,
等微粒形式,![]() 可看作是H3O+与H2O通过氢键形成的离子,则
可看作是H3O+与H2O通过氢键形成的离子,则![]() 的结构式为___________。
的结构式为___________。
(3)Zn的某种化合物M是很好的补锌剂,结构式如图:

①1 mol M含有的σ键的数目为___________。
②常见含氮的配体有 H2NCH2 COOˉ、NH3、![]() 等,NH3的分子空间构型为____________,
等,NH3的分子空间构型为____________,![]() 的中心氮原子杂化方式为__________。
的中心氮原子杂化方式为__________。
③M在人体内吸收率高的原因可能是锌形成配合物后,电荷__________(填“变多”“变少”或“不变”),可在消化道内维持良好的稳定性。
(4)卤化锌的熔点如表:
卤化锌/ ZnX2 | ZnF2 | ZnCl2 | ZnBr2 |
熔点/℃ | 872 | 283 | 394 |
则ZnX2熔点如表变化的原因是____________________。
(5)Zn的某种硫化物的晶胞如图所示。已知S2-和Zn2+的半径分别为r1 pm、r2 pm,且S2-与Zn2+相切,NA为阿伏加德罗常数的值。则该晶体的密度为________g·cm-3(写计算表达式)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下0.1molL﹣1醋酸溶液的pH=a,下列能使溶液pH=(a+1)的措施是
A. 将溶液稀释到原体积的2倍B. 加入适量的醋酸钠固体
C. 加入等体积0.2 molL﹣1盐酸D. 加少量冰醋酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】800℃时,在2 L密闭容器中发生反应:2NO(g)+O2(g)![]() 2NO2(g),该反应体系中n(NO)随时间的变化如下表:
2NO2(g),该反应体系中n(NO)随时间的变化如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.022 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
下列有关说法不正确的是
A. 用氧气表示0~3 s内该反应的平均速率ν(O2)=0.0025 mol·L-1·s-1
B. 容器内颜色保持不变时,说明该反应达到平衡状态
C. 增大氧气的浓度,既加快反应速率,又使平衡正向移动
D. 该反应达到平衡时,转移电子总数为0.03NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.H2(g)+I2(g)![]() 2HI(g),平衡后,减压平衡不移动,气体颜色不变
2HI(g),平衡后,减压平衡不移动,气体颜色不变
B.H2(g)+I2(g)![]() 2HI(g),平衡后,加压平衡不移动,气体颜色不变
2HI(g),平衡后,加压平衡不移动,气体颜色不变
C.2NO2(g)![]() N2O4(g),平衡后,加压平衡正向移动,气体颜色变浅
N2O4(g),平衡后,加压平衡正向移动,气体颜色变浅
D.2NO2(g)![]() N2O4(g),平衡后,加压平衡正向移动,气体颜色先变深后变浅
N2O4(g),平衡后,加压平衡正向移动,气体颜色先变深后变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①N2(g)+2O2(g)![]() 2NO2(g) △H=+67.7kJ/mol
2NO2(g) △H=+67.7kJ/mol
②2N2H4(g)+2O2(g)![]() 2N2(g)+4H2O(g) △H=-1068kJ/mol
2N2(g)+4H2O(g) △H=-1068kJ/mol
(1)火箭发射时可用肼(N2H4)作燃料,以二氧化氮作氧化剂,它们相互反应生成氮气和水蒸气。根据盖斯定律写出N2H 4和NO2反应的热化学方程式为____;
(2)肼(N2H4)和氧气反应的能量变化如图所示,图中E1表示___,E2表示____,△H=-534kJ/mol表示_____。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示___________,K值大小与温度的关系是:温度升高,K值_________(填一定增大、一定减小、或可能增大也可能减小)。
(2)对于可逆反应CO(g) +H2O(g) ![]() CO2(g)+H2(g) △H<0在850℃时,KC=1 该反应的平衡常数K的表达式为K=______;若温度为900℃,达到平衡后KC_____1 (填“>“<”=)
CO2(g)+H2(g) △H<0在850℃时,KC=1 该反应的平衡常数K的表达式为K=______;若温度为900℃,达到平衡后KC_____1 (填“>“<”=)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了验证卤素单质氧化性的相对强弱,某小组用如图所示装置进行实验(夹 持仪器已略去,气密性已检验)。

实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹.。
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a。
Ⅳ.…
(1)A中反应的化学方程式为:KMnO4+HCl(浓)=KCl+MnCl2+Cl2↑+H2O,则氧化性KMnO4____Cl2(填“>”“<”或“=”)。
(2)验证氯气的氧化性强于碘的实验现象是____。
(3)过程Ⅲ的实验目的是____。
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是____。
(5)浸有NaOH溶液的棉花团的作用是____。此处发生的化学方 程式是____。
(6)氰(CN)2、硫氰(SCN)2的化学性质和卤素很相似,化学上称为“类卤素”,它们单质氧化性强弱为:Cl2>Br2>(CN)2>(SCN)2>I2。试写出:在NaBr和KSCN的混合溶液中加入(CN)2的化学方程式:____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com