
分析 (1)废覆铜板(Cu和Sn组成)可用CuSO4和H2SO4混合溶液作电解质溶液,直接电解回收精铜,阳极为活性电极本身失电子发生氧化反应;
(2)①用FeCl3溶液浸取铜是氯化铁和铜反应生成氯化亚铜和氯化亚铁;若加盐酸不足,反应一段时间后线路板表面有红褐色沉淀是因为氢离子浓度小的溶液中铁离子会水解生成氢氧化铁红褐色沉淀;
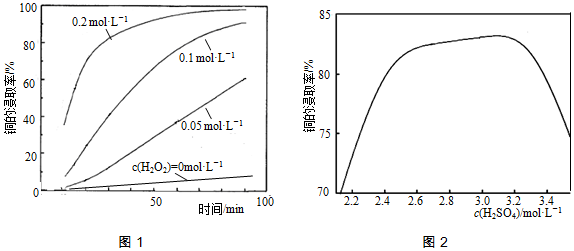
②当c(H2O2)=0mol•L-1时,液面上方空气中O2随搅拌不断进入溶液,溶解的O2将铜氧化而被浸取;
③a.依据浸取过程发生反应与钠离子无关解答;
b.依据方程式(Ⅱ) Cu2++Cu?2Cu+,判断;
c.依据方程式(Ⅲ) Cu++nCl-?CuCln(n-1)-,判断;
d.氢氧根离子能够与氢离子、铜离子反应;
(3)①Cu2S在盐酸的酸性环境下被过氧化氢生成硫酸铜、氯化铜和水;
②硫酸容易与铅离子反应生成硫酸铅沉淀,附着在铅冰铜颗粒表面,阻止反应的进行.
解答 解:(1)电解法精炼铜,阳极为活性电极,电极本身参与放电,铜失去电子发生氧化反应,电极反应式:Cu-2e-=Cu2+;锡失去电子生成锡离子,电极反应式:Sn-2e-=Sn2+;
故答案为:Cu-2e-=Cu2+ 和Sn-2e-=Sn2+;
(2)①三价铁离子能够氧化铜生成铜离子,本身被还原为二价铁离子,离子方程式:2Fe3++Cu=2Fe2++Cu2+;
若加盐酸不足,溶液中氢离子浓度较小,三价铁离子水解生成氢氧化铁,所以若加盐酸不足,反应一段时间后线路板表面有红褐色沉淀;
故答案为:2Fe3++Cu=2Fe2++Cu2+;
c(H+)和c(Fe3+)小,有利于Fe3+水解生成Fe(OH)3沉淀;
②当c(H2O2)=0mol•L-1时,液面上方空气中O2随搅拌不断进入溶液,溶解的O2将铜氧化而被浸取,所以也有少量的铜被浸出;
故答案为:液面上方空气中O2随搅拌不断进入溶液,溶解的O2将铜氧化而被浸取;
③a.依据给出的方程式可知,上述反应与钠离子都无关,所以改变钠离子的浓度,不影响Cu从废电路板中浸出,故a不选;
b.由Cu2++Cu?2Cu+可知增大铜离子浓度,上述反应的速率加快,故b选;
c.由Cu++nCl-?CuCln(n-1)-可知增大Cl-浓度,反应Ⅲ加快,故c选;
d.氢氧根离子能够与氢离子、铜离子反应,增大氢氧根离子浓度,能够使氢离子、铜离子浓度减小,反应速率减慢,故d不选;
故选:bc;
(3)①Cu2S在盐酸的酸性环境下被过氧化氢生成硫酸铜、氯化铜和水,依据得失电子守恒,原子个数守恒反应的方程式为:Cu2S+5H2O2+2HCl=CuCl2+CuSO4+6H2O;
故答案为:Cu2S+5H2O2+2HCl=CuCl2+CuSO4+6H2O;
②由H2SO4代替HCl-H2O2中的HCl,其他条件相同,铜的浸取率随硫酸浓度的变化如图2所示.当H2SO4浓度大于3.1mol•L-1时,过量的硫酸会生成PbSO4沉淀包裹在铅冰铜颗粒表面,使铜无法与浸出液接触,使得硫酸浓度越大,铜的浸取率反而越小;
故答案为:过量的硫酸会生成PbSO4沉淀包裹在铅冰铜颗粒表面,使铜无法与浸出液接触;
点评 本题考查了电解法精炼铜电极反应书写、氧化还原反应方程式的书写、水解平衡移动的影响因素等,熟悉电解池工作原理,盐类水解规律及影响因素,明确氧化还原反应得失电子守恒是解题关键,题目综合性强,难度较大.


科目:高中化学 来源: 题型:多选题
| A. | 一定温度下,反应MgCl2(l)=Mg(l)+Cl2(g)的△H>0、△S>0 | |
| B. | 水解反应NH4++H2O?NH3•H2O+H+达到平衡后,升高温度平衡逆向移动 | |
| C. | AlCl3溶液蒸干、灼烧至恒重,最终剩余固体是AlCl3 | |
| D. | 对于反应2H2O2=2H2O+O2↑,加入MnO2或升高温度都能加快O2的生成速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用100 mL量筒量取12.5 mL盐酸 | |
| B. | 用托盘天平称量5.85g食盐 | |
| C. | 需用220 mL 1 mol•L-1 CuSO4溶液,配制时需称62.5g 的CuSO4•5H2O 晶体 | |
| D. | 所配得的500 mL 0.5mol•L-1 Na2CO3溶液中,Na+的物质的量浓度为0.5mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
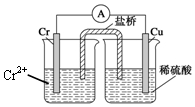 金属铬和氢气在工业上都有重要的用途.已知:铬能与稀硫酸反应,生成氢气和硫酸亚铬(CrSO4).铜铬构成原电池如图所示,盐桥中装的是饱和KCl琼脂溶液,下列关于此电池的说法正确的是( )
金属铬和氢气在工业上都有重要的用途.已知:铬能与稀硫酸反应,生成氢气和硫酸亚铬(CrSO4).铜铬构成原电池如图所示,盐桥中装的是饱和KCl琼脂溶液,下列关于此电池的说法正确的是( )| A. | 盐桥的作用是使整个装置构成通路、保持溶液呈电中性,凡是有盐桥的原电池,盐桥中均可以用饱和KCl琼脂溶液 | |
| B. | 理论上1molCr溶解,盐桥中将有2molCl-进入左池,2molK+进入右池 | |
| C. | 此过程中H+得电子,发生氧化反应 | |
| D. | 电子从铬极通过导线到铜极,又通过盐桥到转移到左烧杯中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
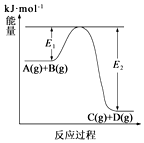
| A. | 上述反应为吸热反应 | B. | 上述反应的△H=E1kJ•mol-1 | ||
| C. | A(g)的能量一定大于C(g) | D. | 反应物的总焓大于反应产物的总焓 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com