
 �ϲ��뺣�����ƣ���һ�ָ��������ĺ���ֲ���Ʒ�ϲ��ᱡ�ɴࡢ�Ⱥ������ױ����ճɻң���ʱ��ת��Ϊ�⻯�����Σ������ڵⵥ�ʵ���ȡ��
�ϲ��뺣�����ƣ���һ�ָ��������ĺ���ֲ���Ʒ�ϲ��ᱡ�ɴࡢ�Ⱥ������ױ����ճɻң���ʱ��ת��Ϊ�⻯�����Σ������ڵⵥ�ʵ���ȡ��| �Ҵ� | ���Ȼ�̼ | �⣨���壩 | |
| �ܶ�/g•cm-3 | 0.7893 | 1.595 | 4.94 |
| �е�/�� | 78.5 | 76.8 | 184.35 |
 ��
�� ���� ��1��ʵ�����б����ϲˣ���Ϊ�ϲ��ǹ��壬Ҫ���������м��ȣ�����Ҫ�õ����������������ƾ��ơ����żܡ������ǵȣ�
��2���������õ��ϲ˻���Ҫ���е����ӣ���������˫��ˮ��ϡ�������ã��ᷢ��������ԭ��Ӧ������ʽΪ��2I-+H2O2+2H+=I2+2H2O��
��3�������ݺ��ϲ˻Һ���Һ�Ļ������˳�ȥ���ʣ����º������ӵ���Һ�ڷ�Һ©���м�����ȡ������ȡ��ˮ�еĵ⣬ѡ���Ȼ�̼����ȡ������Ϊ�Ҵ���ˮ���ܣ����ʺ�����ȡ����
���Ȼ�̼������ˮ��������ȡ�����ѵⵥ�ʴ�ˮ����ȡ�����Ȼ�̼��Һ�У��ֲ���ܽ�ⵥ�ʵ����Ȼ�̼���²㣻
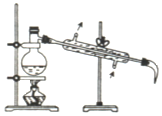
��4��Ϊ��ʵ��ʵ��Ŀ�ģ�ͼ��ȱ���¶ȼơ�����Һ���װ�á���ʯ��������ˮԡ����װ�ú��¶ȼƣ�
��� �⣺��1��ʵ�����б����ϲˣ���Ϊ�ϲ��ǹ��壬Ҫ���������м��ȣ�����Ҫ�õ����������������ƾ��ơ����żܡ������ǵȣ�
�ʴ�Ϊ��DFGH��
��2���������õ��ϲ˻���Ҫ���е����ӣ���������˫��ˮ��ϡ�������ã��ᷢ��������ԭ��Ӧ������ʽΪ��2I-+H2O2+2H+=I2+2H2O��Ŀ���ǽ���Һ�е�I-ת��ΪI2��
�ʴ�Ϊ������Һ�е�I-ת��ΪI2��
��3�������ݺ��ϲ˻Һ���Һ�Ļ����������ͨ�����˳��ӣ��õ��������ӵ���Һ����Ϊ�Ҵ���ˮ���ܣ����ʺ�����ȡ�������Ȼ�̼������ˮ��������ȡ������Ҫ�ǰѵⵥ�ʴ�ˮ����ȡ�����Ȼ�̼��Һ�У�Ȼ���ٷ�Һ�����ڷ�Һʱ�²�Һ����¿ڷų����ϲ�Һ��Ҫ���Ͽڵ�����
�ʴ�Ϊ�����ˣ���Һ©�������Ȼ�̼����ɫ�²�Һ�壻
��5��Ϊ��ʵ��ʵ��Ŀ�ģ�ͼ��ȱ���¶ȼơ�����Һ���װ�á���ʯ��������ˮԡ����װ�ú��¶ȼƣ�װ����ͼ ��
��
�ʴ�Ϊ�� ��
��
���� �����Ե����ȡΪ���壬������ѧ���Ի����ķ����ᴿ�����������ͬʱ������������ԭ��Ӧ����д����Ŀ�ѶȲ������ջ����ǽ���ؼ���


 �¿α�ͬ��ѵ��ϵ�д�
�¿α�ͬ��ѵ��ϵ�д� һ����ʦ����Ӧ����������һ��ȫϵ�д�
һ����ʦ����Ӧ����������һ��ȫϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ͨ��Ĥ��ؿɳ�ȥ��ˮ�е������ƺͶ��ȱ��ӣ�
ͨ��Ĥ��ؿɳ�ȥ��ˮ�е������ƺͶ��ȱ��ӣ�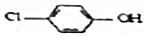 ������ԭ����ͼ��ʾ������˵����ȷ���ǣ�������
������ԭ����ͼ��ʾ������˵����ȷ���ǣ�������| A�� | BΪ��ص�������������ԭ��Ӧ | |
| B�� | ���������B���ص��߾�С��������A�� | |
| C�� | A���ĵ缫��ӦʽΪ +e-�TCl-+ +e-�TCl-+ | |
| D�� | �����·����0.2mole-ת��ʱ��A�������ӵ�H+����ĿΪ0.1NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
 ij��ѧ����С���ͬѧ����ԭ���ԭ��̽��һ���¶��£�ʵ��ʱʵ�ʵĻ����¶ȣ�ʹ���ۻ�����������Ũ�ȣ�
ij��ѧ����С���ͬѧ����ԭ���ԭ��̽��һ���¶��£�ʵ��ʱʵ�ʵĻ����¶ȣ�ʹ���ۻ�����������Ũ�ȣ�| ʵ����� | ʵ���¶ȣ��棩 | ע��ˮ�������mL�� |
| 1 | 17.2 | 2.4 |
| 2 | T1 | 2.5 |
| 3 | T2 | 2.3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
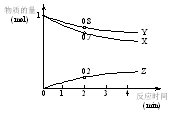 ij�����£���2L�ܱ������У�X��Y��Z������������ʵ�����ʱ��ı仯������ͼ��ʾ�������й�˵������ȷ���ǣ�������
ij�����£���2L�ܱ������У�X��Y��Z������������ʵ�����ʱ��ı仯������ͼ��ʾ�������й�˵������ȷ���ǣ�������| A�� | ��Ӧ2minĩX��Ũ��Ϊ0.35mol/L | |
| B�� | �÷�Ӧ�Ļ�ѧ����ʽ�ɱ�ʾΪ��2Z?2Y+3X | |
| C�� | ��Ӧ2min����ZŨ�ȱ仯��ʾ��ƽ����Ӧ����Ϊ0.05mol/��L•min�� | |
| D�� | �κ�ʱ����Z��YŨ�ȱ仯��ʾ�ķ�Ӧ���ʹ�ϵ���Ϧ���Z��=����Y�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
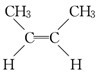 ��
��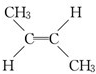 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
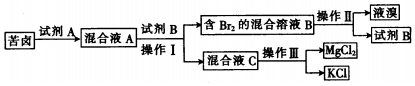
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| �� | �� | �� | �� | ||
| �ܱ��������/L | 2 | 2 | 2 | 1 | |
| ��ʼ���ʵ��� | n��SO2��/mol | 0.4 | 0.8 | 0.8 | 0.4 |
| n��O2��/mol | 0.24 | 0.24 | 0.48 | 0.24 | |
| SO2��ƽ��ת����/% | 80 | a1 | a2 | a3 | |
| A�� | ���¶��£��÷�Ӧ��ƽ�ⳣ��KΪ400 | |
| B�� | SO2��ƽ��ת���ʣ�a1��a2=a3 | |
| C�� | �ﵽƽ��ʱ���������е�����Ӧ���ʱ��������еĴ� | |
| D�� | �ﵽƽ��ʱ����������c�� SO3��������������c�� SO3�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | 0.1mol•L-1NaHC2O4��Һ��pH=5.5����c��Na+����c��HC2O4-����c��H2C2O4����c��C2O42-�� | |
| B�� | 0.1mol•L-1NaHS��Һ��c��OH-��+c��S2-���Tc��H+��+c��H2S�� | |
| C�� | 0.1mol•L-1CH3COOH��Һ��0.1mol•L-1CH3COONa��Һ�������ϣ�c��Na+����c��CH3COOH����c��CH3COO-����c��H+����c��OH-�� | |
| D�� | 0.1mol•L-1NH4HSO4��Һ�еμ�0.1mol•L-1NaOH��Һ�����ԣ�c��Na+����c��SO42-����c��NH4+����c��OH-��=c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| W | Q | ||
| X | Y |
| A�� | �����Ӱ뾶��X��Q | B�� | ��̬�⻯����ȶ��ԣ�Y��Q | ||
| C�� | X������������������ | D�� | Y�������Ӧˮ������ǿ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com