
 SO2通入BaCl2溶液中并不产生沉淀,而通入另一种气体后可以产生白色沉淀.则图中右侧Y形管中放置的药品组合不符合要求的是(必要是可以加热)( )
SO2通入BaCl2溶液中并不产生沉淀,而通入另一种气体后可以产生白色沉淀.则图中右侧Y形管中放置的药品组合不符合要求的是(必要是可以加热)( )| A、Cu和浓硝酸 |
| B、CaO和浓氨水 |
| C、大理石和稀盐酸 |
| D、高锰酸钾溶液和浓盐酸 |


科目:高中化学 来源: 题型:
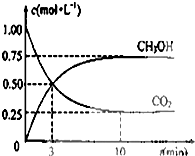 由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视.目前工业上有一种方法是用CO2生产燃料甲醇,一定条件下发生如下反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视.目前工业上有一种方法是用CO2生产燃料甲醇,一定条件下发生如下反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)查看答案和解析>>
科目:高中化学 来源: 题型:
| A、60mL | B、40mL |
| C、30mL | D、15mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应后的溶液一定c(NH4+)<c(Cl-) |
| B、盐酸的物质的量浓度一定小于氨水的物质的量浓度 |
| C、反应后生成的盐溶液一定没有发生水解 |
| D、盐酸中HCl的物质的量一定等于NH3?H2O的物质的量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
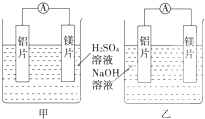 某探究活动小组想利用原电池反应检测金属的活动性顺序,有甲、乙两位同学均使用镁片与铝片作电极,但甲同学将电极放入6mol?L-1稀H2SO4中,乙同学将电极放入6mol?L-1的NaOH溶液中,如图所示.
某探究活动小组想利用原电池反应检测金属的活动性顺序,有甲、乙两位同学均使用镁片与铝片作电极,但甲同学将电极放入6mol?L-1稀H2SO4中,乙同学将电极放入6mol?L-1的NaOH溶液中,如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| A、-131.5kJ?mol-1 |
| B、+352.5kJ?mol-1 |
| C、-352.5kJ?mol-1 |
| D、+131.5kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | 所含杂质 | 除去杂质的试剂或方法 | |
| A | KNO3溶液 | KOH | H滴入稀HNO3的同时用pH试纸测定至溶液呈中性 |
| B | FeSO4溶液 | CuSO4 | 加入过量铁粉并过滤 |
| C | H2 | CO2 | 依次通过盛有NaOH溶液和浓硫酸的洗气瓶 |
| D | NaNO3 | CaCO3 | 加稀盐酸溶液、过滤、蒸发、结晶 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com