
【题目】除去镁粉中混有的少量铝粉, 可选用的试剂是
A. 盐酸 B. NaOH溶液 C. 硝酸 D. 食盐水
科目:高中化学 来源: 题型:
【题目】认识有机物相关问题
(1)有机物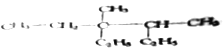 的系统命名为________________。
的系统命名为________________。
(2)有机物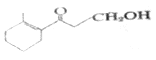 的分子式为_____________。所含的含氧官能团的名称为___________。
的分子式为_____________。所含的含氧官能团的名称为___________。
(3)根据题意,将下列正确的组号填写在空格上
①金刚石与“足球烯”;②氧气(O2)与臭氧(O2)
③16O、17O、18O;④CH4和CH3CH3CH3;
⑤乙烯和乙烷⑥![]() 和
和![]() ⑦
⑦![]() 和
和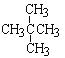
⑧D和T⑨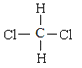 和
和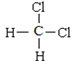 ⑩
⑩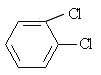 和
和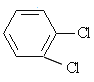
是同分异构体的是__________________。
(4)有机物A的分子式为C6H12O,其核磁共振氢谱如图A所示。有机物B的分子式为C2H6Br3,核磁共振氢谱如图B所示
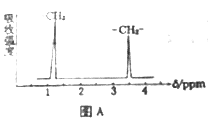

A的结构简式为:_____________,B的结构简式为:____________________;
(5)分子式C6H12的化合物有多种同分异构体,其中有一种同分异构体中所有碳原子都在同一平面上,则该烃的结构简式为:_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(13分)【[化学—有机化学基础】没食子酸丙酯简称PG,结构简式为 ,是白色粉末,难溶于水,微溶于棉子油等油脂,是常用的食用油抗氧化剂。
,是白色粉末,难溶于水,微溶于棉子油等油脂,是常用的食用油抗氧化剂。
(1)PG的分子式为 ,请写出PG分子中所含官能团的名称 ,1molPG与足量氢氧化钠溶液完全反应时,消耗的氢氧化钠的物质的量是 。
PG可发生如下转化:
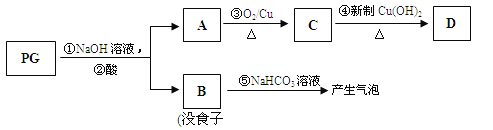
(2)A的结构简式为 ,1mol没食子酸最多可与 mol H2 加成。
(3)上图的有关变化中,属于氧化反应的有(填序号) 。
(4)从分子结构或性质上看,PG具有抗氧化作用的主要原因是(填序号) 。
a.含有苯环 b.含有羧基 c.含有酚羟基 d.微溶于食用油
(5)反应④的化学方程式为: 。
(6)B有多种同分异构体,写出其中符合下列要求的同分异构体的结构简式: 。
i.含有苯环,且苯环上的一溴代物只有一种;
ii.既能发生银镜反应,又能发生水解反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是( )
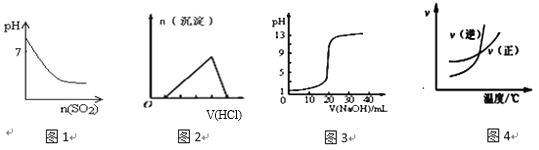
A. 图1表示将SO2气体通入溴水中,所得溶液的pH变化
B. 图2表示向含有少量氢氧化钠的偏铝酸钠溶液中滴加盐酸所得沉淀的物质的量与盐酸体积的关系
C. 图3表示常温下,向0.1000molL-1HCl溶液中滴加20.00mL0.1000molL-1氨水的滴定曲线
D. 图4表示乙醇的催化氧化反应中速率随温度的变化图像,升高温度该反应的平衡常数减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2与Cl2的氧化性相近,常温下均为气体,在自来水消毒和果蔬保鲜等方面应用广泛某兴趣小组通过图1装置(夹持装置略)对其制备吸收释放和应用进行了研究
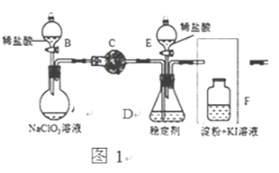
(1)仪器B的名称是:____,请在方框中画出F中缺少的部分____。

(2)打开B的活塞,A中氯酸钠和稀盐酸混和产生Cl2和ClO2,写出反应化学方程式:_______________________; 调节分液漏斗B的旋塞,减缓稀盐酸滴加速度的作用是________
(3)关闭B的活塞,ClO2在D中被稳定剂完全吸收生成1.81g NaClO2,此时F中溶液的颜色不变,则装置C中装的药品的作用是:__________。
(4)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为:_____________________________________________________________________。
(5)在ClO2释放实验中,打开E的活塞,D中发生反应,理论上产生ClO2 在标准状况下的体积为_____________ (保留两位小数); 此时装置F的作用是:______________
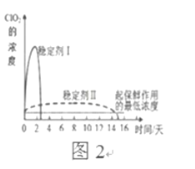
(6)已吸收ClO2气体的稳定剂Ⅰ和Ⅱ,加酸后释放ClO2的浓度随时间的变化如图2所示,若将其用于水果保鲜,你认为效果较好的稳定剂是____,(选填“I”或“II”)
理由是:_________________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关晶体的说法中错误的是
A. 晶体中只要有阴离子就一定有阳离子
B. 原子晶体中共价键越强,熔点越高
C. 晶体中分子间作用力越大,分子越稳定
D. 晶体中不一定存在化学键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)接触法制硫酸工艺中,其主反应是在恒容、温度为450℃并有催化剂存在的条件下进行:
2SO2(g)+O2(g) ![]() 2SO3(g) ΔH=-190Kj/mol
2SO3(g) ΔH=-190Kj/mol
①下列描述中能说明上述反应已达平衡的是____________。
a. ![]() (O2)正=2
(O2)正=2![]() (SO3)逆 b.容器中气体的密度不随时间而变化
(SO3)逆 b.容器中气体的密度不随时间而变化
c.容器中气体的平均相对分子质量不随时间而变化 d.容器中气体的分子总数不随时间而变化
②在一个固定容积为5L的密闭容器中充入0.20molSO2和0.10molO2,半分钟后达到平衡,测得容器中含SO30.18mol,则![]() (O2)=__________mol·L-1·min-1,若继续通入0.40 mol SO2和0.20molO2则平
(O2)=__________mol·L-1·min-1,若继续通入0.40 mol SO2和0.20molO2则平
衡______移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡后,________mol3) <_____mol。
(2)工业生成尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为2NH3 (g)+ CO2(g) ![]() CO(NH2)2(1)+H2O(1),该反应的平衡常数和温度关系如下:
CO(NH2)2(1)+H2O(1),该反应的平衡常数和温度关系如下:
T/℃ | 165 | 175 | 185 | 195 |
K | 111.9 | 74.1 | 50.6 | 34.8 |
①ΔH_______0(填“>”、“<”或“=”)
②在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比)![]() =x,下图是氨碳比(x)与CO2平衡转化率(α)的关系,α随着x增大而增大的原因是___________。
=x,下图是氨碳比(x)与CO2平衡转化率(α)的关系,α随着x增大而增大的原因是___________。

③右图中的B点对应的NH3的平衡转化率为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关离子检验的方法正确的是
A.NH4+:加NaOH溶液,加热,滴入酚酞溶液检验所得溶液
B.CO32-:加入稀盐酸,产生无色能使澄清石灰水变浑浊的气体
C.Fe3+:加入KSCN溶液,溶液呈血红色
D.Cl-:加入AgNO3溶液,产生白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述错误的是( )
A. 丁达尔效应可以用来鉴别胶体和溶液
B. 在水溶液中 NaHSO4 的电离:NaHSO4=Na++ HSO4-
C. 配置 FeSO4溶液时,需加入少量铁粉防止 Fe2+被氧化
D. 碳酸氢钠在医疗上可用于治疗胃酸过多
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com