
| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 二氧化硅性质稳定,不溶于任何酸和碱 | 纯净的二氧化硅是制造光导纤维的基本原料 | Ⅰ对;Ⅱ错;无 |
| B | Cl2和SO2都有较好的漂白作用 | Cl2和SO2混合后漂白效果一定加强 | Ⅰ对;Ⅱ对;有 |
| C | 稀硝酸具有强氧化性 | 铜与稀硝酸能反应且放出红棕色气体 | Ⅰ对;Ⅱ对;无 |
| D | 石墨常用作电解池的电极 | 石墨的化学性质稳定且导电性好 | Ⅰ对;Ⅱ对;有 |


科目:高中化学 来源: 题型:
下表中,对陈述Ⅰ、Ⅱ的正确性及两者间是否具有因果关系的判断都正确的是( )
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 青铜是我国使用最早的合金 | 合金是指多种金属熔合成的金属材料 | Ⅰ错;Ⅱ对;无 |
| B | 精炼铜时,粗铜板作阳极 | 铜具有良好的导电性 | Ⅰ对;Ⅱ对;无 |
| C | 铜锌原电池中,铜是正极 | CuO和Cu2O都是黑色固体 | Ⅰ错;Ⅱ错;无 |
| D | CuO能与水反应生成Cu(OH)2 | 金属氧化物都能与水反应生成相应的金属氢氧化物 | Ⅰ对;Ⅱ对;有 |
查看答案和解析>>
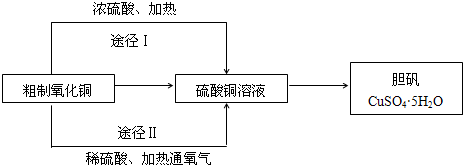
科目:高中化学 来源: 题型:阅读理解
| 矿石名称 | 黄铜矿 | 斑铜矿 | 辉铜矿 | 孔雀石 |
| 主要成分 | CuFeS2 | Cu5FeS4 | Cu2S | CuCO3?Cu(OH)2 |
| ||
| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 铜绿的主成分是碱酸铜 | 可用稀盐酸除铜器表面的铜绿 | Ⅰ对;Ⅱ对;有 |
| B | 铜表易形成致密的氧化膜 | 铜容器可以盛放浓硫酸 | Ⅰ对;Ⅱ对;有 |
| C | 铁比铜活泼 | 例在铜板上的铁钉在潮湿空气中不易生锈 | Ⅰ对;Ⅱ对;有 |
| D | 蓝色硫酸铜晶体受热转化为白色硫酸铜粉末是物理变化 | 硫酸铜溶液可用作游泳池的消毒剂 | Ⅰ错;Ⅱ对;无 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(2011?肇庆一模)下表中,对陈述Ⅰ、Ⅱ的正确性及两者间因果关系的判断,完全正确的是( )
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 铝制饮具最好不要盛放酸性或碱性较强的液体食物 | 因为Al和Al2O3既可以与酸反应、又可以与碱反应 | Ⅰ对,Ⅱ对,有 |
| B | 氯气既能使湿润的有色布条褪色,又能使干燥的有色布条褪色 | 因为氯气和次氯酸均有较强的氧化性 | Ⅰ对,Ⅱ对,有 |
| C | 双氧水、氯气、苯酚、硫酸铜均可用作杀菌消毒剂 | 因为双氧水、氯气、苯酚、硫酸铜都具有较强氧化性 | Ⅰ对,Ⅱ对,有 |
| D | 铁或铝制成的槽车可以密封贮运浓硫酸或浓硝酸 | 因为铁和铝不能与浓硫酸或浓硝酸反应 | Ⅰ错,Ⅱ对,无 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com