
在0.1mol•L﹣1 NH3•H2O溶液中存在如下电离平衡:NH3•H2O⇌NH4++OH﹣.对于该平衡,下列叙述中正确的是( )
|
| A. | 降低温度,溶液中c(NH4+)增大 |
|
| B. | 加入少量NaOH固体,平衡向逆反应方向移动,电离平衡常数减小 |
|
| C. | 加入少量0.1 mol•L﹣1 HCl溶液,溶液中c(OH﹣)增大 |
|
| D. | 加入水时,溶液中 |
考点:
弱电解质在水溶液中的电离平衡.
专题:
电离平衡与溶液的pH专题.
分析:
弱电解质的电离是吸热反应,降低温度抑制弱电解质电离,向氨水中加入酸促进一水合氨电离,加入碱抑制一水合氨电离,加水稀释促进一水合氨电离,注意电离平衡常数只与温度有关.
解答:
解:A.一水合氨的电离是吸热反应,降低温度抑制其电离,则溶液中铵根离子浓度减小,故A错误;
B.向氨水中加入少量氢氧化钠,溶液中氢氧根离子浓度增大,则抑制一水合氨电离,温度不变,电离平衡常数不变,故B错误;
C.向氨水中加入少量浓盐酸,氢离子和氢氧根离子反应生成水,所以氢氧根离子浓度减小,故C错误;
D.加水稀释时,促进一水合氨电离,氢氧根 离子的物质的量增大,一水合氨的物质的量减小,所以溶液中氢氧根离子浓度与一水合氨分子浓度之比增大,故D正确;
故选D.
点评:
本题考查了弱电解质的电离,明确影响弱电解质电离的因素,难度中等,注意加水稀释氨水溶液,溶液中氢离子浓度增大,为易错点.


科目:高中化学 来源: 题型:
25℃,水的电离达到平衡:H2O⇌H++OH﹣,下列叙述正确的是( )
|
| A. | 向水中加入稀醋酸,平衡逆向移动,c(H+)降低 |
|
| B. | 向水中加入少量固体碳酸氢钠,c(H+)增大,Kw不变 |
|
| C. | 向水中加入少量固体CH3COONa,平衡正向移动,c(H+)降低 |
|
| D. | 将水加热,Kw增大,pH不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
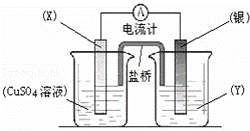
依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.
请回答下列问题:
(1)电极X的材料是 ;电解质溶液Y是 ;
(2)银电极为电池的 极,发生的电极反应为 ;X电极上发生的电极反应为 ;
(3)外电路中的电子是从 电极流向 电极.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实能够说明亚硝酸(HNO2)为弱电解质的是( )
|
| A. | 0.1mol/L的亚硝酸水溶液的PH=2.1 |
|
| B. | 亚硝酸不与硫酸钠溶液反应 |
|
| C. | 25℃时,HNO2的水溶液的PH<7 |
|
| D. | 用亚硝酸做导电实验时,灯泡很暗 |
查看答案和解析>>
科目:高中化学 来源: 题型:
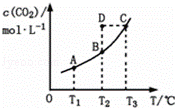
在恒容密闭容器中存在下列平衡:CO(g)+H2O(g)⇌CO2(g)+H2(g).CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示.下列说法错误的是( )
|
| A. | 反应CO(g)+H2O(g)⇌CO2(g)+H2(g)的△H>0 |
|
| B. | 在T2时,若反应处于状态D,则一定有ν正<ν逆 |
|
| C. | 平衡状态A与C相比,平衡状态A的c(CO)小 |
|
| D. | 若T1、T2时的平衡常数分别为K1、K2,则K1<K2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
如图装置,将溶液A逐滴加入固体B中,下列叙述正确的是()
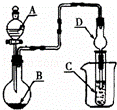
A. 若A为浓盐酸,B为MnO2,C中盛品红溶液,则C中溶液褪色
B. 若A为醋酸,B为贝壳,C中盛过量澄清石灰水,则C中溶液变浑浊
C. 若A为浓氨水,B为生石灰,C中盛AlCl3溶液,则C中先产生白色沉淀后沉淀又溶解
D. 若A为浓硫酸,B为Na2SO3固体,C中盛石蕊试液,则C中溶液先变红后褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
镍电池广泛应用于混合动力汽车系统,电极材料由Ni(OH)2、碳粉、氧化铁等涂覆在铝箔上制成。由于电池使用后电极材料对环境有危害。某兴趣小组对该电池电极材料进行资源回收研究,设计实验流程如下:

已知:①NiCl2易溶于水,Fe3+不能氧化Ni2+。
②K (Ni(OH)
(Ni(OH) ): 5.0×10-16 , K
): 5.0×10-16 , K (NiC2O4): 4.0×10-10
(NiC2O4): 4.0×10-10
回答下列问题:
(1)酸溶后所留残渣的主要成份 (填物质名称)。
(2)用NiO调节溶液的pH,析出沉淀的成分为____________________(填化学式);用pH试纸测定某溶液pH的具体操作是 。
(3)写出加入Na2C2O4溶液后反应的化学方程式_____________________________。
(4)写出加入NaOH溶液所发生反应的离子方程式 ,该反应的平衡常数为 。
(5)沉淀Ⅲ可被电解所得产物 (填化学式)氧化生成Ni(OH)3 ,如何洗涤Ni(OH)3 沉淀 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com