
| n(B)/mol | n(C)/mol | n(D)/mol | 反应时间/min |
| 0.12 | 0.06 | 0.10 | t1 |
| 0.06 | 0.12 | 0.20 | t2 |
A、0~t1时间段内,平均反应速率v(B)=
| ||
B、若起始时n(D)=0,则t2时v(D)=
| ||
| C、升高温度,v(B)、vC)、v(D)均增大 | ||
| D、b:d=6:1 |
| 0.20 |
| t2 |


科目:高中化学 来源: 题型:
 某研究性学习小组将一定浓度Na2CO3溶液滴入CuSO4溶液中得到蓝色沉淀.
某研究性学习小组将一定浓度Na2CO3溶液滴入CuSO4溶液中得到蓝色沉淀.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Y、Z、W能形成含有相同电子数的简单离子,且W形成的简单离子的半径最大 |
| B、XZ2、W2Z2均为直线形的共价化合物 |
| C、Z与M形成的3原子化合物比Y的M形成的4原子化合物稳定 |
| D、由X、Y、Z、M四种元素形成的化合物一定既有离子键,又有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图是硫酸的试剂标签上的部分内容.某次学生实验需要0.5mol?L-1 H2SO4溶液480mL,若由你来配制所需溶液,请根据实验室已有的仪器和药品情况回答下列问题:
如图是硫酸的试剂标签上的部分内容.某次学生实验需要0.5mol?L-1 H2SO4溶液480mL,若由你来配制所需溶液,请根据实验室已有的仪器和药品情况回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
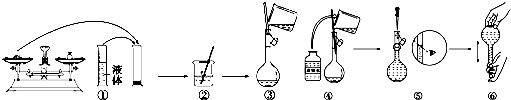
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com