
(1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有湿润的有色布条的广口瓶,可观察到的现象是____________________________________。

(2)为防止氯气尾气污染空气,实验室通常用________溶液吸收多余的氯气,原理是(用化学方程式表示)____________________________。根据这一原理,工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是________(填化学式),长期露置于空气中的漂白粉,加稀盐酸后产生的气体是________(用字母代号填)。
A.O2 B.Cl2
C.CO2 D.HClO
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列化学式与指定物质的主要成分对应正确的是
A.CH4——天然气 B.CO2——水煤气
C.CuSO4▪5H2O——明矾 D.NaHCO3——苏打粉
查看答案和解析>>
科目:高中化学 来源: 题型:
I、恒温下,将a mol N2与b mol H2的混合气体通入一个固体容积的密闭容器中,发生如下反应:N2(g)+3H2(g)  2NH3(g)
2NH3(g)
(1)若反应进行到某时刻t时,nt(N2)=13 mol,nt(NH3)=6 mol,计算 a= 。
(2)反应达到平衡时,混合气体的体积为716.8L(标况下),其中NH3的含量(体积分数)为25%。计算平衡时NH3的物质的量 。。
(3)原混合气体与平衡混合气体的总物质的量之比(写出最简整数比,下同),
n( 始):n(平)= 。
(4)原混合气体中,a:b= 。
(5)达到平衡时,N2和H2的转化率之比,a(N2):a(H2)= 。
(6)平衡混合气体中,n(N2):n(H2):n(NH3)= 。
II、若向体积不变的密闭容器中充入2 mol N2和6 mol H2,一定条件下发生反应:
N2(g)+ 3 H2(g) 2 NH3(g),平衡时混合气共7 mol.令a、b、c分别代表N2、H2、NH3起始加入的物质的量,维持温度不变,使达到平衡时各成分的百分含量不变.则:
2 NH3(g),平衡时混合气共7 mol.令a、b、c分别代表N2、H2、NH3起始加入的物质的量,维持温度不变,使达到平衡时各成分的百分含量不变.则:
(1)若a=0,b=0,则c= .
(2)若a=0.7,b=2.1,则:
① c= .
②这时反应向 进行,因为: .
查看答案和解析>>
科目:高中化学 来源: 题型:
Q、W、X、Y、Z为五种原子序数依次增大的短周期元素。已知:
①Q原子的核外电子数等于电子层数,且与W组成的一种化合物是沼气的主要成分;
②元素X的最高价氧化物的水化物和其气态氢化物能够反应,生成离子化合物甲;
③W与Y组成的化合物乙,是机动车排出的大气污染物之一,也是造成“雾霾”天气的有害物质之一;
④Y与Z能形成电子总数为30和38的两种离子化合物,分别为丙和丁
(1)W在周期表中的位置是_______________;
丁的电子式是 ____ _______。
(2)WY2与Z2Y2反应的化学方程式是__________________。
(3)甲在水溶液中的水解方程式为_______________
(4)写出一种实验室制取XQ3的方法____________(用化学方程式表示)
(5)标准状况下22.4L X的气态氢化物,与0.5L 1mol/L的X最高价氧化物的水化物反应,所得溶液中离子浓度由大到小的顺序是__________(用化学式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
空气中的自由电子附着在分子或原子上形成的空气负离子(也叫阴离子)被称为“空气维生素”。O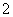 就是一种空气负离子,其摩尔质量为( )
就是一种空气负离子,其摩尔质量为( )
A.32 g B.33 g
C.32 g·mol-1 D.33 g·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
含a个氧原子的硫酸中:
(1)H2SO4分子的个数为________;
(2)H2SO4的物质的量为________;
(3)H2SO4的质量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
家庭厨房实际上就是一个化学世界,柴、米、油、盐、酱、醋、糖等都属于化学物质。请回答:
(1)加碘食盐所含的碘酸钾(KIO3)中,碘元素的化合价是________。
(2)白糖与红糖的主要成分都是蔗糖。利用活性炭的______,可将红糖脱色变成白糖。
(3)食醋不慎滴在大理石台面上,会使其表面变得粗糙而失去光泽。这是因为食醋中的________与大理石发生了化学反应。
(4)东部城市部分家庭厨房中的“柴”将被“西气东输”工程送来的“天然气”所替代,请写出天然气主要成分的化学式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验操作和说法正确的是
A、用pH试纸检验气体的酸碱性时,一定要先用蒸馏水润湿
B、润洗滴定管:从滴定管上口加入所要盛装的酸或碱溶液至“0”刻线,再将液体从滴定管下部放出,重复操作2~3次
C、用瓷坩埚加热熔化碳酸钠固体
D、Mg和Al分别为电极,插入NaOH溶液中,构成原电池,探究Mg、Al的活泼性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com