
 £®
£®·ÖĪö øĆ·“Ó¦ÖŠFeŌŖĖŲ»ÆŗĻ¼ŪÓÉ+2¼Ū±äĪŖ0¼Ū”¢CŌŖĖŲ»ÆŗĻ¼ŪÓÉ+2¼Ū±äĪŖ+4¼Ū£¬ĖłŅŌŃõ»ÆĢśŹĒŃõ»Æ¼Į”¢COŹĒ»¹Ō¼Į£¬Ńõ»Æ¼Į±»»¹Ō”¢»¹Ō¼Į±»Ńõ»Æ£¬ŅŌ“ĖĄ“½ā“š£®
½ā“š ½ā£ŗ£Ø1£©FeŌŖĖŲµÄ»ÆŗĻ¼Ū½µµĶµĆµ½µē×Ó£¬CŌŖĖŲµÄ»ÆŗĻ¼ŪÉżøߏ§Č„µē×Ó£¬øĆ·“Ó¦ÖŠ×ŖŅĘ6e-£¬Ė«ĻßĒŷرź³öøĆ·“Ó¦ÖŠµē×Ó×ŖŅʵķ½ĻņŗĶŹżÄæĪŖ £¬
£¬
¹Ź“š°øĪŖ£ŗ £»
£»
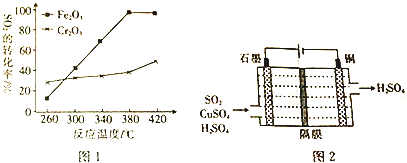
£Ø2£©FeŌŖĖŲµÄ»ÆŗĻ¼Ū½µµĶ£¬ŌņFe2O3ĪŖŃõ»Æ¼Į£¬CŌŖĖŲµÄ»ÆŗĻ¼ŪÉżøߣ¬Ź§Č„µē×Ó±»Ńõ»Æ£¬ŌņŃõ»Æ²śĪļĪŖCO2£¬¹Ź“š°øĪŖ£ŗFe2O3£»CO2£®
µćĘĄ ±¾Ģāæ¼²éŃõ»Æ»¹Ō·“Ó¦£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕ·“Ó¦ÖŠŌŖĖŲµÄ»ÆŗĻ¼Ū±ä»ÆĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲŃõ»Æ»¹Ō·“Ó¦»ł±¾øÅÄī¼°×ŖŅʵē×Ó±ķŹ¾·½·ØµÄ漲飬ĢāÄæÄŃ¶Č²»“ó£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĮņĖįĀĮČÜŅŗÖŠ¼ÓČė¹żĮæ°±Ė®£¬Õńµ“£¬æɹŪ²ģµ½Éś³É°×É«³Įµķ | |
| B£® | ÄĘŌŚæÕĘųÖŠ¼ÓČČ£¬ÄĘæéĻČČŪ³É¹āĮĮµÄŅų°×É«Š”ĒņŗóČ¼ÉÕ£¬·¢³ö»ĘÉ«»šŃę | |
| C£® | ŌŚŹ¢Na2O2¹ĢĢåµÄŹŌ¹ÜÖŠĻČŗóµĪČėĖ®ŗĶ·ÓĢŖČÜŅŗ£¬ČÜŅŗ×īÖÕ³ŹŗģÉ« | |
| D£® | ŠĀÖĘĀČĖ®ÖŠµĪ¼Ó×ĻÉ«ŹÆČļČÜŅŗĻȱäŗģŗóĶŹÉ«£® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ĪļÖŹ | ŌÓÖŹ | ŹŌ¼Į | Ö÷ŅŖ²Ł×÷ | |
| A | SiO2 | Fe2O3 | ŃĪĖį | ¹żĀĖ |
| B | Mg | Al | NaOH | ¹żĀĖ |
| C | FeCl2 | FeCl3 | Cu | ¹żĀĖ |
| D | KNO3 | KCl | H2O | ĄäČ“½į¾§ |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĒāĘųŌŚĀČĘųÖŠ°²¾²Č¼ÉÕ£¬·¢³ö²Ō°×É«»šŃę | |
| B£® | ĢśĖæŌŚĀČĘųÖŠČ¼ÉÕ£¬²śÉś×ŲŗÖÉ«µÄŃĢ | |
| C£® | ĶĖæŌŚĀČĘųÖŠČ¼ÉÕ£¬²śÉś×Ų»ĘÉ«µÄŃĢ | |
| D£® | ÄĘŌŚĀČĘųÖŠČ¼ÉÕ£¬²śÉś»ĘÉ«µÄŃĢ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĀČĘųČÜÓŚĖ®£ŗCl2+H2OØT2H++Cl-+ClO- | |
| B£® | Ļ” H2SO4ÓėĢś·Ū·“Ó¦£ŗ2Fe+6H+ØT2Fe3++3H2”ü | |
| C£® | ÄĘ·ÅČėĖ®ÖŠ£ŗNa+H2OØTNa++OH-+H2”ü | |
| D£® | ĒāŃõ»ÆĆ¾ČÜÓŚŃĪĖį£ŗMg£ØOH£©2+2H+ØTMg2++2H2O£® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
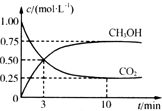 ¶žŃõ»ÆĢ¼ŹĒµŲĒņĪĀŹŅŠ§Ó¦µÄ×ļæż»öŹ×£¬ÄæĒ°ČĖĆĒ“¦Ąķ¶žŃõ»ÆĢ¼µÄ·½·ØÖ®Ņ»ŹĒŹ¹ĘäÓėĒāĘų·“Ó¦ŗĻ³É¼×“¼£®ŅŃÖŖĒāĘų”¢¼×“¼Č¼ÉÕµÄČČ»Æѧ·½³ĢŹ½ČēĻĀ£ŗ
¶žŃõ»ÆĢ¼ŹĒµŲĒņĪĀŹŅŠ§Ó¦µÄ×ļæż»öŹ×£¬ÄæĒ°ČĖĆĒ“¦Ąķ¶žŃõ»ÆĢ¼µÄ·½·ØÖ®Ņ»ŹĒŹ¹ĘäÓėĒāĘų·“Ó¦ŗĻ³É¼×“¼£®ŅŃÖŖĒāĘų”¢¼×“¼Č¼ÉÕµÄČČ»Æѧ·½³ĢŹ½ČēĻĀ£ŗ| ĪļÖŹ | CH3OH | CH3OCH3 | H2O |
| ÅضČ/£Ømol/L£© | 0.44 | 0.6 | 0.6 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  | B£® | 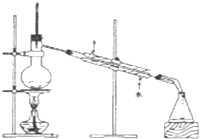 | ||
| C£® | 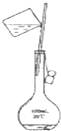 | D£® | 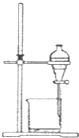 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¼×±½ĪŽĶ¬·ÖŅģ¹¹Ģå | B£® | ¼ä¶ž¼×±½Ć»ÓŠĶ¬·ÖŅģ¹¹Ģå | ||
| C£® | ĮŚ¶ž¼×±½Ć»ÓŠĶ¬·ÖŅģ¹¹Ģå | D£® | 1 mol±½Ö»ÄÜÓė3 molH2¼Ó³É |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com