
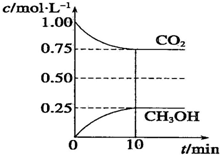
 在一定温度下的2L固定容积的密闭容器中,通入2mol CO2和3mol H2,发生的反应为CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-akJ.mol-1(a>0),测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示.
在一定温度下的2L固定容积的密闭容器中,通入2mol CO2和3mol H2,发生的反应为CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-akJ.mol-1(a>0),测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示.分析 (1)①平衡状态的标志可以两个方两去判断,一、是看正逆反应速是否相等,二是各组分的浓度和分数是否随时间的改变而改变;也可以抓住未平衡时是个变量,现在不变说明已经达到平衡状态了,来解决问题;
(2)计算二氧化碳的反应速率,结合速率之比等于化学方程式计量数之比计算氢气的反应速率v=$\frac{△c}{△t}$计算得到;
(3)根据外界条件的改变来判断平衡移动方向,然后去分析分子和分母的变化情况;
(4)用三行式来求平衡时的各组分浓度,然后代入平衡常数表达式求解,要注意代入平衡常数表达式是平衡浓度,平衡常数是温度的函数,温度变平衡常数才变,到底如何变,还要看反应的热效应;
解答 解:(1)①未平衡时是个变量,现在不变说明已经达到平衡状态了,
A.未平衡CO2的体积分数是个变化的量,现在混合气体CO2的体积分数保持不变,说明已经平衡了,故A正确;
B.未平衡时混合气体的平均相对分子质量是个变化的量,现在不随时间的变化而变化,说明已经达平衡状态,故B正确;
C.单位时间内每消耗1.2mol H2,向正方向,同时生成0.4mol H2O,也向正方向,不能反映正逆反应之间的关系,故C错误;
D.反应中H2O与CH3OH的物质的量浓度之比为1:1,且保持不变,不能说明各自的量不再随时间的变化而变化,故C错误;
故选AB;
(2)从0min到10min,v(CO2)=$\frac{1.0mol/L-0.75mol/L}{10min}$=0.025mol/L•s,v(H2)=3v(CO2)=0.025mol/L•s×3=0.075mol/L•s,
故答案为:0.075 mol•L-1•min-1;
(3)A.升高温度,平衡逆向移动,故比值减小,故A不选;
B.恒温恒容下充入He(g),平衡不移动,故比值不变,故B不选;
C.将H2O(g)从体系中分离,平衡正向移动,故比值变大,故选C;
D.恒温恒容再充入2mol CO2和3mol H2,相当于增大压强,平衡正向移动,故比值变大,故选D;
故答案为CD;
(4)CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
初始(mol/L) 1 1.5 0 0
变化(mol/L) 0.25 0.75 0.25 0.25
平衡(mol/L) 0.75 0.75 0.25 0.25
所以 K=$\frac{0.25×0.25}{0.75×0.7{5}^{3}}$=0.20,
而平衡常数是温度的函数,只有通过改变温度来改变平衡常数,正反应量放热反应,降低温度,K值变大,
故答案为:0.20;D.
点评 本题考查了化学平衡的有关知识,学生要学会三行式在解题中的应用,综合性强,但难度不大.


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:选择题
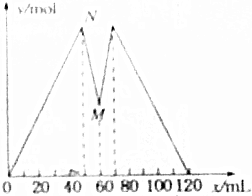 如图所示是向MgCl2和AlCl3的混合溶液中加入NaOH溶液和盐酸时,沉淀的物质的量y(mol)与加入NaOH溶和盐酸的体积x(mL)的关系图.根据图示判断,下列结论中不正确的是( )
如图所示是向MgCl2和AlCl3的混合溶液中加入NaOH溶液和盐酸时,沉淀的物质的量y(mol)与加入NaOH溶和盐酸的体积x(mL)的关系图.根据图示判断,下列结论中不正确的是( )| A. | N点时溶液中的溶质只有NaCl | |
| B. | 原混合溶液中c(MgCl2):c(AlCl3)=1:2 | |
| C. | c(NaOH)=c(HCl) | |
| D. | M点之前加入的是NaOH溶液,M点之后加入的是盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 粗盐过滤时,用玻璃棒搅拌加快过滤的速度 | |
| B. | 蒸发滤液时,待蒸发皿中滤液蒸干时停止加热 | |
| C. | 配制溶液时必须使用的仪器有托盘天平、酒精灯、量筒、烧杯、玻璃棒等 | |
| D. | 配制溶液需要经过计算、称量、溶解、装瓶贴标签等步骤 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 容器内气体密度减小 | B. | 平衡向正反应方向移动 | ||
| C. | 二氧化氮的转化率增大 | D. | 四氧化二氮的体积分数减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
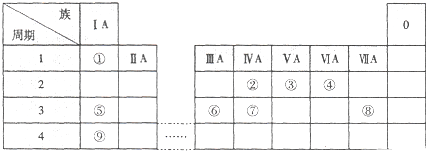
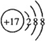 .
.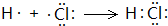 .
.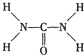 ,尿素分子中σ键和π键数目之比为7:1.
,尿素分子中σ键和π键数目之比为7:1.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 需要加热的化学反应都是吸热反应 | |
| B. | 放热反应都不需要加热就可以发生 | |
| C. | 化学反应除了生成新物质外,还伴随着能量的变化 | |
| D. | 化学反应放热还是吸热,取决于反应条件 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 荧光素属于高分子化合物 | |
| B. | 荧光素与氧化荧光素都至少有6个碳原子共平面 | |
| C. | 荧光素与氧化荧光素都能与碳酸氢钠反应 | |
| D. | 荧光素与氧化荧光素互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 葡萄糖、蔗糖、淀粉都可以食用,都能发生水解 | |
| B. | 苯与液溴在铁作催化剂的条件下的反应为加成反应 | |
| C. | 甲烷、苯、淀粉、蛋白质完全燃烧的产物都只有二氧化碳和水 | |
| D. | 油脂属于酯,在酸性条件下的水解产物都是醇和羧酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
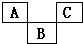 如图为元素周期表的一部分,A、B、C均为短周期元素.B的最高价氧化物的水化物为H3BO4,则A、B、C依次是( )
如图为元素周期表的一部分,A、B、C均为短周期元素.B的最高价氧化物的水化物为H3BO4,则A、B、C依次是( )| A. | C、A1、P | B. | N、Si、S | C. | C、P、O | D. | F、S、Ar |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com