
(1)在化学反应中,随着物质的变化,化学能也发生改变,还可能伴随着不同形式的能量转化。已知:破坏1 mol氢气中的化学键需要吸收436 kJ能量;破坏1/2 mol氧气中的化学键需要吸收 249 kJ的能量;形成水分子中1 mol H—O键能够释放 463 kJ能量。下图表示氢气和氧气反应过程中能量的变化,请将图中①、②、③的能量变化的数值,填在相应的横线上。
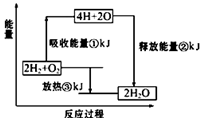
①________kJ ②________kJ ③________kJ
(2)今有2H2+O2 =2H2O反应构成燃料电池,则负极通的应是 ,用KOH溶液作电解质,负极的电极反应式为 ,正极的电极反应式为 。
(3)若把H2改为CH3OH,用KOH溶液作电解质,则负极的电极反应式: .
(4)电解原理在化学工业中有广泛的应用。右图表示一个电解池,电极材料为惰性电极,U形管装有饱和食盐水;实验开始时,同时在两边各滴入几滴酚酞试液,则:
①电解池中阴极上的电极反应式为______________________,在阴极附近观察到的现象是_______________。

②随着气体的生成,饱和食盐水中产生了两种不同的颜色:
阳极区是 色,阴极区是 色。
③电解一段时间后取出电极,将U形管内的液体搅拌混匀,又发生了化学反应,该反应的化学方程式是 ;该溶液可用作消毒剂,原因是__________________
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
下列反应前后物质的总能量变化可用右图表示的是( )
A.生石灰加水生成熟石灰 B.C+H2O=CO+H2
C.金属钠与水反应 D.HNO3+NaOH=NaNO3+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
已知芳香族化合物B的分子式为C9H11Cl,2—甲基苯乙酸(E)是常用的一种有机合成中间体。存在下列转化关系:

(1)B的结构简式为 ▲ 。
(2)转化关系中B→A、B→C的反应类型依次为 ▲ 、 ▲ 。
(3)A的同分异构体F,苯环上有且仅有一个取代基,且能与溴水发生加成反应,任写一种符合条件F的结构简式 ▲ 。
(4)据文献报道,该中间体E的另一合成工艺为 高 考 资 源 网

从反应原理分析,该工艺存在的明显不足为 ▲ ;反应③的化学方程式为 ▲ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示。下列叙述正确的是( )
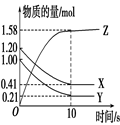
A.反应开始到10 s末时,用Z表示的反应速率为0.158 mol·L-1·s-1
B.反应开始到10 s末时,X的物质的量浓度减少了0.79 mol·L-1
C.反应开始到10 s时,Y的转化率为79.0%
D.反应的化学方程式为X(g)+Y(g)Z(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH。下列叙述不正确的是( )
3Zn(OH)2+2Fe(OH)3+4KOH。下列叙述不正确的是( )
A.放电时锌作负极 B.充电时氢氧化铁被氧化
C.放电时溶液的碱性增强 D.放电时转移3 mol e-,有2 mol FeO 被还原
被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
判断正误,正确的划“√”,错误的划“×”
(1)强氧化剂与强还原剂混合不一定能发生氧化还原反应 ( )
解析 强氧化剂与强还原剂发生反应需要一定的条件,如H2和O2发生反应需要点燃或 光照。
光照。
(2)阳离子只有氧化性,阴离子只有还原性 ( )
(3)元素的非金属性越强,其氧化性越强,相应单质越活泼 ( )
查看答案和解析>>
科目:高中化学 来源: 题型:
亚氨基锂(Li2NH)是一种储氢容量高、安全性好的固体储氢材料,其储氢原理可表示为Li2NH+H2LiNH2+LiH,下列有关说法正确的是 ( )
A.Li2NH中N的化合价是-1
B.该反应中H2既是氧化剂又是还原剂
C.Li+和H-的离子半径相等
D.此法储氢和钢瓶储氢的原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作错误的是( )。
A.用钥匙取用少量的Na2SO4固体
B.用胶头滴管滴加少量的NaCl溶液
C.加热盛有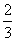 体积K2SO4溶液的试管
体积K2SO4溶液的试管
D.用10mL的量筒量取8mL1.0mol/LNaOH溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com