
【题目】研究和深度开发CO、CO2的应用具有重要的社会意义。回答下列问题:
(1)CO可用于高炉炼铁,已知:
Fe3O4(s)+4CO(g)=3Fe(s)+4CO2 (g) △H1= a kJ/mol
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2 (g) △ H2= b kJ/mol
则反应Fe2O3(s)+3CO(g)=2Fe(s)+3CO2 (g)的△H=________kJ/mol
(2)某温度下,在容积为2 L的密闭容器甲中投入8molCO2(g)、16molH2(g)发生反应:
CO2 (g)+H2(g) ![]() CO(g)+H2O(g)
CO(g)+H2O(g)
甲容器15 min后达到平衡,此时CO2的转化率为75%。则015 min内用二氧化碳表示平均反应速率v(CO2)=_______,计算此条件下该反应的平衡常数K= __________。
(3)捕碳技术是指从空气中捕获二氧化碳的各种科学技术的统称。目前NH3和(NH4)2CO3等物质已经被用作工业捕碳剂。
①下列物质中不可能作为CO2捕获剂的是___________。
A.Na2CO3 B.NaOH C.CH3CH2OH D.NH4Cl
②用(NH4)2CO3捕碳的反应:(NH4)2CO3(aq)+H2O(l)+CO2(g) ![]() 2NH4HCO3(aq)。为研究温度对(NH4)2CO3捕获CO2效率的影响,将一定量的(NH4)2CO3溶液置于密闭容器中,并充入一定量的CO2气体,保持其它初始实验条件不变,分别在不同温度下,经过相同时间测得CO2气体浓度,得到趋势图:
2NH4HCO3(aq)。为研究温度对(NH4)2CO3捕获CO2效率的影响,将一定量的(NH4)2CO3溶液置于密闭容器中,并充入一定量的CO2气体,保持其它初始实验条件不变,分别在不同温度下,经过相同时间测得CO2气体浓度,得到趋势图:
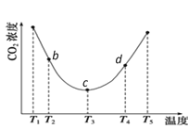
I. c点的逆反应速率和d点的正反应速率的大小关系为
V逆c _____V正d (填“>”、“=”或“<”)
II. b、c、d三点的平衡常数K b 、K c、 Kd 从大到小的顺序为_______。(填“>”、“=”或“<”)
III.T3~T4温度区间,容器内CO2气体浓度呈现增大的变化趋势,其原因是____________。
【答案】(2a+b)/3 0.2 mol/(L·min) 1.8 CD < K b>K c >Kd T3-T4 区间,化学反应已达到平衡,由于正反应是放热反应,温度升高平衡向逆反应方向移动,所以不利于 CO2 的捕获
【解析】
(1)根据盖斯定律分析解答;
(2)甲容器15min后达到平衡,此时CO2的转化率为75%,则转化CO2为8mol×75%=6mol,根据三段式分析计算;
(3)①具有碱性的物质能反应二氧化碳反应,能够捕获CO2;②c点是平衡点,正逆反应速率相同,根据温度对化学反应速率和平衡的影响分析解答。
(1)①Fe3O4(s)+4CO(g)═3Fe(s)+4CO2(g)△H1=akJ/mol,②3Fe2O3(s)+CO(g)═2Fe3O4(s)+CO2(g)△H2=bkJ/mol,根据盖斯定律:![]() 可得Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g),故△H3=
可得Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g),故△H3=![]() =
=![]() kJ/mol,故答案为:
kJ/mol,故答案为:![]() ;
;
(2)甲容器15min后达到平衡,此时CO2的转化率为75%,则转化CO2为8mol×75%=6mol,列三段式:
CO2(g)+H2(g)CO(g)+H2O(g)
起始(mol/L):4 8 0 0
转化(mol/L):3 3 3 3
平衡(mol/L):1 5 3 3
则0~15min内平均反应速率v(CO2)=![]() =0.2mol/(Lmin);此条件下该反应的平衡常数K=
=0.2mol/(Lmin);此条件下该反应的平衡常数K=![]() =1.8,故答案为:0.2mol/(Lmin);1.8;
=1.8,故答案为:0.2mol/(Lmin);1.8;
(3)①A.Na2CO3 和二氧化碳反应生成碳酸氢钠,故A不符合;B.NaOH显碱性,可以吸收二氧化碳,故B不符合;C.CH3CH2OH 为中性分子不能和二氧化碳反应,不能吸收二氧化碳,故C符合;D.NH4Cl溶液显酸性,不能吸收二氧化碳,故D符合,故答案为:CD;
②I.温度越高,反应速率越快,d点温度高,则c点的逆反应速率和d点的正反应速率的大小关系为V逆c<V正d,故答案为:<;
II.根据图像,温度为T3时反应达平衡,此后温度升高,c(CO2)增大,平衡逆向移动,说明反应是放热反应,升高温度,平衡逆向进行,平衡常数减小,Kb>Kc>Kd,故答案为:Kb>Kc>Kd;
III.T3-T4区间,化学反应已达到平衡,由于正反应是放热反应,温度升高,平衡向逆反应方向移动,不利于CO2的捕获,所以容器内CO2气体浓度呈现增大的变化趋势,故答案为: T3-T4区间,化学反应已达到平衡,由于正反应是放热反应,温度升高,平衡向逆反应方向移动,不利于CO2的捕获。


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.Na与H2O的反应是熵增的放热反应,该反应能自发进行
B.饱和Na2SO4溶液或浓硝酸均可使蛋白质溶液产生沉淀,但原理不同
C.FeCl3和MnO2均可加快H2O2分解,同等条件下二者对H2O2分解速率的改变相同
D.Mg(OH)2固体在溶液中存在平衡:Mg(OH)2(s)![]() Mg2+(aq)+2OH—(aq),该固体可溶于NH4Cl溶液
Mg2+(aq)+2OH—(aq),该固体可溶于NH4Cl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的氧化物和氮的氢化物的任意排放均会对环境造成污染,因此关于其转化的研究对于消除环境污染有着重要意义。
(1)已知T℃时,有如下反应:
反应I:4NH3(g) + 6NO(g)![]() 5N2 ( g) + 6H2O(g) △H = -1804 kJmol-1
5N2 ( g) + 6H2O(g) △H = -1804 kJmol-1
反应II:N2(g) +2O2(g) ![]() 2NO2(g) △H = +67.8 kJmol-1
2NO2(g) △H = +67.8 kJmol-1
反应III:2NO(g) + O2 (g) ![]() 2 NO2 (g) △H =-116.2 kJmol-1
2 NO2 (g) △H =-116.2 kJmol-1
试写出T℃ 时,NH3与NO2反应生成不污染环境的物质的热化学反应方程式 ______。
(2)T℃时,向2L密闭容器中加入一定量的NO2、NO和O2,发生(1)中反应III,不同时间测得各物质的部分浓度(molL-1) 如下表所示:
时间( min) | NO | O2 | NO2 |
0 | a | 0.30 | 0.10 |
10 | 0.14 | 0.27 | b |
20 | 0.10 | c | 0.20 |
30 | d | 0.24 | 0.22 |
40 | 0.08 | e | f |
①温度不变,反应达平衡后容器中的压强与最初加入气体时的压强之比为_______。
②反应的前 20 min 的平均反应速率v(NO)=________molL-1·min-1。
③若温度不变,平衡后将反应容器压缩为1L,达到新的平衡后,c(O2)_____0.48molL-1(填“>”“<”或“ =”)。
(3)某化学兴趣小组利用电解原理设计实验消除NH3 与 NO对环境的影响, 并制取KOH溶液和H2SO4溶液,其工作原理如下图所示:
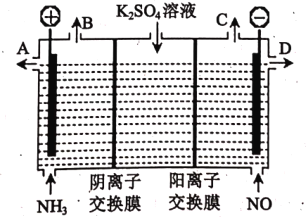
①从出口B、C产生的气体相同,该气体是_____:从出口 D 得到的溶液是____。
②电解槽左池中发生的电极反应式为________ 。
③电解一段时间,两电极共收集到22.4L气体(标准状况下)时,理论上将生成____________mol KOH。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数,下述正确的是( )
A.64gSO2含有硫原子数为2NA
B.NA个氧气分子和NA个氢气分子的质量比等于16∶1
C.28g氮气所含的原子数目为NA
D.标准状况下,22.4L的水含有 NA个水分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼氢化物NaBH4(B元素的化合价为+3价)燃料电池(DBFC), 由于具有效率高、产物清洁无污染和燃料易于储存和运输等优点,被认为是一种很有发展潜力的燃料电池。其工作原理如下图所示,下列说法正确的是
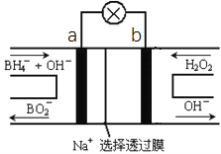
A. 电池的负极反应为BH4-+2H2O-8e-=BO2-+8H+
B. 放电时,每转移2mol电子,理论上需要消耗9.5gNaBH4
C. 电池放电时Na+从b极区移向a极区
D. 电极a采用MnO2,MnO2既作电极材料又有催化作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下 ,下列各组离子在指定溶液中能大量共存的是
A.0.1 mol L-1的盐酸:Na+、Cu2+、SO![]() 、NO
、NO![]()
B.0. 1 mol L-1的氨水:K+、Al3+、Cl、CH3COO-
C.0. 1 mol L-1的Fe(NO3)3溶液: H+、K+、Cl-、I-
D.0.1 mol L -1的Na2SO3溶液:NH![]() 、Na+、ClO-、SO
、Na+、ClO-、SO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W 为短周期主族元素,其常见化合价与原子半径的关系如图所示。已知四种元素中只有 Y 与 Z 同周期,下列说法正确的是( )
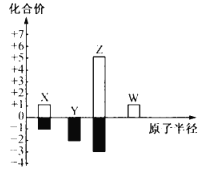
A.简单氢化物的稳定性:Y<Z
B.X、Y、Z 可组成盐类化合物
C.X 的氧化物中不可能含非极性键
D.W 的最高价氧化物对应水化物为弱碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】粘合剂M的合成路线如下图所示:
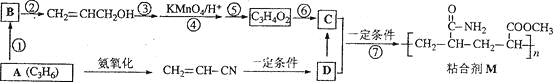
完成下列填空:
1)写出A和B的结构简式。
A___________B_______________
2)写出反应类型。反应⑥______________反应⑦______________
3)写出反应条件。反应②______________反应⑤______________
4)反应③和⑤的目的是____________________。
5)C的具有相同官能团的同分异构体共有________________种。
6)写出D在碱性条件下水解的反应方程式。
____________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SF6可用作高压电力设备中的“气体绝缘开关”,由S(g)与F2(g)制备SF6(g)的能量变化如图所示,下列说法正确的是
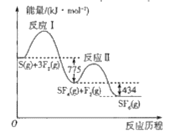
A.若已知S-F键的键能则可确定F-F键的键能
B.S(g)+3F2(g)=SF6(g)△H=+1209kJ·mol-1
C.与S(g)+3F2(g)=SF6(g)相比,S(s)+3F2(g)=SF6(g)放出的热量较多
D.由于反应Ⅰ放出的热量大于反应Ⅱ,所以反应速率:Ⅰ>Ⅱ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com