
| A£® | 25”ꏱ£¬pH=13µÄ1.0LBa£ØOH£©2ČÜŅŗÖŠŗ¬ÓŠµÄOH-ŹżÄæĪŖ0.2NA | |
| B£® | -¶ØĢõ¼žĻĀŌŚĆܱÕČŻĘ÷ÖŠ2molSO2Óė2molO2³ä·Ö·“Ó¦£¬×īÖÕµÄĘųĢå·Ö×ÓŹżĪŖ3NA | |
| C£® | ½«1molNH4NO3ČÜÓŚĻ”°±Ė®ÖŠŹ¹ČÜŅŗ³ŹÖŠŠŌ£¬ČÜŅŗÖŠNH4+ŹżÄæĪŖNA | |
| D£® | 4.6gŅŅ“¼ŗ¬ÓŠ¹²¼Ū¼üµÄŹżÄæĪŖ0.9NA |
·ÖĪö A£®PH¼ĘĖćČÜŅŗÖŠĒāŃõøłĄė×ÓÅØ¶Č£¬½įŗĻĢå»żŗĶĒāŃõøłĄė×ÓÅØ¶Č¼ĘĖćČÜÖŹĪļÖŹµÄĮæ·ÖĪö£»
B£®·“Ó¦ĪŖæÉÄę·“Ó¦²»ÄܽųŠŠ³¹µ×£»
C£®ČÜŅŗÖŠ“ęŌŚµēŗÉŹŲŗć·ÖĪö£»
D£®Ņ»øöŅŅ“¼·Ö×ÓÖŠŗ¬ÓŠ¹²¼Ū¼üŹżÄæŹĒ8øö¹²¼Ū¼ü£»
½ā“š ½ā£ŗA”¢pH=13µÄ1.0LBa£ØOH£©2ČÜŅŗÖŠ£¬ĒāŃõøłĄė×ÓÅضČ=$\frac{1{0}^{-14}}{1{0}^{-13}}$=0.1mol/L£¬ĖłŅŌŗ¬ÓŠµÄOH-ŹżÄæ=0.1mol/L”Į1L”ĮNA=0.1NA£¬¹ŹA“ķĪó£»
B£®ŌŚĆܱÕČŻĘ÷ÖŠ2molSO2Óė2molO2³ä·Ö·“Ó¦“ļµ½»ÆŃ§Ę½ŗā£¬×īÖÕµÄĘųĢå·Ö×ÓŹż“óÓŚ3NA£¬¹ŹB“ķĪó£»
C£®½«1molNH4NO3ČÜÓŚĻ”°±Ė®ÖŠŹ¹ČÜŅŗ³ŹÖŠŠŌ£¬c£ØH+£©=c£ØOH-£©£¬ČÜŅŗÖŠ“ęŌŚµēŗÉŹŲŗć£¬c£ØNH4+£©+c£ØH+£©=c£ØOH-£©+c£ØNO3-£©£¬ŌņČÜŅŗÖŠn£ØNH4+£©=n£ØNO3-£©=1mol£¬NH4+ŹżÄæĪŖNA£¬¹ŹCÕżČ·£»
D.4.6gµÄŅŅ“¼µÄĪļÖŹµÄĮæĪŖ$\frac{4£¬6g}{46g/mol}$=0.1mol£¬ŗ¬ÓŠ¹²¼Ū¼ü0.8mol£¬ŹżÄæĪŖ0.8NA£¬¹ŹD“ķĪó£»
¹ŹŃ”C£®
µćĘĄ ±¾Ģā漲鰢·ü¼ÓµĀĀŽ³£ŹżµÄÓŠ¹Ų¼ĘĖćŗĶÅŠ¶Ļ£¬ŹģĮ·ÕĘĪÕ¹«Ź½µÄŹ¹ÓĆŗĶĪļÖŹµÄ½į¹¹ŹĒ½āĢāµÄ¹Ų¼ü£¬×¢ŅāæÉÄę·“Ó¦·ÖĪö£¬ĢāÄæÄŃ¶Č²»“ó£®


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
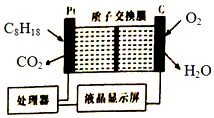
| A£® | ŹÆÄ«µē¼«×÷Õż¼«£¬·¢Éś»¹Ō·“Ó¦ | |
| B£® | ²¬µē¼«µÄµē¼«·“Ó¦Ź½£ŗC8H18+16H2O-50e-ØT8CO2”ü+50H+ | |
| C£® | H+ÓÉÖŹ×Ó½»»»Ä¤×ó²ąĻņÓŅ²ąĒØŅĘ | |
| D£® | ĆæĻūŗÄ5.6LO2£¬µēĀ·ÖŠĶعż1 molµē×Ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ²»Ö»ŹĒĖį”¢¼ī”¢ŃĪĄąĪļÖŹ²ÅŹōÓŚµē½āÖŹ | |
| B£® | ĀČ»ÆÄĘČÜŅŗŌŚµēĮ÷×÷ÓĆĻĀµēĄėĪŖÄĘĄė×ÓÓėĀČĄė×Ó | |
| C£® | µē½āÖŹĪ“±ŲÄܵ¼µē£¬Äܵ¼µēµÄŅ²Ī“±ŲŹĒµē½āÖŹ | |
| D£® | ĮņĖį±µµÄĖ®ČÜŅŗĖäµ¼µēŠŌ¼«Čõ£¬µ«ĮņĖį±µŹĒĒæµē½āÖŹ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
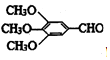 £©ŗĶæ¹ń²šļŅ©ĪļH£Ø
£©ŗĶæ¹ń²šļŅ©ĪļH£Ø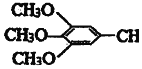 =CHCONHCH£ØCH3£©2£©µÄĀ·ĻßČēĶ¼£Ø²æ·Ö·“Ó¦ĀŌČ„Ģõ¼žŗĶŹŌ¼Į£©£ŗ
=CHCONHCH£ØCH3£©2£©µÄĀ·ĻßČēĶ¼£Ø²æ·Ö·“Ó¦ĀŌČ„Ģõ¼žŗĶŹŌ¼Į£©£ŗ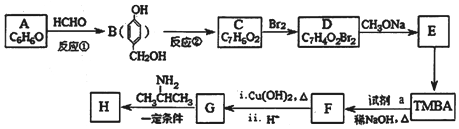
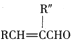 £ØR”¢R”å±ķŹ¾Ģž»ł»ņĒā£©
£ØR”¢R”å±ķŹ¾Ģž»ł»ņĒā£©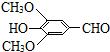 £¬ŹŌ¼ĮaµÄ·Ö×ÓŹ½ŹĒC2H4O£®
£¬ŹŌ¼ĮaµÄ·Ö×ÓŹ½ŹĒC2H4O£®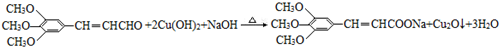 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | K+”¢Cu2+”¢SO42-”¢Cl- | B£® | Na+”¢H+”¢Cl-”¢CO32- | ||
| C£® | H+”¢Ba2+”¢Cl-”¢NO3- | D£® | K+”¢Fe2+”¢OH-”¢NO3- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | K +”¢£®MnO 4 -”¢Cl -”¢SO 4 2- | B£® | Na +”¢CO 3 2-”¢Cl -”¢SO 4 2- | ||
| C£® | NO 3 -”¢Na +”¢HCO 3 -”¢Ba 2+ | D£® | Na +”¢NO 3 -”¢NH 4 +”¢SO 4 2- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĻņĻ”HNO3ÖŠ¼ÓČėĶ·Ū²śÉśĘųĢå£ŗCu+4H++2NO3-ØTCu2++2NO2”ü+H2O | |
| B£® | ĻņH2SO4ČÜŅŗÖŠ¼ÓČėBa£ØOH£©2²śÉś³Įµķ£ŗSO42-+Ba2+ØTBaSO4”ż | |
| C£® | ĻņCa£ØClO£©2ČÜŅŗÖŠĶØČė¹żĮæCO2ÖĘČ”HClO£ŗ2ClO-+H2O+CO2ØTHClO+CO32- | |
| D£® | ĻņĖ®ÖŠ¼ÓČė½šŹōÄĘ²śÉśĘųĢå£ŗ2Na+2H2OØT2Na++2OH-+H2”ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
 Na2S2O3ŹĒÖŲŅŖµÄ»Æ¹¤ŌĮĻ£¬Ņ×ČÜÓŚĖ®£¬ŌŚÖŠŠŌ»ņ¼īŠŌ»·¾³ÖŠĪČ¶Ø£®
Na2S2O3ŹĒÖŲŅŖµÄ»Æ¹¤ŌĮĻ£¬Ņ×ČÜÓŚĖ®£¬ŌŚÖŠŠŌ»ņ¼īŠŌ»·¾³ÖŠĪČ¶Ø£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 95”ę“æĖ®µÄ pH£¼7£¬ĖµĆ÷¼ÓČČæɵ¼ÖĀĖ®³ŹĖįŠŌ | |
| B£® | pH=3µÄ“×ĖįČÜŅŗ£¬Ļ”ŹĶÖĮ 10 ±¶ŗó pH=4 | |
| C£® | pH=3µÄ“×ĖįČÜŅŗ£¬ÓėpH=11µÄĒāŃõ»ÆÄĘČÜŅŗµČĢå»ż»ģŗĻŗópH£¾7 | |
| D£® | pH ¾łĪŖ3µÄ“×ĖįŗĶŃĪĖį·Ö±šÓė×ćĮæZn·“Ó¦£¬“×Ėį²śÉśµÄH2¶ą |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com