
a、b、c、d是四种短周期元素。a、b、d同周期,c、d同主族。a的原子结构示意图为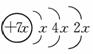 ,b与c形成化合物的电子式为
,b与c形成化合物的电子式为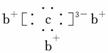 ,下列比较中正确的是( )
,下列比较中正确的是( )
A.原子半径:a>c>d>b B.最高价氧化物对应水化物的酸性:c>d>a
C.原子序数:a>d>b>c D.单质的氧化性:a>b>d>c
科目:高中化学 来源: 题型:
为增强铝的耐腐蚀性,现以铅蓄电池为外电源,以A1作阳极、pb作阴极,电解稀硫酸,使铝表面的氧化膜增厚。反应原理如下:
电池:Pb(s) + PbO2(s) + 2H2SO4(aq) = 2PbSO4(s) + 2H2O(l)
电解池:2Al+3H2O  Al2O3+3H2↑
Al2O3+3H2↑
电解过程中,以下判断正确的是
| 电池 | 电解池 | |
| A | H+移向Pb电极 | H+移向Pb电极 |
| B | 每消耗3 mol Pb | 生成2 mol Al2O3 |
| C | 正极:PbO2 + 4H+ + 2e- = Pb2+ + 2H2O | 阳极:2Al + 3H2O-6e- = Al2O3 + 6H+ |
| D |
|
|
查看答案和解析>>
科目:高中化学 来源: 题型:
有A、B、C、D四种短周期元素,它们的原子序数由A到D依次增大, 已知A和B原子有相同的电子层数, 且A的L层电子数是K层电子数的两倍, C燃烧时呈现黄色火焰, C的单质在高温下与B的单质充分反应, 可以得到与D单质颜色相同的淡黄色固态化合物, 试根据以上叙述回答:
(1 )元素名称: A B _________ C __________ D ___________
(2) 写出AB2与过量氢氧化钠反应的离子方程式 ______________
(3) 画出D的原子结构示意图 ____________ _______, 用电子式表示化合物 C2D 的
形成过程_______________________________ _ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关原子结构和元素周期律表述正确的是
①原子序数为15的元素的最高化合价为+3
②ⅦA族元素是同周期中非金属性最强的元素
③第二周期ⅣA族元素的原子核电荷数和中子数一定为6
④原子序数为12的元素位于元素周期表的第三周期ⅡA族
A.①② B.①③ C.②④ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
某氧化物的相对分子质量为a,其相同价态的硫酸盐的相对分子质量为b,则该元素的化合价的数值为:
A .(b-a)/20 B.(b-a)/40 C.(a -b)/80 D.(a-b)/20
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是一个化学过程的示意图。
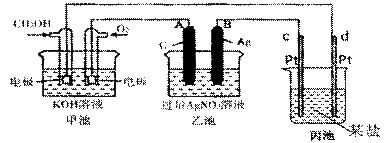
(1)图中乙池是 装置。
(2)c(Pt)电极的名称是 。
(3)写出通入CH3OH的电极的电极反应式是 。
(4)乙池中反应的离子方程式为 。
(5)当乙池中B(Ag)极的质量增加5.40g时,甲池中理论上消耗O2 mL(标准状况下);此时丙池某电极析出0.64g某金属,则丙中的某盐溶液可能是 (填序号)
A. MgSO4 B.CuSO4 C.NaCL D.AgNO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com