
| A. | 甲醛、甲酸、甲酸甲酯和乙醇都能使酸性高锰酸钾溶液褪色 | |
| B. | 相同条件,等物质的量的乙醇、乙二醇、丙三醇中分别加入足量的金属钠产生氢气的体积之比是2:3:6 | |
| C. | 苯酚和乙醛都可以使溴水褪色,但发生的反应类型不同 | |
| D. | 溴水既可鉴别乙烷与乙烯,又可除去乙烷中的乙烯而得到纯净的乙烷 |
分析 A.甲醛、甲酸、甲酸甲酯都含有醛基,乙醇含有羟基,可被氧化;
B.等物质的量的乙醇、乙二醇、丙三醇含有的羟基数目比值为1:2:3;
C.苯酚与溴水发生取代反应,乙醛与溴水发生氧化还原反应;
D.乙烯含有碳碳双键,可与溴水发生加成反应.
解答 解:A.甲醛、甲酸、甲酸甲酯都含有醛基,乙醇含有羟基,可被氧化,都可被酸性高锰酸钾氧化,故A正确;
B.等物质的量的乙醇、乙二醇、丙三醇含有的羟基数目比值为1:2:3,则等物质的量的乙醇、乙二醇、丙三醇中分别加入足量的金属钠产生氢气的体积之比是1:2:3,故B错误;
C.苯酚含有酚羟基,可与溴水发生取代反应,乙醛与溴水发生氧化还原反应,反应类型不同,故C正确;
D.乙烷与溴水不反应,而乙烯含有碳碳双键,可与溴水发生加成反应,则溴水既可鉴别乙烷与乙烯,又可除去乙烷中的乙烯而得到纯净的乙烷,故D正确.
故选B.
点评 本题考查有机物的结构与性质,为高频考点,侧重于学生的分析能力的考查,把握官能团与性质的关系为解答的关键,题目难度不大.


 名题金卷系列答案
名题金卷系列答案科目:高中化学 来源: 题型:推断题
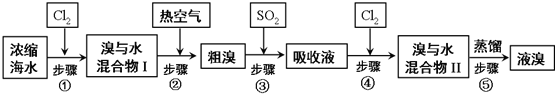
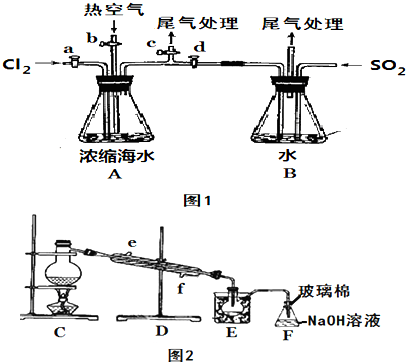
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢离子在银表面被还原,产生气泡 | B. | 银片质量逐渐增大 | ||
| C. | 电子从锌片经导线流向银片 | D. | 锌是负极,其质量逐渐减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
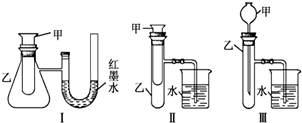
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| ⅠA | ⅧA | |||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | ⑧ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑨ | ||||
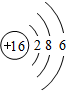 ;
; .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H1=-178.32kJ•mol-1△H2=-78.3kJ•mol-1 | |
| B. | △H1=178.32kJ•mol-1△H2=-78.3kJ•mol-1 | |
| C. | △H1=-178.32kJ•mol-1△H2=78.3kJ•mol-1 | |
| D. | △H1=178.32kJ•mol-1△H2=78.3kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{72}^{185}$Hf的质量数为72 | |
| B. | ${\;}_{72}^{185}$Hf的核外电子数为72 | |
| C. | ${\;}_{72}^{185}$Hf的中子数为103 | |
| D. | ${\;}_{72}^{185}$Hf与${\;}_{72}^{179}$Hf互为同素异形体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com