
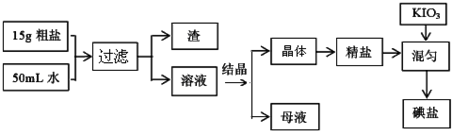
分析 15g粗盐溶于50ml水中过滤除去不溶性杂质,得到的溶液蒸发结晶得到氯化钠晶体加入碘酸钾混均得到碘盐;
(1)在检验SO42-时,加入氯化钡之前要先加盐酸以排除CO32-离子的干扰;
(2)过滤时,用到的玻璃仪器有漏斗、玻璃棒、烧杯;
(3)根据碘盐的含碘量=$\frac{m(碘)}{m(总)}$进行计算判断;
(4)反应生成碘,淀粉遇碘变蓝;
(5)根据碘盐中的碘酸钾在560℃开始分解产生无色气体即氧气,剩余固体加硝酸酸化的硝酸银有黄色沉淀说明有碘离子产生据此书写.
解答 解:(1)在检验SO42-时,加入氯化钡之前要先加盐酸以排除CO32-离子的干扰.即先加盐酸酸化,无现象,再加氯化钡溶液,出现白色沉淀,说明含有SO42-,
故答案为:取少量母液先加入稀盐酸酸化,再加入BaCl2溶液,若有白色沉淀,则说明有SO42-离子;
(2)过滤时,用到的玻璃仪器有漏斗、玻璃棒、烧杯,
故答案为:漏斗;玻璃棒;烧杯;
(3)根据碘盐的含碘量=$\frac{m(碘)}{m(总)}$=$\frac{1×1{0}^{-3}×0.001×127×1{0}^{-3}mg}{5×1{0}^{-3}kg}$=25.4mg/kg,
故答案为:25.4;不合格;
(4)反应生成碘,淀粉遇碘变蓝,则检验时,除需用KCNS外,还需要的一种试剂最好是淀粉,
故答案为:淀粉溶液;
(5)根据碘盐中的碘酸钾在560℃开始分解产生无色气体即氧气,剩余固体加硝酸酸化的硝酸银有黄色沉淀说明有碘离子产生,所以方程式为2KIO3$\frac{\underline{\;\;△\;\;}}{\;}$2KI+3O2↑,碘盐在热水中,也会反应生成两种单质,其中一种是无色气体,在反应后的溶液中滴加酚酞试液显红色说明生成碱,所以判断单质为碘单质和氧气,反应的化学方程式为12KIO3+6H2O$\frac{\underline{\;\;△\;\;}}{\;}$6I2+12KOH+15O2↑,
故答案为:2KIO3$\frac{\underline{\;\;△\;\;}}{\;}$KI+3O2↑;12KIO3+6H2O$\frac{\underline{\;\;△\;\;}}{\;}$6I2+12KOH+15O2↑.
点评 本题考查制取碘盐的流程,涉及硫酸根的检验、实验操作及计算等,侧重分析能力、知识迁移应用能力的综合考查,题目难度中等.


科目:高中化学 来源: 题型:选择题
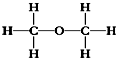 央视3•15曝光,在液化石油气中掺混二甲醚的事件.二甲醚(常压下沸点-24.9℃)是一种可溶于水的化工原料,常被用作一些燃料的替代品,其结构式如下.下列有关二甲醚的叙述中正确的是( )
央视3•15曝光,在液化石油气中掺混二甲醚的事件.二甲醚(常压下沸点-24.9℃)是一种可溶于水的化工原料,常被用作一些燃料的替代品,其结构式如下.下列有关二甲醚的叙述中正确的是( )| A. | 二甲醚和乙醇互为同分异构体且和甲醇互为同系物 | |
| B. | 二甲醚是一种有机物,属于非电解质 | |
| C. | 标准状况下,燃烧11.2L二甲醚一定生成22.4LCO2 | |
| D. | 4.6g该物质中含有共价键的数目为7×6.02×1022 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,11.2 L氧气所含的原子数为NA | |
| B. | 含NA个H2SO4分子的浓硫酸与足量铜反应可制得0.5mol SO2 | |
| C. | 15.6 g Na2O2与过量CO2反应时,转移的电子数为0.2NA | |
| D. | 标准状况下,0.5mol NO和0.5mol O2组成的混合气体,体积约为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ①②③ | C. | ②③④ | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:X>Y>Z | |
| B. | 气态氢化物稳定性按X、Y、Z依次减弱 | |
| C. | 非金属性:X>Y>Z | |
| D. | 阴离子还原性:X-<Y2-<Z3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
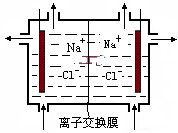
| A. | 离子交换膜既能让Na+通过,又能让OH-通过 | |
| B. | 阳极产生氯气和氢氧化钠 | |
| C. | 阴极区要定时添加饱和食盐水 | |
| D. | 阴极区流出的是氢氧化钠和氯化钠的混合溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

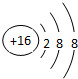 ;D与E能形成一种非极性分子,该分子的结构式为S=C=S;E的单质中,质软有润滑性的是石墨(填写单质名称).
;D与E能形成一种非极性分子,该分子的结构式为S=C=S;E的单质中,质软有润滑性的是石墨(填写单质名称).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
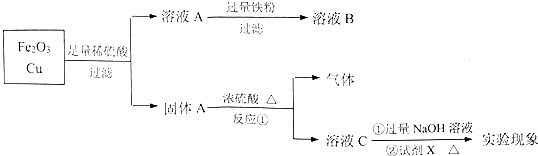
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C60是一种新型的化合物 | B. | C60的熔点高于石墨 | ||
| C. | C60和石墨都是碳的同素异形体 | D. | C60的摩尔质量为720 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com