
铅蓄电池的电极分别是Pb、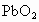 电解质是一定浓度的硫酸,工作时的反应方程式为:
电解质是一定浓度的硫酸,工作时的反应方程式为: .请写出放电时的电极反应式.
.请写出放电时的电极反应式.
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案科目:高中化学 来源:2013届吉林省高一下学期期初考试化学试卷 题型:填空题
(每空2分共计8分)铅蓄电池的电极分别是PbO2和Pb,电解质溶液为稀H2SO4溶液,工作时原电池的总反应式为PbO2+Pb+2H2SO4===2PbSO4+2H2O据上述变化判断:
①原电池的负极是 (填电极材料)。电极反应式
②工作时正极反应式为
③工作时电解质溶液的c(H+)_________(填“增大”、“不变”或“减小”)
查看答案和解析>>
科目:高中化学 来源: 题型:
(每空2分共计8分)铅蓄电池的电极分别是PbO2和Pb,电解质溶液为稀H2SO4溶液,工作时原电池的总反应式为PbO2+Pb+2H2SO4===2PbSO4+2H2O据上述变化判断:
①原电池的负极是 (填电极材料)。电极反应式
②工作时正极反应式为
③工作时电解质溶液的c(H+)_________(填“增大”、“不变”或“减小”)
查看答案和解析>>
科目:高中化学 来源:2010—2011学年吉林省油田高中高一下学期期初考试化学试卷 题型:填空题
(每空2分共计8分)铅蓄电池的电极分别是PbO2和Pb,电解质溶液为稀H2SO4溶液,工作时原电池的总反应式为PbO2+Pb+2H2SO4===2PbSO4+2H2O据上述变化判断:
①原电池的负极是 (填电极材料)。电极反应式
②工作时正极反应式为
③工作时电解质溶液的c(H+)_________(填“增大”、“不变”或“减小”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com