
| A. | 青铜是我国使用最早的合金 | |
| B. | 光导纤维做通讯材料有许多优点,但怕腐蚀,铺设也很不方便 | |
| C. | 高温结构陶瓷比金属材料具有许多优点,如不怕氧化、密度小等优点 | |
| D. | 光导纤维除用于通讯外,还可以用于医疗、信息处理等许多方面 |
分析 A.铜性质不活泼,易冶炼,为最早使用金属;
B.二氧化硅性质稳定;
C.高温结构陶瓷性质稳定,密度小;
D.光导纤维可以用于医疗、信息处理.
解答 解:A.铜性质不活泼,易冶炼,为最早使用的合金材料,如黄铜等,故A正确;
B.导纤维的主要成分是二氧化硅,二氧化硅性质稳定,耐腐蚀,故B错误;
C.高温结构陶瓷包括高温氧化物和高温非氧化物(或称难熔化合物)两大类,不怕氧化,密度小,故C正确;
D.光导纤维在信息传递方面有很多应用,如内窥镜、光纤通信等,故D正确.
故选B.
点评 本题考查较为综合,涉及合金、硅和二氧化硅的性质和用途,为高频考点,侧重考查化学与生活、生产的知识,有利于培养学生良好的科学素养,难度较小,注意基础知识的积累掌握.


科目:高中化学 来源: 题型:解答题
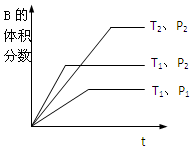 (1)在一定温度下,将2molA和2molB两种气体相混合后于容积为2L的某密闭容器中,发生如下反应3A(g)+B(g)?xC(g)+2D(g),2min末反应达到平衡状态,生成了0.8molD,并测得C的浓度为0.4mol/L,请填写下列空白:
(1)在一定温度下,将2molA和2molB两种气体相混合后于容积为2L的某密闭容器中,发生如下反应3A(g)+B(g)?xC(g)+2D(g),2min末反应达到平衡状态,生成了0.8molD,并测得C的浓度为0.4mol/L,请填写下列空白:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 编号 | ① | ② | ③ | ④ |
| 稀硝酸体积/mL | 100 | 200 | 300 | 400 |
| 剩余金属/g | 18.0 | 9. 6 | 0 | 0 |
| NO体积/mL | 2240 | 4480 | 6720 | V |
| A. | ①的上层清液中含有Fe2+、Fe3+、Cu2+ | |
| B. | 硝酸的浓度为1mol•L-1 | |
| C. | 每份混合物中铁粉的质量为16.8g | |
| D. | ④中V=11.2L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 明矾净水原理不涉及化学变化 | |
| B. | 现代科技已经能够拍到氢键的“照片”,直观地证实了水分子间的氢键是一个水分子中的氢原子与另一个水分子中的氧原子间形成的化学键 | |
| C. | 在食品袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质 | |
| D. | 将单质铜制成“纳米铜”时,具有非常强的化学活性,在空气中可以燃烧,说明“纳米铜”的还原性比铜片更强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CaO+H2O=Ca(OH)2 | B. | 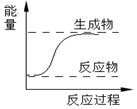 如图所示的反应为吸热反应 | ||
| C. | Fe2O3+2Al $\frac{\underline{\;高温\;}}{\;}$ 2Fe+Al2O3 | D. | 2Na+O2 $\frac{\underline{\;点燃\;}}{\;}$ Na2O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com