
【题目】一定温度下,在甲、乙、丙、丁四个恒容密闭容器中投入SO2(g)和O2(g),进行反应,2SO2+O22SO3,其起始物质的量及SO2的平衡转化率如下表所示.下列判断中正确的是( )
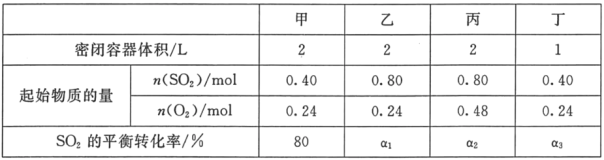
A.该温度下,该反应的平衡常数K为400
B.SO2的平衡转化率:a1>a2=a3
C.达到平衡时,容器丁中的正反应速率比容器丙中的大
D.达到平衡时,容器丙中c( SO3)大于容器甲中c( SO3)的两倍
【答案】AD
【解析】
对比四个容器投料和体积,乙与甲比较, SO2的投料加倍了,则平衡正向移动;丙与甲比较,投料是甲的两倍,相当于增大了压强,平衡正向移动;丁与甲比较,体积缩小了一倍,也相当于增大了压强,平衡正向移动。
A、2SO2+O22SO3,
开始 0.2 0.12 0
转化 0.16 0.08 0.16
平衡 0.04 0.04 0.16
K=![]() =400,故A正确;
=400,故A正确;
B、乙、丙相比,丙中氧气浓度大,丙、丁相比浓度相同,则SO2的平衡转化率:a1<a2=a3,故B错误;
C、丙、丁相比浓度相同,温度相同,则达到平衡时,容器丁中的正反应速率等于容器丙中的,故C错误;
D、甲、丙相比,丙中浓度为甲的2倍,且增大压强平衡正向移动,则达到平衡时,容器丙中c( SO3)大于容器甲中c(SO3)的两倍,故D正确;
答案选AD。


科目:高中化学 来源: 题型:
【题目】某学生用下图所示装置研究化学反应X+2Y=2Z的能量变化情况。向试管中滴加试剂Y时,看到U形管中液面甲下降,液面乙上升。下列关于该反应的叙述中正确的是( )
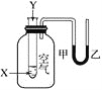
①该反应释放能量;②生成物的总能量比反应物的总能量高;③该反应过程可以看成是“贮存”于X、Y内部的能量转化为热量而释放出来。
A. ①②③B. ①③C. ①②D. ②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由CO2、H2和CO组成的混合气体在同温同压下与氮气的密度相同,则该混合气体中CO2、H2和CO的体积比可能为( )
A.13:8:29B.22:1:14C.29:8:13D.44:2:23
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是( )
A.实验室用浓盐酸和MnO2混合加热制Cl2:MnO2+4H++2Cl﹣![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
B.将Cl2溶于水制备次氯酸:Cl2+H2O=2H++Cl﹣+ClO﹣
C.用过量的NaOH溶液吸收SO2:OH﹣+SO2=HSO3﹣
D.向AlCl3溶液中加入氨水:Al3++3OH﹣=Al(OH)3↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A为常见的金属单质,根据下图所示的关系:
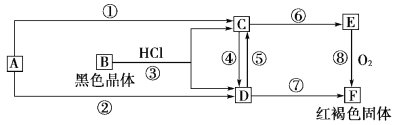
(1)确定A、B、C、D、E、F的化学式,A为________,B为________,C为________,D为________,E为________,F为________。
(2)写出⑧的化学方程式,④、⑤的离子方程式。
⑧_________________________________________________,
④________________________________________________,
⑤___________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是 ( )
A.氢氧化铁胶体制备的化学方程式为:FeCl3+H2O![]() Fe(OH) 3 ↓+3HCl
Fe(OH) 3 ↓+3HCl
B.在硫酸氢钾溶液中加入Ba(OH)2溶液至过量:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O
C.少量氯气通入溴化亚铁溶液中:Cl2+2Br- =Br2+2Cl-
D.向Fe(OH)3中加入氢碘酸:2Fe(OH)3+6H++2I-=2Fe2++I2+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A. 当H2O与Na2O2反应生成1molO2时,转移的电子数目为2×6.02×1023
B. 用pH均为2的盐酸和醋酸分别中和等物质的量的NaOH,消耗醋酸的体积更大
C. 常温下2S2O(g)![]() 3S(s)+SO2(g)能自发进行,可推断该反应为吸热反应
3S(s)+SO2(g)能自发进行,可推断该反应为吸热反应
D. 氯水通入SO2后溶液的酸性减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中进行A(g)+2B(s)![]() 2C(s)+3D(s) ΔH>0的反应,下列说法正确的是( )
2C(s)+3D(s) ΔH>0的反应,下列说法正确的是( )
A. 升高温度,正反应速率增大,逆反应速率减小
B. 容器内气体平均相对分子质量不变时达到化学平衡状态
C. 温度不变,增大B的投入量,正反应速率增大
D. 温度不变,压缩容器体积重新达到平衡后,A的浓度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法正确的是( )
A. 标准状况下,22.4 L氢气中含有2NA个中子
B. 0.1NA个氯化氢分子占有体积为2.24 L
C. 2克金属钙变成钙离子时失去的电子数为0.1NA
D. 50 mL 0.1 mol·L-1H2SO4溶液中含有H+数为0.005NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com