
| A. | SO2、SiO2、CO均为酸性氧化物 | |
| B. | 稀豆浆、硅酸、氯化铁溶液均为胶体 | |
| C. | 烧碱、氨、四氯化碳均为电解质 | |
| D. | 胶体、食用盐、点豆腐的卤水均为混合物 |
分析 A、酸性氧化物是指能和碱反应生成盐和水的化合物;
B、胶体分散系的分散质微粒直径介于1nm-100nm;
C、电解质是指在水溶液或是熔融状态下能导电的化合物;
D、混合物是指由不同分子构成的物质.
解答 解:A、SO2、SiO2均能和碱反应生成盐和水,属于酸性氧化物,但是CO不属于酸性氧化物,故A错误;
B、稀豆浆、硅酸均为胶体,氯化铁溶液属于溶液,故B错误;
C、电解质是指在水溶液或是熔融状态下能导电的化合物,烧碱属于电解质、氨、四氯化碳属于非电解质,故C错误;
D、胶体、食用盐、点豆腐的卤水由不同分子构成,属于混合物,故D正确.
故选D.
点评 本题是对物质的化学式及分类的考查,对物质的名称、分类及化学式有较明确的认识即可顺利解答,属基础知识考查题,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | ④⑥ | B. | ①③⑤ | C. | ③④⑥ | D. | ①④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 强电解质:盐酸、氢氧化钡、明矾 | B. | 弱电解质:甲酸、纯碱、醋酸铵 | ||
| C. | 非电解质:液氨、二氧化硫、苯 | D. | 同系物:CH2O2、C2H4O2、C3H6O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3被氧化,表现氧化性 | |
| B. | 此条件下氧化性强弱为:Cl2>N2 | |
| C. | 若有8mol NH3 被氧化,生成的N2体积(标准状况)为22.4L | |
| D. | 若有3 mol e-转移,被还原的Cl2的物质的量为3mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| NaOH溶液 | 银氨溶液 | 新制Cu(OH)2 | 金属钠 | |
| A | 发生水解 | 无银镜反应 | 不反应 | 不反应 |
| B | 发生中和反应 | 无银镜反应 | 溶解 | 放出H2 |
| C | 不反应 | 有银镜反应 | 有红色沉淀 | 放出H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 铁粉与稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 钠与水反应:Na+H2O═Na++OH-+H2↑ | |
| C. | 二氧化碳通入澄清石灰水中CO2+Ca2++2OH-═CaCO3↓+H2O | |
| D. | 氢氧化钡溶液与盐酸混合OH-+H+═H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 降低温度,H2S浓度减小,表明该反应是吸热反应 | |
| B. | 通入CO后,正反应速率逐渐增大 | |
| C. | 反应前H2S物质的量为10 mol | |
| D. | H2S的平衡转化率为28.6% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
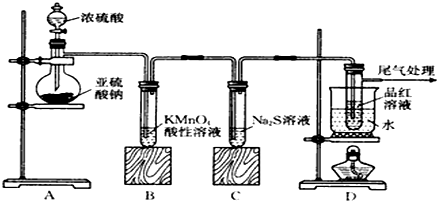
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com