
”¾ĢāÄæ”æÓŠ»śĪļFŹĒŅ»ÖÖÓĆĶ¾¹ć·ŗµÄĻćĮĻ,æÉÓĆĢžAÓėÓŠ»śĪļEĪŖŌĮĻ,°“ÕÕČēĻĀĮ÷³Ģ½ųŠŠŗĻ³É”£ŅŃÖŖAŌŚ±ź×¼×“æöĻĀµÄĆܶČĪŖ1.25 g”¤L-1”£
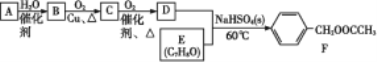
»Ų“šĻĀĮŠĪŹĢā:
(1)ÓŠ»śĪļFÖŠŗ¬ÓŠµÄ¹ŁÄÜĶÅĆū³ĘĪŖ____”£
(2)AÉś³ÉBµÄ·“Ó¦ĄąŠĶĪŖ________”£
(3)Š“³öĮ÷³ĢÖŠBÉś³ÉCµÄ»Æѧ·½³ĢŹ½_______”£
(4)ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ____”£
A Į÷³ĢĶ¼ÖŠÓŠ»śĪļB×Ŗ»ÆĪŖC£¬Cu²ĪÓėĮĖ»Æѧ·“Ó¦,µ«·“Ó¦Ē°ŗóµÄÖŹĮæ±£³Ö²»±ä
B ÓŠ»śĪļC²»æÉÄÜŹ¹äåĖ®ĶŹÉ«
C ÓŠ»śĪļD”¢EÉś³ÉFµÄ·“Ó¦ĪŖõ„»Æ·“Ó¦,±¾ÖŹÉĻŹĒČ”“ś·“Ó¦
D ŗĻ³É¹ż³ĢÖŠŌ×ӵĥķĀŪĄūÓĆĀŹĪŖ100%µÄ·“Ó¦Ö»ÓŠŅ»øö
”¾“š°ø”æõ„»ł ¼Ó³É·“Ó¦ 2CH3CH2OH+O2![]() 2CH3CHO+2H2O AC
2CH3CHO+2H2O AC
”¾½āĪö”æ
ÓÉAŌŚ±ź×¼×“æöĻĀµÄĆܶČæÉŅŌĒó³öAµÄĻą¶Ō·Ö×ÓÖŹĮæĪŖ22.4 L”¤mol-1”Į1.25 g”¤L-1=28 g”¤mol-1£¬A ĪŖCH2=CH2£¬ŗĶĖ®¼Ó³ÉÉś³ÉŅŅ“¼£¬BĪŖCH3CH2OH£¬ŅŅ“¼“ß»ÆŃõ»ÆÉś³ÉŅŅČ©£¬CĪŖCH3CHO£¬ŅŅČ©ŌŁ“ß»ÆŃõ»ÆĪŖŅŅĖį£¬DĪŖCH3COOH”£FĪŖŅŅĖį±½¼×õ„£¬ÓÉŅŅĖįŗĶEÉś³É£¬¹ŹEĪŖ±½¼×“¼”£
£Ø1£©FŹĒõ„£¬ŗ¬ÓŠµÄ¹ŁÄÜĶÅĪŖõ„»ł£»
£Ø2£©ŅŅĻ©Éś³ÉŅŅ“¼ŹĒ·¢ÉśĮĖŅŅĻ©ŗĶĖ®µÄ¼Ó³É·“Ó¦£¬¹Ź·“Ó¦ĄąŠĶĪŖ¼Ó³É·“Ó¦£»
£Ø3£©ŅŅ“¼“ß»ÆŃõ»ÆÉś³ÉŅŅČ©µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ2CH3CH2OH+O2![]() 2CH3CHO+2H2O£»
2CH3CHO+2H2O£»
£Ø4£©A.ŅŅ“¼×Ŗ»ÆĪŖŅŅČ©µÄ·“Ó¦ÖŠ£¬CuŹĒ“߻ƼĮ£¬CuĻČŗĶŃõĘųÉś³ÉCuO£¬CuOŌŁŗĶŅŅ“¼Éś³ÉCuŗĶŅŅČ©£¬ĖłŅŌCu²ĪÓėĮĖ»Æѧ·“Ó¦,µ«·“Ó¦Ē°ŗóµÄÖŹĮæ±£³Ö²»±ä£¬¹ŹAÕżČ·£»
B.ŅŅČ©ÓŠ»¹ŌŠŌ£¬æÉŅŌ±»äåĖ®ÖŠµÄäåŃõ»Æ“Ó¶ųŹ¹äåĖ®ĶŹÉ«£¬¹ŹB“ķĪó£»
C.ŅŅĖįŗĶ±½¼×“¼Éś³ÉŅŅĖį±½¼×õ„µÄ·“Ó¦ŹĒõ„»Æ·“Ó¦£¬±¾ÖŹÉĻŹĒČ”“ś·“Ó¦£¬¹ŹCÕżČ·£»
D.ŗĻ³É¹ż³ĢÖŠŌ×ӵĥķĀŪĄūÓĆĀŹĪŖ100%µÄ·“Ó¦ÓŠ2øö£¬·Ö±šŹĒŅŅĻ©¼Ó³ÉÉś³ÉŅŅ“¼ŗĶŅŅČ©“ß»ÆŃõ»ÆĪŖŅŅĖį”£¹ŹD“ķĪó”£
¹ŹŃ”AC”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻņ100mL FeI2ČÜŅŗÖŠÖš½„ĶØČėCl2(ČÜŅŗĢå»ż±ä»ÆŗöĀŌ²»¼Ę),Éś³ÉI2”¢Fe3+µÄĪļÖŹµÄĮæĖęĶØČėCl2µÄĪļÖŹµÄĮæµÄ±ä»ÆČēĶ¼ĖłŹ¾,ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ( )
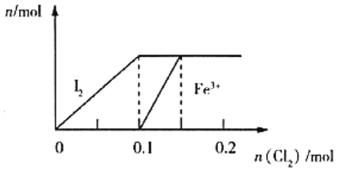
A.»¹ŌŠŌĒæČõ:Fe2+£¼I-
B.n(Cl2)=0.05molŹ±,ČÜŅŗÖŠI-µÄĪļÖŹµÄĮæÅضČĪŖ0.1mol”¤L-1
C.Čōn(Cl2):n(FeI2)=6:5,·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ2Fe2++10I-+6Cl2=5I2+2Fe3++12Cl-
D.n(Cl2)=0.12molŹ±,ČÜŅŗÖŠµÄĄė×ÓÖ÷ŅŖÓŠFe3+”¢Cl-
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŹµŃéŹŅÓūÓĆNaOH¹ĢĢåÅäÖĘ1.0 mol”¤L1µÄNaOHČÜŅŗ240 mL£ŗ
(1)ÅäÖĘČÜŅŗŹ±£¬Ņ»°ćæÉŅŌ·ÖĪŖŅŌĻĀ¼øøö²½Öč£ŗ
¢Ł³ĘĮæ””¢Ś¼ĘĖć””¢ŪČܽā””¢Üµ¹×ŖŅ”ŌČ””¢Ż×ŖŅĘ ¢ŽĻ“µÓ””¢ß¶ØČŻ””¢ąĄäČ“
ĘäÕżČ·µÄ²Ł×÷Ė³ŠņĪŖ________________”£±¾ŹµŃé±ŲŠėÓƵ½µÄŅĒĘ÷ÓŠĢģĘ½”¢Ņ©³×”¢²£Į§°ō”¢ÉÕ±”¢½ŗĶ·µĪ¹Ü”¢»¹ÓŠ________”£
(2)ijĶ¬Ń§Óū³ĘĮæŅ»¶ØĮæµÄNaOH¹ĢĢ壬ĖūĻČÓĆĶŠÅĢĢģĘ½³ĘĮæÉÕ±µÄÖŹĮ棬ĢģĘ½Ę½ŗāŗóµÄדĢ¬ČēĶ¼”£ÉÕ±µÄŹµ¼ŹÖŹĮæĪŖ____________ g£¬ŅŖĶź³É±¾ŹµŃéøĆĶ¬Ń§Ó¦³Ę³ö____________ g NaOH”£
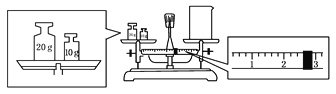
(3)Ź¹ÓĆČŻĮæĘæĒ°±ŲŠė½ųŠŠµÄŅ»²½²Ł×÷ŹĒ________”£
(4)ŌŚÅäÖĘ¹ż³ĢÖŠ£¬ĘäĖū²Ł×÷¶¼ŹĒÕżČ·µÄ£¬ĻĀĮŠ²Ł×÷»įŅżĘšÅضČĘ«øߵďĒ________”£
¢ŁĆ»ÓŠĻ“µÓÉÕ±ŗĶ²£Į§°ō
¢Ś×ŖŅĘČÜŅŗŹ±²»É÷ÓŠÉŁĮæČ÷µ½ČŻĮæĘæĶāĆę
¢ŪČŻĮæĘæ²»øÉŌļ£¬ŗ¬ÓŠÉŁĮæÕōĮóĖ®
¢Ü¶ØČŻŹ±ø©ŹÓæĢ¶ČĻß
¢ŻĪ“ĄäČ“µ½ŹŅĪĀ¾Ķ½«ČÜŅŗ×ŖŅʵ½ČŻĮæĘæ²¢¶ØČŻ
¢Ž¶ØČŻŗóČūÉĻĘæČū·“ø“Ņ”ŌČ£¬¾²ÖĆŗó£¬ŅŗĆęµĶÓŚæĢ¶ČĻߣ¬ŌŁ¼ÓĖ®ÖĮæĢ¶ČĻß
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĮ¢·½Ķé(C8H8)Ęä°ĖøöĢ¼Ō×Ó¶Ō³ĘµŲÅÅĮŠŌŚĮ¢·½ĢåµÄ°Ėøö½ĒÉĻ”£ŅŌĻĀĻą¹ŲĖµ·Ø“ķĪóµÄŹĒ
A.Į¢·½ĶéŹĒ±½(C6H6)µÄĶ¬ĻµĪļ
B.Į¢·½ĶéŅ»ĀČ“śĪļ1ÖÖ”¢¶žĀČ“śĪļÓŠ3ÖÖ
C.Į¢·½ĶéŌŚæÕĘųÖŠæÉČ¼£¬Č¼ÉÕÓŠŗŚŃĢ²śÉś
D.Į¢·½ĶéČżĀČ“śĪļŗĶĪåĀČ“śĪļÖÖĄąĻąĶ¬
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚ2 LµÄĆܱÕČŻĘ÷ÄŚ£¬800”ꏱ·“Ó¦2NO(g)£«O2(g)2NO2(g)ĢåĻµÖŠ£¬n(NO)Ėꏱ¼äµÄ±ä»ÆČē±ķ£ŗ
Ź±¼ä(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
£Ø1£©Š“³öøĆ·“Ó¦µÄĘ½ŗā³£Źż±ķ“ļŹ½£ŗK£½___________________________”£ŅŃÖŖ£ŗK300”ę>K350”ę£¬ŌņøĆ·“Ó¦ŹĒ______ČČ·“Ó¦”£
£Ø2£©ĻĀĶ¼±ķŹ¾NO2±ä»ÆµÄĒśĻߏĒ____”£ÓĆO2±ķŹ¾“Ó0”«2 sÄŚøĆ·“Ó¦µÄĘ½¾łĖŁĀŹv£½_________”£

£Ø3£©ÄÜĖµĆ÷øĆ·“Ó¦ŅŃ“ļµ½Ę½ŗāדĢ¬µÄŹĒ________”£
a£®v(NO2)£½2v(O2) b£®ČŻĘ÷ÄŚŃ¹Ēæ±£³Ö²»±ä
c£®vÄę(NO)£½2vÕż(O2) d£®ČŻĘ÷ÄŚĆܶȱ£³Ö²»±ä
£Ø4£©ĪŖŹ¹øĆ·“Ó¦µÄ·“Ó¦ĖŁĀŹŌö“ó£¬ĒŅĘ½ŗāĻņÕż·“Ó¦·½ĻņŅĘ¶ÆµÄŹĒ________”£””””””””””””””””””””””””””””””””””
a£®¼°Ź±·ÖĄė³öNO2ĘųĢå b£®ŹŹµ±ÉżøßĪĀ¶Č
c£®Ōö“óO2µÄÅØ¶Č d£®Ń”Ōńøߊ§“߻ƼĮ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijČÜŅŗÖŠ¼ÓČėĀĮ·ŪÄܷųöĒāĘų£¬“ĖČÜŅŗÖŠŅ»¶ØÄÜ“óĮæ¹²“ęµÄĄė×Ó×éŹĒ(””””)
A.H+”¢Cu2+”¢Cl©”¢![]() B. HCO3-”¢NO3-”¢SO42-”¢Na+
B. HCO3-ӢNO3-ӢSO42-ӢNa+
C.Cl©”¢SO42-”¢Na+”¢K+D.Fe3+”¢SO42-”¢Cl©”¢AlO2-
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ(””””)
A.SO2µÄĖ®ČÜŅŗÄܵ¼µē£¬¹ŹSO2ĪŖµē½āÖŹ
B.ŃōĄė×ÓŌŚ·“Ó¦ÖŠÖ»ÄܵƵē×Ó±»»¹Ō×÷Ńõ»Æ¼Į
C.±ź×¼×“æöĻĀ£¬6.72LµÄNH3µÄĪļÖŹµÄĮæĪŖ0.3mol
D.ĀČĖ®”¢Ņŗ°±”¢æÕĘų”¢ŃĪĖį¶¼ŹĒ»ģŗĻĪļ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ5©¶ž¼×Ńõ»ł±½·ÓŹĒÖŲŅŖµÄÓŠ»śŗĻ³ÉÖŠ¼äĢ壬æÉÓĆÓŚĢģČ»ĪļÖŹ°×ÄūĆŹĖŲµÄŗĻ³É£¬Ņ»ÖÖŅŌ¼ä±½Čż·ÓĪŖŌĮĻµÄŗĻ³É·“Ó¦ČēĻĀ£ŗ

¼×“¼”¢ŅŅĆŃŗĶ3£¬5©¶ž¼×Ńõ»ł±½·ÓµÄ²æ·ÖĪļĄķŠŌÖŹ¼ūĻĀ±ķ£ŗ
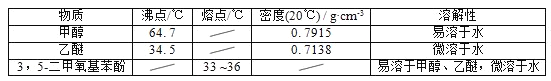
£Ø1£©·“Ó¦½įŹųŗó£¬ĻČ·ÖĄė³ö¼×“¼£¬ŌŁ¼ÓČėŅŅĆŃ½ųŠŠŻĶČ”£¬¢Ł·ÖĄė³ö¼×“¼µÄ²Ł×÷ŹĒµÄ______£»¢ŚŻĶČ”ÓƵ½µÄ·ÖŅŗĀ©¶·Ź¹ÓĆĒ°Šč__________________²¢Ļ“¾»£¬·ÖŅŗŹ±ÓŠ»ś²ćŌŚ·ÖŅŗĀ©¶·µÄ________Ģī£Ø”°ÉĻ”±»ņ”°ĻĀ”±£©²ć£»
£Ø2£©·ÖĄėµĆµ½µÄÓŠ»ś²ćŅĄ“ĪÓƱ„ŗĶNaHCO3ČÜŅŗ”¢±„ŗĶŹ³ŃĪĖ®”¢ÉŁĮæÕōĮóĖ®½ųŠŠĻ“µÓ£®ÓƱ„ŗĶNaHCO3ČÜŅŗĻ“µÓµÄÄæµÄŹĒ__£¬ÓƱ„ŗĶŹ³ŃĪĖ®Ļ“µÓµÄÄæµÄŹĒ______£»
£Ø3£©Ļ“µÓĶź³Éŗó£¬ĶعżŅŌĻĀ²Ł×÷·ÖĄė”¢Ģį“æ²śĪļ£¬ÕżČ·µÄ²Ł×÷Ė³ŠņŹĒ__£ØĢī×ÖÄø£©£»
a£®ÕōĮó³żČ„ŅŅĆŃ b£®ÖŲ½į¾§ c£®¹żĀĖ³żČ„øÉŌļ¼Į d£®¼ÓČėĪŽĖ®CaCl2øÉŌļ
£Ø4£©¹ĢŅŗ·ÖĄė³£²ÉÓĆ¼õŃ¹¹żĀĖ£®ĪŖĮĖ·ĄÖ¹µ¹Īü£¬¼õŃ¹¹żĀĖĶź³ÉŗóÓ¦ĻČ________________£¬ŌŁ______”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ25”ꏱ£¬ŌŚŗ¬CH3COOHŗĶCH3COO-µÄČÜŅŗÖŠ£¬ CH3COOH”¢CH3COO-¶žÕßÖŠø÷×ŌĖłÕ¼µÄĪļÖŹµÄĮæ·ÖŹż(a)ĖęČÜŅŗpH±ä»ÆµÄ¹ŲĻµČēĶ¼ĖłŹ¾”£

ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
A. ŌŚpH<4.76µÄČÜŅŗÖŠ£¬c(CH3COO-)<c(CH3COOH)
B. ŌŚpH=7µÄČÜŅŗÖŠ£¬a(CH3COOH)=0£¬a(CH3COO-)=1.0
C. ŌŚpH>4.76µÄČÜŅŗÖŠ£¬c(CH3COO-)Óėc(OH-)Ö®ŗĶæÉ“óÓŚc(H+)
D. ŌŚpH=4.76µÄČÜŅŗÖŠ¼ÓŃĪĖį£¬a(CH3COOH)Óėa(CH3COO-)Ö®ŗĶ±£³Ö²»±ä
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com