
Ϊ��֤���ʵ�Ũ�ȶԻ�ѧ��Ӧ���ʵ�Ӱ�죬����1 mol ? L-1���������ڴ��ձ��У���ȡ3mL0.1 mol ? L-1��Na2S2O3��Һ��3 mL�����ᷴӦ���������Ի���Լ��80s���ڶ�������3 mL 0.2 mol ? L-1��Na2S2O3��Һ��ԭ����3mL��Ӧ����������Ҳ��80s ���ң���֪��Na2S2O3+2HCl = 2NaCl+S��+ SO2��+H2O�������й��ڸ�ʵ������ۼ�������ȷ���ǣ� ��
A��Ũ�ȶԷ�Ӧ���ʵ�Ӱ�첻��
B���ڶ������õ�����Ũ�Ƚ�ϡ
C���÷�Ӧ�������ʾ������������������Ʊ�ʾ��������ֵ���
D���κλ�ѧ��Ӧ����Ӧʱ����ͬ����ѧ��Ӧ���ʾ���ͬ
 ��ս�п�����ϵ�д�
��ս�п�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| �� |
| �� |
| Ũ���� |
| �� |
| Ũ���� |
| �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012���㽭ʡ����һ�и�����ѧ�ڻ�ͷ���Ի�ѧ�Ծ� ���ͣ�ʵ����
ʳ��Ϊ��������ƴ����֡����ұ��涨����ʳ�����Ậ�����õ���3��5g��100mL��
��1��ij�о�С�����õζ��������ⶨijƷ��ʳ���д���ĺ���������˵����ȷ����______
a����NaOH��Һ�ζ�ʱ��Ӧ�����ӷ���ʽΪ��H++OH-=H2O
b��ʳ��������ϡ��һ���������ٽ��еζ�
c����NaOH��Һ�ζ�ʳ�ף���ʹ�÷�̪�������ָʾ��
d������ø�Ʒ��ʳ�����ʵ���Ũ��Ϊ0.75mol��L-1�����ʳ��������Ϊ4.5g/100mL��
��2���о�С���ͬѧ��ϸ�۲��˸�Ʒ��ʳ�ı�ǩ���������л����б���������ΪʳƷ���Ӽ������������Ϸ���֤������ʳƷ���Ӽ�����������C6H5COONa�����ᷢ�����ӻ�����Ӧ���������һ���¶��µĴ����뱽�����________ ����д��ţ���
a��pH b������� c�����볣�� d���ܽ��
��3�������£���0.1000 mol��L-1NaOH��Һ�ֱ�ζ�20.00mL 0��1000 mol��L-1HCl��Һ��20.00mL 0.1000 mol��L-1CH3COOH��Һ���õ�2���ζ����ߣ�����ͼ��ʾ��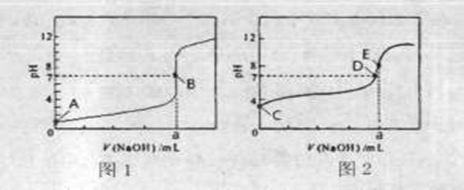
�ٵζ�������Һ��������_______ ���ͼl����ͼ2�������ζ�������a=_____ mL��
��E��pH>8��ԭ�������ӷ���ʽ��ʾ________��
��4���������Բⶨһδ֪Ũ�ȵ�CH3COOH��Һ�ĵ���ȣ�Ӧ����ʵ���������Լ�����ֽ����________����д��ţ�
a����⣬NaOH��Һ b������Na2CO3��Һ
c��������Ӧ��ʯ����Һ d���к͵ζ���pH��ֽ
��5��Ϊ�궨ij������Һ��ȷŨ�ȣ���0.2000 mol?L-1 ��NaOH��Һ��20.00 mL������Һ���еζ������εζ�����NaOH��Һ��������£�
| ʵ����� | 1 | 2 | 3 | 4 |
| ����NaOH��Һ�������mL�� | 20.05 | 20.00 | 18.80 | 19.95 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ���㽭ʡ������ѧ�ڻ�ͷ���Ի�ѧ�Ծ� ���ͣ�ʵ����
ʳ��Ϊ��������ƴ����֡����ұ��涨����ʳ�����Ậ�����õ���3��5g��100mL��
��1��ij�о�С�����õζ��������ⶨijƷ��ʳ���д���ĺ���������˵����ȷ����______
a����NaOH��Һ�ζ�ʱ��Ӧ�����ӷ���ʽΪ��H++OH-=H2O
b��ʳ��������ϡ��һ���������ٽ��еζ�
c����NaOH��Һ�ζ�ʳ�ף���ʹ�÷�̪�������ָʾ��
d������ø�Ʒ��ʳ�����ʵ���Ũ��Ϊ0.75mol��L-1�����ʳ��������Ϊ4.5g/100mL��
��2���о�С���ͬѧ��ϸ�۲��˸�Ʒ��ʳ�ı�ǩ���������л����б���������ΪʳƷ���Ӽ������������Ϸ���֤������ʳƷ���Ӽ�����������C6H5COONa�����ᷢ�����ӻ�����Ӧ���������һ���¶��µĴ����뱽�����________ ����д��ţ���
a��pH b������� c�����볣�� d���ܽ��
��3�������£���0.1000 mol��L-1NaOH��Һ�ֱ�ζ�20.00mL 0��1000 mol��L-1HCl��Һ��20.00mL 0.1000 mol��L-1CH3COOH��Һ���õ�2���ζ����ߣ�����ͼ��ʾ��
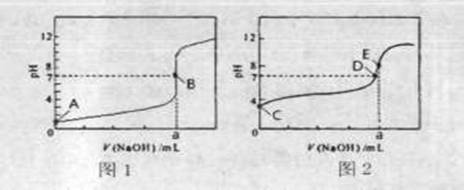
�ٵζ�������Һ��������_______ ���ͼl����ͼ2�������ζ�������a=_____ mL��
��E��pH>8��ԭ�������ӷ���ʽ��ʾ________��
��4���������Բⶨһδ֪Ũ�ȵ�CH3COOH��Һ�ĵ���ȣ�Ӧ����ʵ���������Լ�����ֽ����________����д��ţ�
a����⣬NaOH��Һ b������Na2CO3��Һ
c��������Ӧ��ʯ����Һ d���к͵ζ���pH��ֽ
��5��Ϊ�궨ij������Һ��ȷŨ�ȣ���0.2000 mol•L-1 ��NaOH��Һ��20.00 mL������Һ���еζ������εζ�����NaOH��Һ��������£�
|
ʵ����� |
1 |
2 |
3 |
4 |
|
����NaOH��Һ�������mL�� |
20.05 |
20.00 |
18.80 |
19.95 |
��ô�����Һ��ȷŨ��Ϊ________ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
I���ɻ�β���е�NO���ƻ������㡣���ô�
������ʹβ���е�NO��CO������Ӧ2NO +2CO
![]() 2CO2��+N2����H<0����֪��������ȱ���������ѧ��Ӧ���ʡ�Ϊ�˷ֱ���֤�¶ȡ������ȱ�������Ի�ѧ��Ӧ���ʵ�Ӱ����ɣ�ijͬѧ���������ʵ�飬����ʵ�������Ѿ���������ʵ����Ʊ���
2CO2��+N2����H<0����֪��������ȱ���������ѧ��Ӧ���ʡ�Ϊ�˷ֱ���֤�¶ȡ������ȱ�������Ի�ѧ��Ӧ���ʵ�Ӱ����ɣ�ijͬѧ���������ʵ�飬����ʵ�������Ѿ���������ʵ����Ʊ���
| ʵ���� | T���棩 | NO��ʼŨ�ȣ�mol/L�� | CO��ʼŨ�ȣ�mol/L�� | �����ıȱ������m2/g�� |
| �� | 280 | 1.20��10-3 | 5.80��10-3 | 82 |
| �� | 1.20��10-3 | 124 | ||
| �� | 350 | 5.80��10-3 |
��1������ȫ���еĸ��ո�
��2�������ұ߸���������ͼ�У������ϱ��е���
 ��ʵ�������»��������NOŨ����ʱ���
��ʵ�������»��������NOŨ����ʱ���
������������ͼ���������������ߵ�ʵ���š�
II��������ȼ������ʱ�����ĸ��»�����N2��O2�ķ�Ӧ��
N2��g��+O2��g��![]() =2NO��g���ǵ�������β��
=2NO��g���ǵ�������β��
�к���NO��ԭ��֮һ��
2000Cʱ�����ݻ�Ϊ2L���ܱ������г���10molN2��5mol O2���ﵽƽ���NO�����ʵ���Ϊ2mol����÷�Ӧ��ƽ�ⳣ��K=___ _ �����¶��£�����ʼʱ�����������г���1 molN2��һ������O2��ƽ��ʱO2��NO�����ʵ���ǡ����ȣ���ƽ ��ʱN2�����ʵ����� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com