
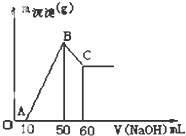
 把一小块镁铝金溶于100mL盐酸中,然后向其中滴入1mol?L-1NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积如图所示.
把一小块镁铝金溶于100mL盐酸中,然后向其中滴入1mol?L-1NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积如图所示.| n |
| V |
| 1mol/L?50×10-3L |
| 0.1L |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、氨水中加入稀硝酸:NH3?H2O+H+═NH4++H2O |
| B、Ag与Cu(NO3)2反应:Ag+Cu2+═Cu+Ag+ |
| C、碳酸氢铵与NaOH反应:NH4++OH-═NH3↑+H2O |
| D、CuSO4与Ba(OH)2反应:SO42-+Ba2+═BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaHCO3溶液与醋酸:CO32-+2CH3COOH=2CH3COO-+H2O+CO2↑ |
| B、硝酸银溶液与铜:Cu+Ag+=Cu2++Ag |
| C、将足量的铁粉投入稀硝酸中:Fe+NO3-+4 H+=Fe3++NO↑+2H2O |
| D、用醋酸除水垢:2CH3COOH+CaCO3=Ca2++2CH3COO-+H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②③④⑥⑦ | B、①②⑤ |
| C、②⑦⑧ | D、①⑤⑨ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、易溶与难溶固体混合物用溶解过滤方法提纯 |
| B、沸点不同的互溶液体可用蒸馏分离 |
| C、用酒精可以从碘水中萃取碘 |
| D、汽油和水的混合物可以用分液漏斗分离 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com