
【题目】4种相邻主族短周期元素的相对位置如表,元素x的原子核外电子数是m的2倍,y的氧化物具有两性.![]() 称为拟卤素,性质与卤素相似.下列说法不正确的是( )
称为拟卤素,性质与卤素相似.下列说法不正确的是( )
M | N | ||
X | Y |
A.X位于三周期IIA,其单质可采用电解熔融![]() 制备
制备
B.元素最高价氧化物的水化物中,酸性最强的是![]()
C.气体分子![]() 的电子式为
的电子式为![]()
D.![]() 其与氢氧化钠溶液反应的化学方程式为
其与氢氧化钠溶液反应的化学方程式为![]()
【答案】D
【解析】
4种元素都是短周期元素,且为相邻主族,根据元素在周期表中的位置知,M和N位于第二周期、X和Y位于第三周期,X原子核外电子数是M的2倍,Y的氧化物具有两性,则Y是Al元素,根据元素相对位置可知,X是Mg元素、M是C元素、N元素为N元素。
A.元素X是Mg元素,其原子序数为12,在周期表中的位置是第三周期第IIA族,镁单质可采用电解熔融![]() 制备,故A正确;
制备,故A正确;
B.M、N、X、Y分别是C、N、Mg、Al,元素的非金属性越强,其最高价氧化物的水化物酸性越强,这四种种元素中非金属性最强的是N元素,所以酸性最强的是![]() ,故B正确;
,故B正确;
C.气体分子![]() 为
为![]() ,其电子式为:
,其电子式为:![]() ,故C正确;
,故C正确;
D.根据氯气和氢氧化钠溶液反应知,![]() 和NaOH反应生成NaCN、NaOCN、
和NaOH反应生成NaCN、NaOCN、![]() ,反应方程式为:
,反应方程式为:![]() ,故D错误;
,故D错误;
答案选D。


科目:高中化学 来源: 题型:
【题目】洛索洛芬钠可用于类风湿性关节炎、肩周炎等炎症的消炎,其合成路线如图:
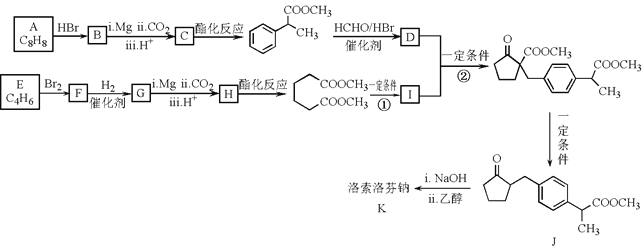
已知:ⅰ.RBr![]() RCOOH
RCOOH
ⅱ.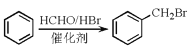
ⅲ. (以上R、R'、R'代表烃基)
(以上R、R'、R'代表烃基)
(1)A属于芳香烃,其结构简式是___。
(2)B的结构简式是___,D中含有的官能团是___。
(3)E属于烯烃。E与Br2反应生成F的化学方程式是___。
(4)反应①的化学方程式是___。
(5)反应②的反应类型是___。
(6)将J和NaOH溶液混合搅拌后,再加入乙醇有大量白色固体K析出,获得纯净固体K的实验操作是___;K的结构简式是___。
(7)以乙烯为起始原料,结合已知信息选用必要的无机试剂合成聚丁二酸乙二醇酯(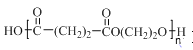 ),写出最多不超过5步的合成路线(用结构简式表
),写出最多不超过5步的合成路线(用结构简式表
示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用0.200 0 mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作如下:
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上;
②固定好滴定管并使滴定管尖嘴处充满液体;
③调节液面至“0”或“0”刻度线以下,并记下读数;
④移取20.00 mL待测液注入洁净的还存有少量蒸馏水的锥形瓶中,并加入3滴酚酞试液;
⑤用标准液滴定至终点,记下滴定管液面读数。
请回答下列问题:
(1)以上步骤有错误的是____。
(2)用标准的NaOH溶液滴定待测的盐酸时,左手握_______(填“酸式”或“碱式”)滴定管的活塞,右手摇动锥形瓶,眼睛注视_______________判断滴定终点的现象是____________________。
(3)若测定结果偏高,其原因可能是_____。
a.配制标准溶液的固体NaOH中混有KOH杂质
b.滴定终点读数时,仰视滴定管的刻度,其他操作正确
c.盛装待测液的锥形瓶用蒸馏水洗过后未用待测液润洗
d.滴定管滴定前无气泡,滴定后有气泡
(4)如图是某次滴定时的滴定管中的液面,其读数为_____mL。
![]()
(5)根据下列数据,请计算待测盐酸的浓度:_________mol·L-1。
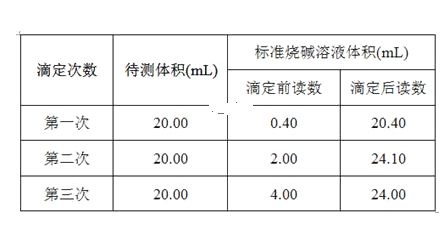
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,某气态烃A的密度是1.25g·L-1,取x L的A在足量的氧气中充分燃烧,生成的混合气体通入到50mLNaOH溶液,随后取此溶液25mL将其稀释至100mL,并向此稀释后的溶液中逐滴加入0.1mol·L-1的HCl溶液,产生的CO2气体体积与所加入的盐酸的体积之间的关系如图所示:
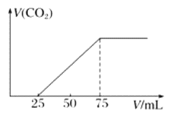
(1)A的摩尔质量为________________。
(2)请计算x的值(写出具体计算过程)。________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,其中X、Y、W、Z为知周期元素,T的单质常温下为液体。下列说法错误的是

A. X、Y的单质均存在同素异形体
B. Y、Z的简单氢化物的稳定性依次递增
C. 工业上电解NaW溶液得W2可使用阴离子交换膜
D. R的单质可用于制造半导体材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是
A.反应MgCl2(l)=Mg(l)+Cl2(g)的ΔH<0、ΔS>0
B.加热Na2CO3溶液,![]() 增大
增大
C.由热化学方程式2CO(g)+O2(g)=2CO2 (g)ΔH=-566 kJ·mol-1可知,CO的燃烧热是566 kJ·mol-1
D.中和等体积、等浓度的醋酸和盐酸,醋酸消耗的NaOH的物质的量小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图象与文字描述正确的是
A.根据图可判断对于“![]() ”:升温,化学反应平衡常数增大
”:升温,化学反应平衡常数增大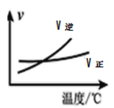
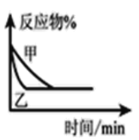
B.图表示压强对可逆反应![]() 的影响且
的影响且![]()
C.图可表示醋酸溶液中通入氨气至过量过程中溶液导电性的变化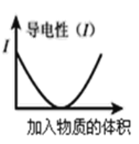
D.根据图,若除去![]() 溶液中的
溶液中的![]() 可采用向溶液中加入适量
可采用向溶液中加入适量![]() 至溶液的pH在4左右即可
至溶液的pH在4左右即可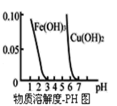
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() △H =akJ/mol ;
△H =akJ/mol ;![]() △H =bkJ/mol。P4具有正四面体结构,PCl5 中 P-Cl 键的键能为cKJ/mol、,PCl3 中 P-Cl 键的键能为1.2cKJ/mol。下列叙述正确的是( )
△H =bkJ/mol。P4具有正四面体结构,PCl5 中 P-Cl 键的键能为cKJ/mol、,PCl3 中 P-Cl 键的键能为1.2cKJ/mol。下列叙述正确的是( )
A.P-P 键的键能大于P-Cl 键的键能
B.可求 ![]() 的反应热 △H
的反应热 △H
C.P-P 键的键能为 ![]()
D.Cl-Cl 键的键能 ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、D、E、F是重要的有机化工原料。烃A的产量是一个国家石油化工发展水平的标志,A的相对分子质量为28。B可用作燃料和溶剂。F为有香味的油状液体。它们之间的转化关系如下图。

(1)A的结构简式是______。反应①属于______(填反应类型)。
(2)B的官能团是______。
(3)反应②的化学方程式是______。
(4)反应④的化学方程式是______。
(5)下列说法不正确的是______(填序号)。
a.A、B均不能被酸性高锰酸钾溶液氧化
b.用饱和Na2CO3溶液能除去F中混有的少量B、E
c.生活中可以用E除去水壶中的水垢
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com