
常温,相应条件下,下列各组离子一定能大量共存的是
| A.c(Al3+)=0.1mol/L的溶液中:Na+、K+、AlO2-、OH- |
| B.无色溶液中:K+、CH3COO-、HCO3-、MnO4- |
C.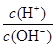 =1×1014的溶液:Ba2+、Na+、SO32-、NO3- =1×1014的溶液:Ba2+、Na+、SO32-、NO3- |
| D.通入足量CO2后所含离子还能大量共存的是:K+、Ca2+、NO3-、Cl- |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:单选题
下列表示对应化学反应的离子方程式正确的是
| A.NO2通入水中:3NO2+H2O=2H++2NO—3+NO |
B.用两个铜电极电解CuSO4溶液: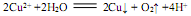 |
| C.SO2通入FeCl3溶液中:SO2+Fe3++2H2O=SO2—4+Fe2++4H+ |
D.过量的CO2通入NaAlO2溶液中: |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
(1)铜粉放入稀H2SO4中,加热后无明显现象,当加入KNO3 后,铜粉质量减小,溶液变蓝,同时气体逸出,该反应的离子方程式为 。(2)在含Cu+的酶的活化中心内,亚硝酸根离子(NO2-)可转化为NO,写出Cu+与亚硝酸根离子在酸性水溶液中反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列离子或分子组中能大量共存,且满足相应要求的是
| 选项 | 离子或分子 | 要求 |
| A | K+、NO3-、Cl-、HS- | c(K+) > c(Cl-) |
| B | Fe3+、MnO4?、SO32-、Cl- | 滴加盐酸立即有气体产生 |
| C | NH4+、Al3+、SO42-、CH3COOH | 滴加NaOH溶液立即有气体产生 |
| D | Na+、HCO3-、Ca2+、I- | 通CO2气体有沉淀产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份100 mL溶液进行如下实验:
(1)第一份:加入AgNO3溶液有沉淀产生;
(2)第二份:加足量NaOH溶液加热后,收集到气体0.04 mol;
(3)第三份:加足量BaCl2溶液后,得干燥沉淀6.27 g,经足量盐酸洗涤、干燥后,沉淀质量为2.33 g。根据上述实验,以下推测正确的是
| A.K+一定存在 |
| B.100 mL溶液中含0.01 mol CO32- |
| C.Cl-一定存在 |
| D.Ba2+一定不存在,Mg2+可能存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列反应离子方程式正确的是
| A.FeCl3溶液刻蚀铜制的印刷电路板:Fe3+ +Cu = Fe2+ + Cu2+ |
| B.硅酸钠溶液和稀硫酸混合:Na2SiO3+2H+ = H2SiO3↓+2Na+ |
| C.Ba(OH)2溶液与稀硫酸反应:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| D.向氯化铝溶液中滴加过量氨水:Al3++3NH3·H2O=Al(OH)3↓+3NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列离子方程式中,正确的是( )
| A.已知电离平衡常数:H2CO3>HClO>HCO3-,向NaClO溶液中通入少量二氧化碳: ClO-+CO2+ H2O =HClO+HCO3- |
| B.硅酸钠溶液与醋酸溶液混合: SiO32-+ 2H+ = H2SiO3↓ |
| C.从酸化的海带灰浸出液中提取碘:2I-+H2O2=I2+2OH- |
| D.FeCl2溶液中滴加NaClO溶液生成红褐色沉淀: |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
能正确表示下列反应的离子方程式是 ( )
| A.Fe3O4溶于足量稀HNO3:Fe3O4+8H+==Fe2++2Fe3++4H2O |
| B.NH4HCO3溶液与足量Ba(OH)2溶液混合:HCO3-+Ba2++OH-==BaCO3↓+H2O |
| C.向澄清石灰水中通入少量CO2:OH-+CO2==HCO3- |
| D.将0.2 mol·L-1的NH4Al(SO4)2溶液与0.3 mol·L-1的Ba(OH)2溶液等体积混合: |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
关于反应的先后顺序,下列评价正确的是
| A.向浓度都为0.1mol·L-1Na2CO3和NaOH混合溶液中通入CO2,NaOH首先反应 |
| B.向NH4Al(SO4)2溶液中滴加少量的NaOH溶液,NH4+首先反应 |
| C.向浓度都为0.1mol·L-1的FeCl3和CuCl2混合溶液中加入铁粉,CuCl2首先反应 |
| D.向0.1mol·L-1的FeCl3溶液中加入质量相同、颗粒大小相同的铁和铜,铜首先反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com