
【题目】水杨酸是一种重要的化工原料,可用于制备阿司匹林、水杨酸钠、水杨酰胺和奥沙拉嗪钠。其中奥沙拉嗪钠是治疗溃疡性结肠炎的常用药物。其合成路线如下所示,回答下列问题:

已知:
I. 
II.
III.NaNO2有强氧化性。
回答下列问题:
(1)有机物A中的官能团名称为________________;奥沙拉嗪钠在核磁共振氢谱中的吸收峰的峰面积之比为__________;
(2)反应②的反应类型为____________;反应③的方程式为______________________;反应④的反应类型为____________;
(3)在溶液中反应⑥所用的试剂X为___________;
(4)设计B→C步骤的目的为______________________;
(5)水杨酸有多种同分异构体,写出符合下列条件的所有同分异构体的结构简式。
a.能发生银镜反应 b.苯环上的一氯代物有两种同分异构体___________________________________________________________________。
【答案】(酚)羟基和酯基 1:1:1:1 取代反应 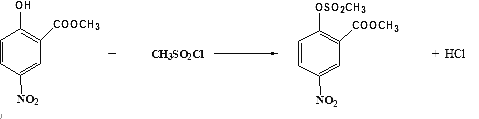 还原反应 CO2 保护酚羟基,防止第⑤步反应时被NaNO2所氧化
还原反应 CO2 保护酚羟基,防止第⑤步反应时被NaNO2所氧化 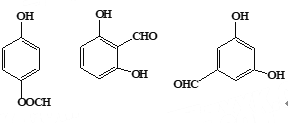
【解析】
根据水杨酸是结构可知,水杨酸分子中含有羧基与羟基,水杨酸与甲醇发生酯化反应生成A,A为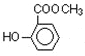 ,观察反应流程,A→B
,观察反应流程,A→B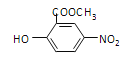 为硝化反应,B→C
为硝化反应,B→C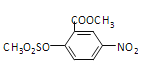 是与酚羟基中的H原子发生取代反应,反应为
是与酚羟基中的H原子发生取代反应,反应为![]() ,C→D为硝基的还原反应,即硝基生成氨基,D
,C→D为硝基的还原反应,即硝基生成氨基,D![]() ,D经过反应⑤得E,E酸化后,反应生成F,
,D经过反应⑤得E,E酸化后,反应生成F,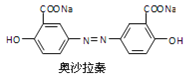 只有酚羟基被酸化,结合有机物的官能团和性质解答该题.
只有酚羟基被酸化,结合有机物的官能团和性质解答该题.
(1)有机物A 中的官能团名称为(酚)羟基和酯基;
中的官能团名称为(酚)羟基和酯基; 结构对称,有4种不同环境的氢,奥沙拉嗪钠在核磁共振氢谱中的吸收峰的峰面积之比为1:1:1:1;
结构对称,有4种不同环境的氢,奥沙拉嗪钠在核磁共振氢谱中的吸收峰的峰面积之比为1:1:1:1;
(2)反应②中A为 ,观察反应流程,A→B
,观察反应流程,A→B 为硝化反应,反应类型为取代反应;B→C
为硝化反应,反应类型为取代反应;B→C 是与酚羟基中的H原子发生取代反应,,反应③的方程式为
是与酚羟基中的H原子发生取代反应,,反应③的方程式为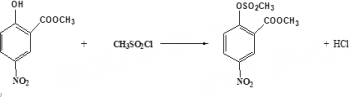 ;C→D为硝基的还原反应,即硝基生成氨基,D
;C→D为硝基的还原反应,即硝基生成氨基,D![]() ,反应④的反应类型为还原反应 ;
,反应④的反应类型为还原反应 ;
(3)D经过反应⑤得E,E酸化后,反应生成F, 只有酚羟基被酸化,X溶液的酸性介于羧基和酚羟基之间,在溶液中反应⑥所用的试剂X为CO2 ;
只有酚羟基被酸化,X溶液的酸性介于羧基和酚羟基之间,在溶液中反应⑥所用的试剂X为CO2 ;
(4)结合奥沙拉秦的结构,生成E的过程中,NaNO2具有强氧化性,若直接将氨基氧化时,同时也会将酚羟基氧化,所以B→C的目的是保护酚羟基,防止第⑤步反应时被NaNO2所氧化;
(5)水杨酸有多种同分异构体,a.能发生银镜反应 ,说明含有醛基或甲酸酯;b.苯环上的一氯代物有两种同分异构体,说明结构对称,符合条件的所有同分异构体的结构简式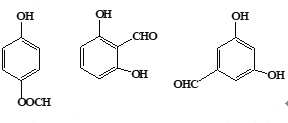 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】常温下,将一定浓度的盐酸和醋酸加水稀释,溶液的导电能力随溶液体积变化的曲线如图所示。下列说法正确的是( )
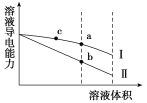
A. 两溶液稀释前的浓度相同
B. a、b、c三点溶液的pH由大到小顺序为a>b>c
C. a点的Kw值比b点的Kw值大
D. a点水电离的n(H+)大于c点水电离的n(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)常温下,0.1 mol·L-1NaHCO3溶液的pH大于8,则溶液中HCO3―、CO32―、H2CO3 三种微粒的浓度由大到小的顺序为:_______________________________。
(2)NaHCO3溶液与硫酸铝溶液混合的离子方程式_______________________________。
(3)Ba(OH)2是一种强电解质,现有25℃、pH=13的Ba(OH)2溶液与某浓度盐酸溶液按体积比(碱与酸之比)1 :9混合后,所得溶液pH=11(假设混合溶液的体积等于混合前两溶液的体积和),该盐酸溶液的pH=____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.用固体烧碱配制480mL 0.1 mol·L-1的NaOH溶液,请回答以下问题:
(1)需称量_______g烧碱固体,它应盛在_____中进行称量。
(2)配制过程中,不需要使用的仪器是(填序号)_____________。
A、托盘天平 B、药匙 C、烧杯 D、胶头滴管 E、玻璃棒 F、1000mL容量瓶 G、500mL容量瓶
(3)若配制0.1 mol·L-1的NaOH溶液的其他操作均正确,但出现下列错误操作,其中将使配制的NaOH溶液浓度偏高的是___________(填序号)。
A.将NaOH溶液转移至容量瓶后,未洗涤烧杯和玻璃棒
B.将烧杯内的NaOH溶液向容量瓶中转移时,因操作不当使部分溅出瓶外
C.定容摇匀后,发现液面低于刻度线,又加水至液面与刻度线相切
D.定容时俯视容量瓶的刻度线
Ⅱ.欲用98% 的浓硫酸(ρ=1.84 g·cm-3 )配制成浓度为0.5 mol·L-1 的稀硫酸480mL。
(1)所需浓硫酸的体积为___mL。
(2)选用的主要仪器有:烧杯、量筒、胶头滴管、玻璃棒和___。
(3)操作正确的顺序为_____(填序号)。
A.用量筒量取浓硫酸 B.反复颠倒摇匀 C.用胶头滴管加水至刻度
D.将配制好的溶液转入试剂瓶中贴上标签 E.稀释浓硫酸 F.将溶液转入容量瓶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)基态Ga原子价电子排布图为________。
(2)经测定发现,N2O5固体由NO2+和NO3-两种离子组成,该固体中N原子杂化类型为___;与NO2+互为等电子体的微粒有_____(写出一种)。
(3)电负性:磷_____硫(填“>”或“<”);第一电离能磷大于硫的原因是________。
(4)NH3分子在独立存在时H-N-H键角为106.7°。如图[Zn(NH3)6]2+离子的部分结构以及H-N-H键角的测量值。解释配合物中H-N-H键角变为109.5°的原因:_______________________________。

(5)已知图中正八面体为[PtCl6]2-离子,白球为K+,立方体晶胞边长为a pm,K2PtCl6的相对式量为M,阿伏加德罗常数的值为NA,其密度为________g·cm3(列出计算式即可)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂用六水合氯化镁和粗石灰制取的氢氧化镁含有少量氢氧化铁杂质,通过如下流程进行提纯精制,获得阻燃剂氢氧化镁。下列说法不正确的是

A. 步骤②中分离操作的名称是过滤,Mg(OH)2可以作阻燃剂是因为它分解需要吸收大量的热
B. 步骤①中的反应式:3Fe(OH)3 +S2O42-+2OH- =3Fe(OH)2 +2SO42-+4H2O
C. 步骤①中保险粉是作还原剂
D. 从步骤② 中可知OH- 和EDTA共存时,Fe2+更易和EDTA结合,生成可溶性化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在电镀车间的含铬酸性废水中,铬的存在形式有Cr(Ⅵ)和Cr(Ⅲ)两种,其中以Cr(Ⅵ)的毒性最大。电解法处理含铬废水如图,铬最终以Cr(OH)3沉淀除去。下列说法正确的是
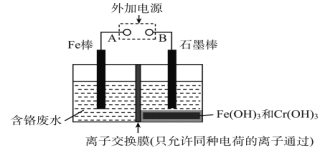
A. Fe为阳极,反应为Fe-2e-=Fe2+
B. 阴极反应为Cr2O72-+7H2O+6e-=2Cr(OH)3↓+8OH-
C. 阳极每转移3mol电子,可处理Cr(Ⅵ)物质的量为1mol
D. 离子交换膜为质子交换膜,只允许H+穿过
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组为了探究一种有机盐 X(仅含四种元素)的组成与性质,设计并完成如下实验:

已知: A为两种常见气体的混合物, B、 C 均为常见物质。
(1)X中除含有氢、氧元素外,还含有的元素为:________________(写元素名称)。
(2)写出 X 受热分解的化学方程式:____________________________________________。
(3)设计实验验证“红棕色固体”中金属阳离子______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烧碱样品中含有少量不与酸作用的可溶性杂质,为了测定其纯度,进行以下滴定操作:
A.用250mL容量瓶等仪器配制成250mL烧碱溶液;
B.用移液管(或碱式滴定管)量取25mL烧碱溶液于锥形瓶中并加几滴甲基橙指示剂;
C.在天平上准确称取烧碱样品W g,在烧杯中加蒸馏水溶解;
D.将物质的量浓度为M molL﹣1的标准HCl溶液装入酸式滴定管,调整液面,记下开始刻度数V1 mL;
E.在锥形瓶下垫一张白纸,滴定到终点,记录终点耗酸体积V2 mL。
回答下列问题:
(1)正确的操作步骤是(填写字母)________→________→________→D→________;
(2)滴定时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视________________;
(3)终点时颜色变化是_____________________;
(4)在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有_____(填字母序号);
A.滴定终点读数时俯视 B.锥形瓶水洗后未干燥
C.酸式滴定管使用前,水洗后未用盐酸润洗 D.酸式滴定管在滴定前有气泡,滴定后气泡消失
(5)该烧碱样品的纯度计算式是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com