
【题目】下列化合物中不能由单质直接化合而制得的是( )
A.FeSB.SO2C.CuSD.FeCl3
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数。下列有关NA的叙述中,正确的是( )
A. 1 mol 任何物质所含的微粒数均为NA
B. 14 g氮气所含的N原子数为NA
C. 标准状况下,22.4 L水所含的H2O分子数为NA
D. 在钠与氧气的反应中,1 mol钠失去电子的数目为2 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化锰是化学工业中常用的氧化剂和有机合成中的催化剂,其主要制备方法是碳酸锰热分解,反应原理为2MnCO3+O2═2MnO2+2CO2 . 经研究发现该反应过程为①MnCO3═MnO+CO2 ②2MnO+O2═2MnO2 .
回答下列问题:
(1)某温度下该平衡体系的压强为P,CO2、O2的物质的量分别为n1和n2 , 用平衡分压代替平衡浓度,碳酸锰热分解反应的平衡常数K=(分压=总压×物质的量分数);K与反应①、②的平衡常数K1、K2的关系为 .
(2)反应②在低温下能自发进行,则其△H0(填“>”、“<”或“=”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A为淡黄色固体,T、R为两种常见的用途很广的金属单质,D是具有磁性的黑色晶体,C是无色无味的气体,H是白色沉淀,W溶液中加入KSCN出现血红色。
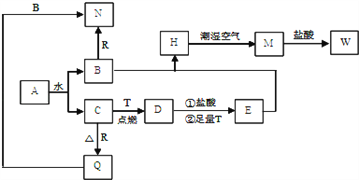
(1)写出下列物质的化学式:D______ N_______
(2)B与E混和得到H并在潮湿空气中变成M的过程中,可能观察到的现象:_______; H在潮湿空气中变成M的过程中发生的化学方程式为:___________________。
(3)按要求写方程式: B和R反应生成N的离子方程式:______________________。M→W的离子方程式:____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质的量浓度表述正确的是( )
A.0.3 mol?L﹣1的Na2SO4溶液中含有的Na+和SO ![]() 的总物质的量为0.9 mol
的总物质的量为0.9 mol
B.当1 L水吸收22.4 L氨气时所得氨水的浓度不是1 mol?L﹣1 , 只有当22.4 L氨气溶于水制得1 L氨水时,其浓度才是1 mol?L﹣1
C.在K2SO4和NaCl的中性混合水溶液中,如果Na+和SO42﹣的物质的量相等,则K+和Cl﹣的物质的量浓度一定相同
D.10℃时,0.35 mol?L﹣1的KCl饱和溶液100 mL蒸发掉5 g水,冷却到10℃时,其体积小于100 mL,它的物质的量浓度仍为0.35 mol?L﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业中采用适当的催化剂利用反应CO(g)+2H2(g)═CH3OH(g)来制取甲醇.
维持体系的压强一定,温度为T时,在体积为2.0L的封闭容器内充入0.6mol CO和0,.4mol H2 , 达到平衡时含有0.15mol CH3OH(g),则该反应平衡常数K=(保留两位小数),此时向容器中再通入0.7mol CO气体,则此平衡将(填“正向”、“不”或“逆向”)移动.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学源于生活,在生产生活中,我们会遇到各种各样的化学反应。
(1)今有铁片、铜片, FeCl2 溶液 、 FeCl3 溶液、 CuSO4溶液, 设计实验证明 Fe3+的氧化性比 Cu2+强, 写出相应的化学方程式______________;
(2)野外作业中用于焊接铁轨,该反应的化学方程式为______________;
(3)将一个铝制易拉罐充满 CO2气体,然后往罐内注入足量的 NaOH 溶液,立即密封罐口,过一段时间后,罐壁内凹而瘪,再过一段时间后又重新鼓起。 试用离子方程式解释易拉罐又重新鼓起的原因______________;
(4)用小苏打片(NaHCO3)治疗胃酸(盐酸)过多的离子方程式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中能证明次氯酸是一种弱酸的是
A.次氯酸不稳定,易分解
B.次氯酸是一种强氧化剂
C.次氯酸钙能与碳酸作用生成碳酸钙和次氯酸
D.次氯酸能使染料和有机色质褪色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com