
| A. | 改用98%的浓硫酸 | B. | 降温 | C. | 加入CuSO4固体 | D. | 加水 |
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:选择题
| A. | 电解饱和食盐水可以得到金属钠 | |
| B. | 电解法精炼粗铜,粗铜作阳极 | |
| C. | 在铁制品上镀上一定厚度的锌层,可用锌做阴极,铁制品做阳极 | |
| D. | 用惰性电极电解Na2SO4溶液,一段时间后再加入硫酸,能使溶液恢复到电解前的状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④⑤⑥ | B. | ②③⑤⑥ | C. | ②④⑤⑥ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 大量燃烧化石燃料是造成雾霾天气的原因之一 | |
| B. | 从海水中提取氯化钠、溴、碘不一定都要通过化学反应才能实现 | |
| C. | 燃料脱硫和减少汽车尾气排放都能减少酸雨的产生 | |
| D. | 用高纯度的硅来制备光导纤维 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
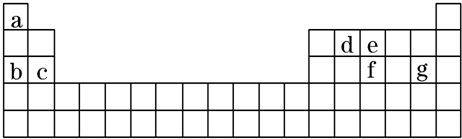
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由溴乙烷制乙醇;由乙烯与水反应制乙醇 | |
| B. | 乙烯使溴的四氯化碳褪色,甲苯使KMnO4酸性溶液褪色 | |
| C. | 苯与浓硝酸、浓硫酸混合共热制取硝基苯; 苯与液溴在催化剂存下制取溴苯 | |
| D. | 1-氯丙烷与NaOH的乙醇溶液加热反应;l-氯丙烷与NaOH的水溶液加热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,22.4 L NH3中含有共价键的数目为3NA | |
| B. | 50mL18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA | |
| C. | 标准状况下,11.2 L CCl4所含的分子数目为0.5NA | |
| D. | 若由CO2和O2组成的混合物中共有NA个分子,则其中的氧原子数为2 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
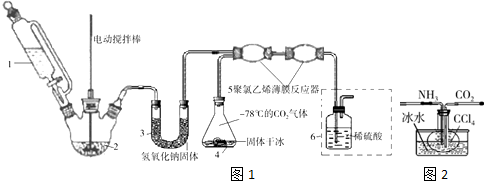
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com