
【题目】将铁粉、铜粉、FeCl3溶液和CuCl2溶液混合于某容器中充分反应(假定容器不参与反应)。试判断下列情况下,容器中存在的金属离子和金属单质。
(1)若铁粉有剩余,则容器中不可能有的离子是________,铜单质______(填“一定”或“可能”)存在。
(2)若CuCl2有剩余,则容器中还可能有的离子为________,铜单质______(填“一定”或“可能”)存在。
(3)若FeCl3和CuCl2都有剩余,则容器中不可能有的单质是______,Fe2+_____(填“一定”或“可能”)存在。
(4)将6g铁粉加入200mLFe2(SO4)3和CuSO4的混合溶液中,充分反应得到200mL 0.5mol/LFeSO4溶液和5.2g固体沉淀物,则原Fe2(SO4)3和CuSO4的混合溶液中Fe2(SO4)3的物质的量浓度为________。
【答案】 Fe3+、Cu2+ 一定 Fe3+ 可能 Fe、Cu 一定 0.1mol/L
【解析】氧化性:FeCl3>CuCl2>FeCl2,还原性Fe>Cu,多种氧化剂、还原剂混合时,强氧化剂先与强还原剂反应。
(1)若铁有剩余,则发生两个反应Fe+2FeCl3=3FeCl2,Fe+CuCl2=Cu+FeCl2,且Fe3+、Cu2+反应完全,Cu还没有参加反应。故溶液中不可能有的离子为:Fe3+、Cu2+;Cu一定存在;
故答案为:Fe3+、Cu2+;一定;
(2)若CuCl2有剩余,由于Fe单质能与CuCl2反应,CuCl2有剩余则说明铁少量,容器中可能还含有Fe3+。此时反应程度分两种情况,第一种:FeCl3未反应完全,CuCl2还未反应,此时不存在Cu单质;第二种:FeCl3反应完全,CuCl2部分反应,此时存在Cu单质。所以,若CuCl2有剩余,溶液中可能存在Fe3+,铜单质可能存在。
故答案为:Fe3+;可能;
(3)若FeCl3和CuCl2都有剩余,则Fe、Cu都已反应完全,发生反应Fe+2FeCl3=3FeCl2,Cu+2FeCl3=CuCl2+2FeCl2,所以容器中一定不含的单质为Fe、Cu;一定存在Fe2+。
故答案为:Fe、Cu;一定;
(4)氧化性:Fe3+>Cu2+,加入Fe单质,Fe先Fe3+反应:2Fe3++Fe=3Fe2+;再与Cu2+反应:Cu2++Fe=Fe2++Cu。反应后,得到200mL 0.5mol/LFeSO4溶液,n(Fe2+)=0.5mol/L×0.2L=0.1mol。m(Fe2+)=5.6g<6g,说明加入的6g铁粉没有反应完,而Fe3+和Cu2+反应完全。
设原混合溶液中含Fe2(SO4)3的物质的量为x mol,CuSO4的物质的量为ymol。
Fe + Fe2(SO4)3= 3FeSO4
x mol x mol 3x mol
Fe + CuSO4 = FeSO4+ Cu
y mol y mol y mol y mol
所以,反应后溶液中n(FeSO4)= 0.5mol/L×0.2L=0.1mol =3x+y;
固体沉淀的质量等于加入的6g铁,减去消耗的铁的质量,加上生成的铜的质量。
m(固体)=6-(x+y)×56+64y=5.2 g
解得x=0.02,即原混合溶液中含Fe2(SO4)3的物质的量为0.02 mol.
所以Fe2(SO4)3的物质的量浓度为![]() =0.1mol/L。
=0.1mol/L。
故答案为:0.1mol/L.


 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:
【题目】火星探测器发回的信息表明,火星上存在针铁矿〔Goethite,化学式:FeO(OH)〕和黄钾铁矾(Jarosite),从而证明火星表面曾经存在过水.这一发现被《人民日报》等媒体评为2004世界十大新闻之首.已知两种矿物中铁的价态相同,则黄钾铁矾〔化学式记为:KFe3(SO4)2(OH)n〕中n值为
A. 4 B. 5 C. 6 D. 7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按如图所示装置进行实验,将液体A逐滴加入到固体B中,下列叙述不正确的是
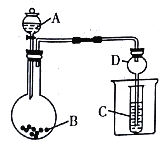
A. 若A为浓盐酸,B为KMnO4,C中盛品红溶液,则C中溶液褪色
B. 若A为醋酸,B为贝壳,C中盛Na2SiO3 溶液,则C中溶液变浑浊
C. 若A为浓氨水,B为生石灰,两者混合后产生NH3,C中盛AlCl3溶液,则C中先产生白色沉淀后沉淀溶解
D. 仪器D可以起到防止溶液倒吸的作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 丙酮是一种常用的有机溶剂,可与水以任意体积比互溶,密度小于1 g/mL,沸点约55 ℃,分离水和丙酮时最合理的方法是( )
A.蒸发B.蒸馏C.过滤D.分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下甲醇与一氧化碳反应可以合成乙酸.通常状况下,将a mol/L的醋酸与b mol/LBa(OH)2溶液等体积混合,反应平衡时,2c(Ba2+)=c(CH3COO﹣),用含a和b.的代数式表示该混合溶液中醋酸的电离常数为: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校研究性学习小组用已部分生锈(Fe2O3)的废铁屑,制作印刷电路板的腐蚀剂,即FeCl3溶液。实验操作过程如下:
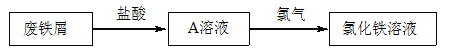
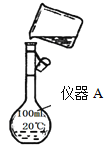
根据要求回答问题:
(1)用浓盐酸配制250mL 0.2molL-1稀盐酸,右图是某同学转移溶液的示意图,写出仪器 A的名称: 。
(2)图中有两处错误分别是 , 。
(3)废铁屑用盐酸处理后,还含有不溶性杂质,为获取澄清的A溶液,进行物质分离的操作名称是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法正确的是( )
A.聚氯乙烯分子中含碳碳双键B.以淀粉为原料可制取乙酸乙酯
C.油脂的皂化反应属于加成反应D.包装用材料聚乙烯和聚氯乙烯都属于烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一定量的K2CO3溶液中缓慢地滴加稀盐酸,并不断搅拌。随着盐酸的加入,溶液中离子数目也相应地发生变化。如图所示,四条曲线与溶液中的离子数目的对应关系,完全正确的是( )

A. a:K+; b:HCO3—;c:CO32—;d:Cl—
B. a:K+; b:CO32—;c:HCO3—;d:Cl—
C. a:K+; b:CO32—;c:Cl—;d:HCO3—
D. a:K+; b:HCO3—;c:Cl—;d:CO32—
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com