
分析 ①测得溶液A、C、E呈碱性,三种溶液为碱液或水解呈碱性的溶液,且碱性为A>E>C,则A为碱,溶液中含有大量的OH-离子,OH-离子与Ag+,Ca2+,Fe2+,Al3+等离子不能大量共存,故A只能为Ba(OH)2,根据越弱越水解,E应为碳酸盐,根据离子共存,只能为K2CO3,C为醋酸盐;
②向B溶液中滴加稀氨水,先出现沉淀,继续滴加氨水,沉淀消失,则B中含有银离子,应为硝酸银溶液,加入氨水发生的反应为AgNO3+NH3•H2O=AgOH↓+NH4NO3;
AgOH+2NH3•H2O=Ag(NH3)2OH+2H2O;
③向D溶液中滴加Ba(NO3)2溶液,无明显现象,说明D中不含SO42-离子;
④向F溶液中滴加氨水,生成白色絮状沉淀,沉淀迅速变成灰绿色,最后变成红褐色,说明F中含有Fe2+离子;
综上分析可知,A为Ba(OH)2,B为AgNO3,C为Ca(CH3COO)2,D为AlCl3,E为K2CO3,F为FeSO4,以此解答该题.
解答 解:①测得溶液A、C、E呈碱性,三种溶液为碱液或水解呈碱性的溶液,且碱性为A>E>C,则A为碱,溶液中含有大量的OH-离子,OH-离子与Ag+,Ca2+,Fe2+,Al3+等离子不能大量共存,故A只能为Ba(OH)2,根据越弱越水解,E应为碳酸盐,根据离子共存,只能为K2CO3,C为醋酸盐;
②向B溶液中滴加稀氨水,先出现沉淀,继续滴加氨水,沉淀消失,则B中含有银离子,应为硝酸银溶液,加入氨水发生的反应为AgNO3+NH3•H2O=AgOH↓+NH4NO3; AgOH+2NH3•H2O=Ag(NH3)2OH+2H2O;
③向D溶液中滴加Ba(NO3)2溶液,无明显现象,说明D中不含SO42-离子;
④向F溶液中滴加氨水,生成白色絮状沉淀,沉淀迅速变成灰绿色,最后变成红褐色,说明F中含有Fe2+离子;
综上分析可知,A为Ba(OH)2,B为AgNO3,C为Ca(CH3COO)2,D为AlCl3,E为K2CO3,F为FeSO4,
(1)在硝酸银溶液中加入氨水生成氢氧化银沉淀,加入过量氨水后生成银氨络离子,反应的化学方程式为AgNO3+NH3•H2O=AgOH↓+NH4NO3; AgOH+2NH3•H2O=Ag(NH3)2OH+2H2O,
故答案为:AgNO3+NH3•H2O=AgOH↓+NH4NO3; AgOH+2NH3•H2O=Ag(NH3)2OH+2H2O;
(2)E应为碳酸盐,六种阳离子中可以与碳酸根形成可溶性盐的只有钾离子,故E为K2CO3,
故答案为:碳酸钾;由①中碱性强弱的顺序可知,E是碳酸盐,六种阳离子中可以与碳酸根形成可溶性盐的只有钾离子,所以E是碳酸钾;
(3)根据以上分析可知A为Ba(OH)2,B为AgNO3,C为Ca(CH3COO)2,D为AlCl3,E为K2CO3,F为FeSO4,
故答案为:Ba(OH)2;Ca(CH3COO)2;AlCl3;FeSO4;
(4)氢氧化亚铁在溶液中被氧气氧化成氢氧化铁,反应的化学方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:4Fe(OH)2+O2+2H2O=4Fe(OH)3.
点评 本题考查无机物的推断,侧重考查物质的鉴别和检验,为高频考点,题目难度中等,把握物质之间的反应、物质的性质为解答的关键,侧重分析、计算及推断能力的考查,注意离子共存及电荷守恒的应用.


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16gCH4含有共价键数为4NA | |
| B. | 1mol甲基中含有电子数为10NA | |
| C. | 7.1g氯气与足量NaOH溶液反应转移的电子数为0.2NA | |
| D. | 1molC3H8分子中共价键总数为8NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | R有多种氧化物 | B. | R的气态氢化物很稳定 | ||
| C. | R的非金属性比Cl的非金属性强 | D. | R的最高价氧化物的水化物是强碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 微粒 | ClO${\;}_{2}^{-}$ | ClO${\;}_{3}^{-}$ | ClO${\;}_{4}^{-}$ |
| 立体结构 | V形 | 三角锥形 | 正四面体 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
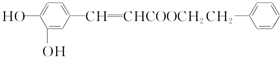
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 氟 | 氯 | 溴 | 碘 | 铍 | |
| 第一电离能(kJ/mol) | 1681 | 1251 | 1140 | 1008 | 900 |
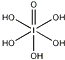 )和HIO4,前者为五元酸,后者为一元酸.请比较二者酸性强弱:H5IO6<HIO4(填“>”、“<”或“=”)
)和HIO4,前者为五元酸,后者为一元酸.请比较二者酸性强弱:H5IO6<HIO4(填“>”、“<”或“=”)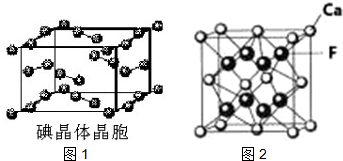
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
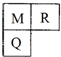 M、R、Q三种短周期元素在元素周期表中的相对位置如图所示,已知M、Q可分别与R形成化合物X和Y,M与R的质子数之和为Q的质子数,下列说法中,正确的是( )
M、R、Q三种短周期元素在元素周期表中的相对位置如图所示,已知M、Q可分别与R形成化合物X和Y,M与R的质子数之和为Q的质子数,下列说法中,正确的是( )| A. | ①②③④ | B. | ①②④ | C. | ②③ | D. | ①② |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com