
某溶液中只可能含有下列离子中的几种(不考虑溶液中含的较少的H+和OH-):Na+、NH 、SO
、SO 、CO
、CO 、NO
、NO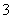 。取200 mL该溶液,分为等体积的两份分别做下列实验。实验1:第一份加入足量的烧碱并加热,产生的气体在标准状况下为224 mL。实验2:第二份先加入足量的盐酸,无现象,再加入足量的BaCl2溶液,得固体2.33 g。下列说法正确的是( )
。取200 mL该溶液,分为等体积的两份分别做下列实验。实验1:第一份加入足量的烧碱并加热,产生的气体在标准状况下为224 mL。实验2:第二份先加入足量的盐酸,无现象,再加入足量的BaCl2溶液,得固体2.33 g。下列说法正确的是( )
A.该溶液中可能含有Na+
B.该溶液中肯定含有NH 、SO
、SO 、CO
、CO 、NO
、NO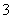
C.该溶液中一定不含NO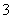
D.该溶液中一定含有Na+,且c(Na+)≥0.1 mol·L-1
 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
如图所示,集气瓶内充满某混合气体,置于光亮处,将滴管内的水挤入集气瓶后,烧杯中的水会进入集气瓶,集气瓶内气体是
①CO、O2 ②Cl2、CH4 ③NO2、O2 ④N2、H2
A.①② B.②④ C.③④ D.②③

查看答案和解析>>
科目:高中化学 来源: 题型:
稀薄燃烧是指汽油在较大空/燃比(空气与燃油气的体积比)条件下的燃烧。随着全球能源危机的加剧,稀薄燃烧技术的研究受到了人们的重视,但稀薄燃烧时,常用的汽车尾气净化装置不能有效地将NOx转化为N2。不同空/燃比时汽车尾气中主要污染物的含量变化如图所示。

⑴稀薄燃烧技术 除能节约能源外,还具有的优点是_______________(填一项)。排放到大气中的NOx会导致酸雨、___________等环境问题(填一项)。
除能节约能源外,还具有的优点是_______________(填一项)。排放到大气中的NOx会导致酸雨、___________等环境问题(填一项)。
⑵某校化学研究性学习小组的同学在技术人员的指导下,按下列流程探究不同 催化剂对NH3还原NO反应的催化性能。
催化剂对NH3还原NO反应的催化性能。

若控制其他实验条件均相同,在催化反应器中装载不同的催化剂,将经催化反应后的混合气体通入滴有酚酞的稀硫酸溶液(溶液的体积、浓度均相同)。为比较不同催化剂的催化性能,需要测量并记录的数据是____________________。
⑶若某一催化剂能同时催化NH3等还原性气体与NOx的反应。将该催化剂分别用于催化还原含等物质的量NOx的两种气体:①纯NO气体,②汽车尾气。消耗NH3的物质的量较多的可能是_____(填字母),原因是______________________________。
A.① B.② C.都有可能
查看答案和解析>>
科目:高中化学 来源: 题型:
研究性学习小组进行SO2的制备及性质探究实验。
⑴ 根据反应Na2SO3(固) + H2SO4(浓) == Na2SO4 + SO2↑+H2O,制备SO2气体。
用下列简图,在答题卡的方框中画出制备并收集SO2的实验装置(含试剂)示意图。

② 实验过程中,使用分液漏斗滴加浓硫酸的操作是__________________
__________。
⑵ 将SO2气体分别通入下列溶液中:
① 品红溶液,现象是__________________________________________________。
② 溴水溶液,现象是_________________________________________________。
③ 硫化钠溶液,现象是________________________________________________。
⑶ 有一小组在实验中发现,SO2氧化产生缓慢,以致后续实验现象很不明显,但又不存在气密性问题。请你推测可能的原因并说明相应的验证方法(可以不填满)
① 原因_______________________,验证方法________________________________。
② 原因_______________________,验证方法________________________________。
③ 原因_______________________,验证方法________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各溶液中一定能大量共存的离子组是( )
A.加入铝粉有氢气生成的溶液中:Mg2+、Cu2+、SO 、K+
、K+
B.使pH试纸呈红色的溶液中:Fe2+、I-、NO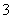 、Cl-
、Cl-
C.常温下,c(H+)=10-14mol/L的溶液中:Na+、AlO 、S2-、SO
、S2-、SO
D.常温下,水电离出的c(H+)与c(OH-)乘积为10-28的溶液中:K+、Na+、HCO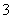 、Ca2+
、Ca2+
查看答案和解析>>
科目:高中化学 来源: 题型:
将足量的铜屑加入到100 mL浓度均为2 mol·L-1的HNO3和H2SO4的混合溶液中,充分反应后,转移电子的物质的量为 ( )
A.0.6 mol B.0.8 mol C.0.45 mol D.0.4 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
NA表示阿伏加德罗常数的值,下列说法正确的是( )
A. 标准状况下,22.4L SO3中所含有分子数为NA
B. 常温下,28 g 乙烯和丙烯的混合物中所含化学键一定为6NA
C. 在O2参与的反应中,1 mol O2作氧化剂时得到的电子数一定为4NA
D. 1 L 1mol/L NH4NO3溶液中氮原子数目小于2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
利用化学原理可以对工厂排放的废水、废渣等进行有效检测。某工厂对制铬工业污泥中Cr(Ⅲ)回收与再利用工艺如下(硫酸浸液中金属离子主要是Cr3+,其次是Fe3+, Fe2+, Al3+, Ca2+, Mg2+)
常温下部分阳离子的氢氧化物形成沉淀时溶液的pH见下表:
| 阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Ca2+ | Cr3+ |
| 开始沉淀时的pH | 1.9 | 7.0 | 9.6 | 4.2 | 9.7 | — |
| 沉淀完全时的pH | 3.2 | 9.0 | 11.1 | 8.0 | 11.7 | 9.0(>9.0溶解) |
(1) 酸浸时,为了提高浸取率可采取的措施是 (至少一条)
(2) 调pH=4.0是为了除去 (填Fe3+, Al3+, Ca2+, Mg2+)
(3) 钠离子交换树脂的原理为Mn+ + n NaR → MRn +nNa+,
被交换的杂质离子是 (填Fe3+, Al3+, Ca2+, Mg2+)
(4) 试配平下列氧化还原反应方程式:
Na2Cr2O7 + SO2 + H2O = Cr(OH)(H2O)5SO4 + Na2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
(1) S2-中的质子数是________,中子数是________,核外电子数是________,质量数是________。
S2-中的质子数是________,中子数是________,核外电子数是________,质量数是________。
(2)Fe、Fe2+、Fe3+是________元素的三种粒子,它们的________数相同,它们所带的________数不相同。
(3)由1H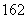 O与2H
O与2H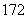 O所代表的物质中,共有________种元素,______种原子,互为同位素的原子有________。
O所代表的物质中,共有________种元素,______种原子,互为同位素的原子有________。
(4)已知元素X、Y的核电荷数分别为a和b,它们的离子Xm+和Yn-核外电子排布相同,则a、b、m、n之间的关系是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com