
| A. | 纤维素、蛋白质、油脂都是高分子化合物 | |
| B. | 糖类、蛋白质、油脂都是由C、H、O三种元素组成的 | |
| C. | 油脂有油和脂肪之分,但都属于酯 | |
| D. | 只用淀粉溶液就可鉴别市售食盐是否为加碘盐 |
分析 A.相对分子质量在10000以上的化合物为高分子化合物;
B.蛋白质除了含有C、H、O以上外还含有N等元素;
C.油脂包含油和脂肪;
D.碘遇淀粉试液变蓝色,但遇碘酸钾不反应.
解答 解:A.相对分子质量在10000以上的化合物为高分子化合物,油脂的相对分子质量较小,不属于高分子化合物,故A错误;
B.蛋白质除了含有C、H、O以上外还含有N等元素,糖类和油脂都含有C、H、O元素,故B错误;
C.油脂包含油和脂肪,但都属于酯,故C正确;
D.碘遇淀粉试液变蓝色,但遇碘酸钾不反应,食盐中加的碘为碘酸钾,和淀粉不反应,所以不能用淀粉鉴别市售食盐是否为加碘盐,故D错误;
故选C.
点评 本题考查较综合,涉及物质鉴别、物质分类、物质组成等知识点,侧重考查学生分析判断能力,易错选项是D,注意:加碘盐加的是碘酸钾而不是碘单质.


科目:高中化学 来源:2016-2017学年甘肃省高二上10月月考化学试卷(解析版) 题型:选择题
在0.lmol/L的CH3COOH溶液中存在如下电离平衡:
CH3COOH CH3COO-+H+对于该平衡,下列叙述正确的是( )
CH3COO-+H+对于该平衡,下列叙述正确的是( )
A.加入少量NaOH固体,平衡向正反应方向移动
B.加水,反应速率增大,平衡向逆反应方向移动
C.滴加少量0.l mol / L HCl溶液,溶液中c?H+?减少
D.加入少量CH3COONa固体,平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
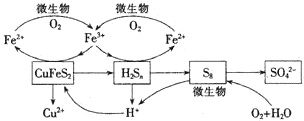 我国产铜主要取自黄铜矿(CuFeS2),随着矿石品味的降低和环保要求的提高,湿法炼铜的优势日益突出.该工艺的核心是黄铜矿的浸出,目前主要有氧化浸出、配位浸出和生物浸出三种方法.
我国产铜主要取自黄铜矿(CuFeS2),随着矿石品味的降低和环保要求的提高,湿法炼铜的优势日益突出.该工艺的核心是黄铜矿的浸出,目前主要有氧化浸出、配位浸出和生物浸出三种方法.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 进入地下矿井中可用火把照明 | |
| B. | 实验时将水倒入浓硫酸中配置稀硫酸 | |
| C. | 节日期间,在开阔的广场燃放烟花爆竹 | |
| D. | 在实验室可以用手接触药品,用嘴吹灭酒精灯 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 道尔顿提出原子学说,门捷列夫发现元素周期律 | |
| B. | 化学研究的主要目的就是认识分子 | |
| C. | 研究物质的性质,常常运用观察、实验、分类、比较等方法 | |
| D. | 化学家可以在微观层面上操纵分子和原子,组装分子材料、分子器件和分子机器 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 如图为实验室某浓硫酸试剂瓶上的标签,试根据有关数据回答下列问题:
如图为实验室某浓硫酸试剂瓶上的标签,试根据有关数据回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com