
(14分)纳米碳酸钙应用非常广泛。实验室中利用下图所示装置(部分夹持装置已略去),向饱和CaCl2溶液中通入NH3和CO2可制得纳米碳酸钙。

供选择的药品:①石灰石 ②氯化铵 ③氢氧化钙 ④饱和氯化钙溶液
⑤浓硫酸 ⑥6 mol·L-1盐酸 ⑦饱和食盐水 ⑧饱和NaHCO3溶液
(1)装置A中,仪器a的名称是 ,仪器b中发生反应的离子方程式为 。装置D的试管中发生反应的化学方程式为 。装置B中盛放的溶液是 (填药品序号)。
(2)设计一个简单的实验方案,判断所得碳酸钙颗粒是否为纳米级。
。(简述实验的步骤、现象和结论)
(3)通人适量气体后,C装置中物质恰好完全反应,过滤,所得滤液显 (填“酸”、“碱”、“中”之一)性,原因是 (用离子方程式表示)。
(4)上述装置存在一处缺陷,该缺陷为 。
(14分)
(1)分液漏斗(1分) CaCO3+2H+===Ca2++H2O+CO2↑(2分)
2NH4Cl+Ca(OH)2 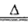 CaCl2+2NH3↑+2H2O(2分) ⑧(1分)
CaCl2+2NH3↑+2H2O(2分) ⑧(1分)
(2)将少量碳酸钙加水充分搅拌,用一束可见光照射,观察是否发生丁达尔现象,若有
丁达尔现象则为纳米级,若没有丁达尔现象则不是纳米级。(3分)
(3)酸(1分) NH4++H2O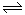 NH3·H2O+H+(2分)
NH3·H2O+H+(2分)
(4)缺少尾气处理装置
【解析】
试题分析:(1)装置A中,仪器a的名称是分液漏斗;仪器b中发生石灰石与盐酸的反应,产生二氧化碳气体,离子方程式为CaCO3+2H+===Ca2++H2O+CO2↑;装置D为产生氨气,用氯化铵与氢氧化钙在加热条件下反应,化学方程式为2NH4Cl+Ca(OH)2 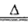 CaCl2+2NH3↑+2H2O;因为制取二氧化碳用的是盐酸,盐酸易挥发,所以产生的二氧化碳气体中可能含有HCl,应除去,选择饱和的碳酸氢钠溶液,所以装置B中盛放的溶液是⑧;
CaCl2+2NH3↑+2H2O;因为制取二氧化碳用的是盐酸,盐酸易挥发,所以产生的二氧化碳气体中可能含有HCl,应除去,选择饱和的碳酸氢钠溶液,所以装置B中盛放的溶液是⑧;
(2)纳米级颗粒属于胶体的分散系,则会发生丁达尔现象,所以可通过丁达尔现象来检验制得的碳酸钙颗粒是否是纳米级。操作如下:将少量碳酸钙加水充分搅拌,用一束可见光照射,观察是否发生丁达尔现象,若有丁达尔现象则为纳米级,若没有丁达尔现象则不是纳米级。
(3)氨气、二氧化碳、饱和氯化钙反应后生成碳酸钙和氯化铵,所以滤液为氯化铵溶液,铵根离子水解使溶液呈酸性;铵根离子的水解离子方程式为NH4++H2O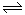 NH3·H2O+H+;
NH3·H2O+H+;
(4)若气体不能恰好完全反应,则会逸出,造成污染,所以缺少尾气处理装置。
考点:考查物质的制备实验,实验方案的设计与评价,离子方程式的书写


 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源:2014-2015广东省汕头市高一上学期10月月考化学试卷(解析版) 题型:选择题
下列每组中的两种物质相互反应时,无论谁过量,都可以用同一离子方程式表示的是
A.碳酸钠溶液和盐酸 B.明矾溶液和烧碱溶液
C.石灰水和二氧化碳 D.硫酸溶液和氢氧化钡溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015学年重庆市七校高三上学期期末联考理综化学试卷 (解析版) 题型:填空题
(共16分)食盐是日常生活的必需品,也是重要的化工原料。
(1)粗盐常含有少量K+、Ca2+、Mg2+、Fe3+、SO42-等杂质离子,实验室提纯NaCl的流程如下:
提供的试剂:饱和Na2CO3溶液 饱和K2CO3溶液 NaOH溶液 BaCl2溶液 Ba(NO3)2溶液 75%乙醇 四氯化碳
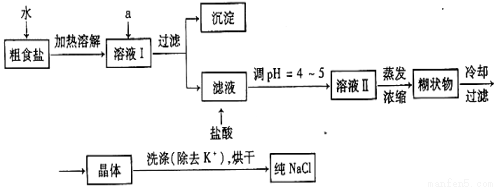
①欲除去溶液Ⅰ中的Ca2+、Mg2+、Fe3+、SO42-离子,选出a所代表的试剂,按滴加顺序依次为__________________(填化学式);滤液中滴加盐酸调PH=4-5的目的是
②选用75%乙醇洗涤除去NaCl晶体表面附带的少量 KCl,检验NaCl是否洗净的方法是
(2)用提纯的NaCl配制480mL 0.40 mol·L-1NaCl溶液,需要称取NaCl的质量为 g,所用仪器除药匙、玻璃棒、烧杯外还有_____________(填仪器名称);
(3)电解饱和食盐水的装置如图所示,
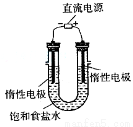
若收集的H2为2L,则同样条件下收集的Cl2 _____(填“>”、“=”或“<”)2L, 写出电解饱和食盐水的离子方程式
查看答案和解析>>
科目:高中化学 来源:2014-2015学年重庆市七校高三上学期期末联考理综化学试卷 (解析版) 题型:选择题
设NA表示阿伏加德罗常数,下列说法正确的是
A.标准状况下,22.4 L水所含电子数约为10 NA
B.25℃时,pH=13的1 L Ca(OH)2溶液中含有OH-数目约为0.2 NA
C.0.5 mol NH4HSO4晶体中,含有H+数目约为0.5 NA
D.常温常压下,3.2 g O2和O3混合气体含有0.2 NA个氧原子
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省协作体高三上学期第二次月考化学试卷(解析版) 题型:选择题
下图两个装置中,液体体积均为200 mL,开始工作前电解质溶液的浓度均为0.5 mol/L,工作一段时间后,测得有0.02 mol电子通过,若忽略溶液体积的变化

下列叙述正确的是
A.产生气体体积 ①=②
B.①中阴极质量增加,②中正极质量减小
C.溶液的pH变化:①减小,②增大
D.电极反应式:①中阳极:4OH- - 4e- = 2H2O+O2↑ ②中负极:2H++2e-=H2↑
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省宁波市高三一月化学试卷(解析版) 题型:推断题
(9分)甲、丙、丁是由短周期元素组成的物质,它们之间存在如下转化关系。
甲 + H2O → 丙 + 丁
(1)转化关系中所涉及的反应为非氧化还原反应。
①若甲是一种钠盐,丁为两性氢氧化物,则甲的化学式为 ,丁的酸式电离方程式为 。
②若甲是由N和Cl元素组成的化合物,其分子结构模型如图所示,丙具有漂白性。则甲中Cl元素的化合价是 ,丁与H2O有相同的电子总数,则丁的电子式为

(2)转化关系中所涉及的反应为氧化还原反应。
①若甲和丙是同主族元素组成的单质,且组成甲的元素位于第三周期,此反应的离子方程式是 。
②若丙和丁都可在一定条件下还原CuO,此反应的化学方程式是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省宁波市高三一月化学试卷(解析版) 题型:选择题
下列表示物质结构的化学用语或模型图正确的是
A. H2O2的电子式:
B.O2-的结构示意图:
C.二氧化硅的分子式:SiO2
D.质子数为8,中子数为10的氧原子:
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省益阳市高三上学期期中考试化学试卷(解析版) 题型:选择题
某溶液中含有AlO2-、SO32-、SO42-、Na+,向其中加入Na2O2后,溶液中浓度基本保持不变的离子是
A.SO32- B.Na+ C.AlO2- D.SO42-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com