
【题目】下列各组数据中,前者刚好是后者两倍的是
A.64g二氧化硫中的氧原子数和标准状况下22.4L二氧化碳中的氧原子数
B.200mL1mol/L氯化钙溶液中c(Cl-)和100mL1mol/L氯化钾溶液中c(Cl-)
C.2mol水的摩尔质量和1mol水的摩尔质量
D.20%氢氧化钠溶液中氢氧化钠物质的量浓度和10%氢氧化钠溶液中氢氧化钠物质的量浓度
【答案】B
【解析】
A.64g二氧化硫的物质的量为64g÷64g/mol=1mol,含有2mol氧原子,标况下22.4L二氧化碳的物质的量为22.4L÷22.4L/mol=1mol,含有2mol氧原子,前者与后者相等,故A不符合题意;
B.c(Cl-)的浓度与体积无关,1 mol/L氯化钙溶液中c(Cl-)=2mol/L,1 mol/L氯化钾溶液中c(Cl-)=1mol/L,故B符合题意;
C.水的摩尔质量为18g/mol,与物质的量多少无关,故C不符合题意;
D. 由c=![]() 可知,M相同,NaOH溶液的ω越大,其ρ越大,则20%氢氧化钠溶液中氢氧化钠物质的量浓度比10%氢氧化钠溶液中氢氧化钠物质的量浓度的2倍大,故D不符合题意;
可知,M相同,NaOH溶液的ω越大,其ρ越大,则20%氢氧化钠溶液中氢氧化钠物质的量浓度比10%氢氧化钠溶液中氢氧化钠物质的量浓度的2倍大,故D不符合题意;
答案为B。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】已知饱和氯化铵溶液与亚硝酸钠晶体混合加热可制备氮气。利用如下装置制取氮气,并用氮气制备Ca3N2,Ca3N2遇水发生水解反应。下列说法错误的是
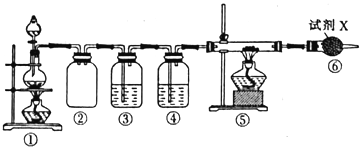
A. ①中发生的化学反应为NaNO2+NH4Cl![]() NaCl+N2↑+2H2O
NaCl+N2↑+2H2O
B. ④、⑥中依次盛装的试剂可以是浓H2SO4、碱石灰
C. ③中盛放的试剂是NaOH 溶液
D. 实验结束,取⑤中的少量产物于试管中,加适量蒸馏水,可以使试管口湿润的红色石蕊试纸变蓝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用甲烷与氯气发生取代反应的副产品生产盐酸的设想在工业上已成为现实。某化学兴趣小组拟在实验室中模拟上述过程,所设计的装置如图所示:

(1)A中制取Cl2的反应的化学方程式是_________________________。
(2)B装置的作用:①______;②______;③______。
(3)D装置中的石棉上吸附着潮湿的KI,其作用是________________。
(4)E装置的作用是_____(填序号)。
A.收集气体 B.吸收氯气 C.吸收氯化氢
(5)E装置中除了有盐酸生成外,还含有有机物,从E中分离出盐酸的最佳方法是______________。
(6)将1 mol CH4与Cl2发生取代反应,测得4种有机取代产物的物质的量相等,则消耗的氯气的物质的量是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温时,向20 mL 0.100 0 mol·L-1 H2C2O4溶液中滴加0.100 0 mol·L-1 NaOH溶液,混合溶液的pH随滴加NaOH溶液体积的变化关系如图所示。下列有关叙述错误的是

A. 忽略H2C2O4的第二步电离,由题给信息,可以计算出常温下H2C2O4的电离常数
B. A、B、C三点所对应的溶液中,水的电离程度最小的是A点
C. A、B、C三点所对应的溶液中,均有c(Na+)<c(OH-)+c(HC2O4-)+2c(C2O42-)
D. 在B点溶液中,生成的含钠化合物有两种,且c(HC2O4-)+2c(C2O42-)=0.100 0 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯醚是一种麻醉剂,其合成路线如图,有关说法正确的是( )
![]()
A. X可能是Br2B. X可能为HO﹣Cl
C. 乙烯醚易溶于水D. ①②③反应类型依次为取代、取代和消去
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积一定的密闭容器中,置入一定量的NO(g)和足量C(s),发生反应C(s)+2NO(g) ![]() CO2(g)+N2(g),平衡状态时NO(g)的物质的量浓度[NO]与温度T的关系如图所示。则下列说法中正确的是( )
CO2(g)+N2(g),平衡状态时NO(g)的物质的量浓度[NO]与温度T的关系如图所示。则下列说法中正确的是( )

A. 该反应的ΔH>0
B. 若该反应在T1、T2时的平衡常数分别为K1、K2,则K1<K2
C. 在T2时,若反应体系处于状态D,则此时一定有v正<v逆
D. 在T3时,若混合气体的密度不再变化,则可以判断反应达到平衡状态C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业生产钠和烧碱的原理如下:①电解熔融氯化钠制钠:2NaCl(熔融) ![]() 2Na+Cl2↑,②电解饱和食盐水制烧碱:2NaCl+2H2O
2Na+Cl2↑,②电解饱和食盐水制烧碱:2NaCl+2H2O ![]() 2NaOH+H2↑+Cl2↑,下列有关说法正确的是( )
2NaOH+H2↑+Cl2↑,下列有关说法正确的是( )
A.在反应①和②中,氯化钠均既是氧化剂,又是还原剂
B.在反应①中氯气是还原产物,在反应②中氢气是还原产物
C.若标准状况下生成等体积的气体,则反应①和②中转移电子总数相等
D.若消耗等质量的氯化钠,则反应①和②中转移电子总数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中的颜色变化,与氧化还原反应无关的是( )
A. NaOH溶液滴入FeSO4溶液中,产生白色沉淀,随后变为红褐色
B. 石蕊溶液滴入氯水中,溶液变红,随后迅速褪色
C. Na2S溶液滴入AgCl浊液中,沉淀由白色逐渐变为黑色
D. 热铜丝插入稀硝酸中,产生无色气体,随后变为红棕色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(加试题)三氧化二镍(Ni2O3)是一种灰黑色无气味有光泽的块状物,常用于制作重要的电子元件材料和蓄电池材料。某实验室尝试用工业废弃的NiO催化剂(还含有Fe2O3、CaO、CuO、BaO等杂质)为原料生产2NiOOHH2O沉淀,继而制备Ni2O3。实验工艺流程为:
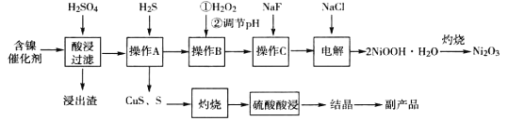
已知:①有关氢氧化物开始沉淀和沉淀完全的pH如表:
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
开始沉淀的pH | 1.5 | 6.5 | 7.2 |
沉淀完全的pH | 3.6 | 9.7 | 9.2 |
②常温下CaF2难溶于水,微溶于无机酸
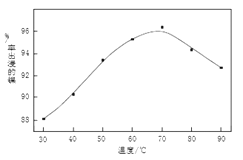
(1)操作B中需调节pH范围为____,使用Na2CO3调节pH过程中发生的反应有___。实验人员发现温度不同时,镍的浸出率不同,浸出率与温度的关系如图所示。请解释当温度高于70℃时,浸出液中Ni2+含量降低的原因____。
(2)下列说法正确的是____
A.为提高酸浸效率,可充分搅拌或适当提高硫酸浓度
B.操作A中应持续通入过量H2S气体使杂质Cu2+彻底沉淀
C.浸出渣的主要成分为CaSO42H2O和BaSO4
D.为得到副产品胆矾,应蒸发浓缩至出现大量晶体,用玻璃纤维代替滤纸进行趁热过滤
(3)电解过程中,Cl-在阳极被氧化为ClO-,但是反应前后溶液中Cl-浓度不变。写出生成沉淀反应的离子方程式_____。
(4)操作C加入NaF后如何证明沉淀完全____。
(5)工业上也可通过将草酸镍(NiC2O42H2O)在热空气中干燥脱水,再在高温下煅烧三小时制得Ni2O3,同时获得混合气体。草酸镍受热分解的化学方程式为____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com