
| A、使用催化剂和施加高压,都能提高反应速率,都对化学平衡状态无影响 |
| B、使用催化剂和施加高压,都能提高反应速率,只有压强对化学平衡状态有影响 |
| C、采用循环操作,能提高NH3的平衡浓度 |
| D、采用循环操作,能加快反应速率 |


科目:高中化学 来源: 题型:


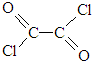 )与足量有机物D反应的化学方程式
)与足量有机物D反应的化学方程式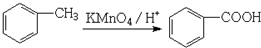

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2,其它条件相同的情况下,使用不同催化剂(Ⅰ,Ⅱ,Ⅲ),CH4的产量随光照时间的变化如图所示.
利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2,其它条件相同的情况下,使用不同催化剂(Ⅰ,Ⅱ,Ⅲ),CH4的产量随光照时间的变化如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
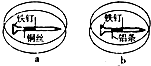 如图所示,将紧紧缠绕不同金属的铁钉放入培养皿中,再加入含有适量酚酞和
如图所示,将紧紧缠绕不同金属的铁钉放入培养皿中,再加入含有适量酚酞和| A、a中铁钉发生还原反应 |
| B、b中铁钉附近呈现红色 |
| C、a中铜丝附近呈现蓝色 |
| D、b中铝条附近有气泡产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图是干冰的晶胞结构示意图.请完成下列问题:
如图是干冰的晶胞结构示意图.请完成下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
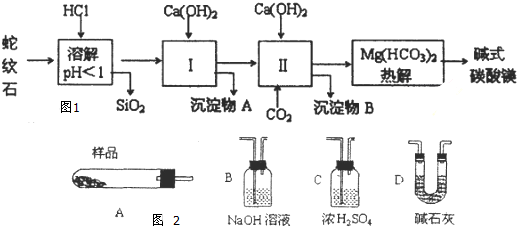
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 1.9 | 3.3 | 9.4 |
沉淀完全时PH | 3.2 | 5.4 | 12.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
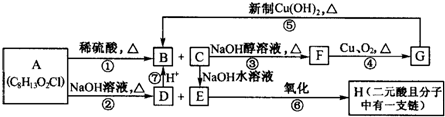
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、酸式滴定管滴至终点,俯视读数 |
| B、碱液移入锥形瓶后,加入10mL蒸馏水 |
| C、酸式滴定管注入酸溶液后,尖嘴无气泡时开始滴定,滴定后有气泡 |
| D、酸式滴定管用蒸馏水洗涤后,未用标准液润洗 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com