
【题目】合成氨生产技术的创立开辟了人工固氮的途径,对化学工业技术也产生了重大影响.利用N2和H2合成氨,目前工业的生产条件为:催化剂(铁触媒),温度(400~500℃),压强(30~50MPa),如图为流程示意图:
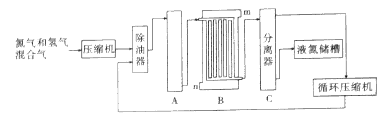
请回答下列问题:
(1)工业合成氨的原料是氮气和氢气.氮气是从空气中分离出来的,通常使用的两种分离方法是__________,__________;氢气的来源是水和碳氢化合物,写出分别采用煤和天然气为原料制取氢气的化学反应方程式__________,__________;
(2)设备A中含有电加热器、铁触煤和热交换器,设备A的名称__________,其中发生的化学反应方程式为__________;实际生产中采用400~500℃的高温,原因之一是__________,原因之二是__________。
(3)设备B的名称__________,其中m和n是两个通水口,入水口是__________(填“m”或“n”).不宜从相反方向通水的原因是__________;
(4)设备C的作用__________;
(5)在原料气制备过程中混有CO对催化剂有毒害作用,欲除去原料气中的CO,可通过如下反应来实现:CO(g)+H2O(g)![]() CO2(g)+H2(g),已知1000K时该反应的平衡常数K=1,若要使CO的转化超过90%,则起始物中c(H2O):c(CO)不低于__________。
CO2(g)+H2(g),已知1000K时该反应的平衡常数K=1,若要使CO的转化超过90%,则起始物中c(H2O):c(CO)不低于__________。
【答案】
(1)液化、分馏 与碳反应后除去CO2
C+H2O![]() CO+H2 CH4+H2O
CO+H2 CH4+H2O![]() CO+3H2
CO+3H2
(2)合成(氨)塔 N2+3H2![]() 2NH3(必须注明反应条件)
2NH3(必须注明反应条件)
温度太低,反应速率慢,温度太高,平衡逆向移动;在400~500℃时催化剂的活性最高
(3)冷却塔(或冷凝器) n 高温气体由冷却塔的上端进入,冷却水从下端进入,逆向冷却效果好
(4)将液氨与未反应的原料气分离
(5)9
【解析】
试题分析:(1)分离空气提取氮气的方法有两种,以上液化、分馏空气,另一种为空气与碳反应生成二氧化碳,反应后除去二氧化碳气体;C和水反应的方程式为C+H2O![]() CO+H2,甲烷与水反应的方程式为CH4+H2O
CO+H2,甲烷与水反应的方程式为CH4+H2O![]() CO+3H2,故答案为:液化、分馏;与碳反应后除去CO2;C+H2O
CO+3H2,故答案为:液化、分馏;与碳反应后除去CO2;C+H2O![]() CO+H2;CH4+H2O
CO+H2;CH4+H2O![]() CO+3H2;
CO+3H2;
(2)合成氨的设备为合成塔,发生N2(g)+3H2(g)![]() 2NH3(g),实际生产中采用400~500℃的高温,原因之一是考虑到催化剂的催化活性,升高温度虽然不利于平衡向正反应方向移动,但能增大反应速率,缩短达到平衡的时间,这是原因之二,故答案为:合成(氨)塔;N2(g)+3H2(g)
2NH3(g),实际生产中采用400~500℃的高温,原因之一是考虑到催化剂的催化活性,升高温度虽然不利于平衡向正反应方向移动,但能增大反应速率,缩短达到平衡的时间,这是原因之二,故答案为:合成(氨)塔;N2(g)+3H2(g)![]() 2NH3(g);催化剂的催化活性;增加反应速率,缩短达到平衡的时间;
2NH3(g);催化剂的催化活性;增加反应速率,缩短达到平衡的时间;
(3)冷凝分离设备为冷凝塔或冷凝器,水流和气流方向应逆向,则入水口是n,高温气体由冷凝塔上端进入,冷凝水从下端进入,可使冷水充满冷凝器,逆向冷凝效果好,故答案为:冷凝塔或冷凝器;n;高温气体由冷凝塔上端进入,冷凝水从下端进入,逆向冷凝效果好;
(4)分离器用来分离液氨和原料气,故答案为:将液氨与未反应的原料气分离;
(5)设CO、H2O起始物质的量浓度分别为x和y,按CO的转化率为90%计算,则
CO(g) + H2O(g)![]() CO2(g) + H2(g)
CO2(g) + H2(g)
起始浓度: x y 0 0
转化浓度: 0.9x 0.9x 0.9x 0.9x
平衡浓度: 0.1x ![]() 0.9x 0.9x
0.9x 0.9x
根据![]() ,求得
,求得![]() 。只要y∶x不低于9,CO的转化率便会超过90%。故答案为:9。
。只要y∶x不低于9,CO的转化率便会超过90%。故答案为:9。


科目:高中化学 来源: 题型:
【题目】在容器可变的密闭容器中,反应N2(g)+3H2(g)![]() 2NH3(g)在一定条件下达到平衡。完成下列填空:
2NH3(g)在一定条件下达到平衡。完成下列填空:
(1)在其他条件不变的情况下,缩小容器体积以增大反应体系的压强,v正______(选填“增大”、“减小”,下同),v逆______,平衡向______方向移动(选填“正反应”、“逆反应”)。
(2)在其他条件不变的情况下,降低温度平衡向正反应方向移动,为______反应(选填“吸热”、“放热”)。
(3)如图为反应速率(ν)与时间(t)关系的示意图,由图判断,在t1时刻曲线发生变化的原因是______(填写编号)。

a.增大N2的浓度 b.扩大容器体积 c.加入催化剂 d.升高温度
改变条件后,平衡混合物中NH3的百分含量______(选填“增大”、“减小”、“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有反应mA(g)+nB(g)![]() pC(g),达到平衡后,当升高温度时,B的转化率减小;当减小压强时,混合体系中A的质量分数增大,则
pC(g),达到平衡后,当升高温度时,B的转化率减小;当减小压强时,混合体系中A的质量分数增大,则
(1)该反应的正反应是__________热反应,且m+n__________p (填“>”、“<”或“=”)。
(2)增大压强时,B的转化率__________(填“增大”、“减小”或“不变”,下同),逆反应速率__________。
(3)若加入C(体积不变),则A的体积分数__________。
(4)若降低温度,则平衡时B、C的浓度之比c(C)/c(B)比值将________。
(5)若加入催化剂,该反应的反应热________。
(6)若B是有色物质,A、C均为无色物质,维持容器体积不变,充入氖气时,混合气体的颜色__________(填“变浅”、“变深”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】芳香化合物A是一种基本化工原料,可以从煤和石油中得到。OPA是一种重要的有机化工中间体.A、B、C、D、E、F和OPA的转化关系如下所示:
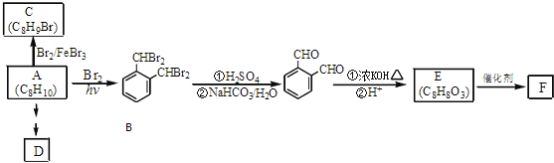
回答下列问题:
(1)A的化学名称是____________;
(2)由A生成B 的反应类型是____________,在该反应的副产物中,与B互为同分异构体的化合物的结构简式为____________;
(3)写出C所有可能的结构简式____________;
(4)D(邻苯二甲酸二乙酯)是一种增塑剂.请用A、不超过两个碳的有机物及合适的无机试剂为原料,经两步反应合成D。用结构简式表示合成路线____________;
(5)OPA的化学名称是____________,OPA经中间体E可合成一种聚酯类高分子化合物F,由E合成F的反应类型为____________,该反应的化学方程式为____________;(提示![]() )
)
(6)芳香化合物G是E的同分异构体,G分子中含有醛基、酯基和醚基三种含氧官能团,写出G所有可能的结构简式____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【加试题】在一个容积固定不变的密闭容器中进行反应:
2X(g) + Y(g) ![]() 2Z(g) ,已知将2molX和1molY充入该容器中,反应在绝热条件下达到平衡时,Z的物质的量为pmol。回答下列问题:21m
2Z(g) ,已知将2molX和1molY充入该容器中,反应在绝热条件下达到平衡时,Z的物质的量为pmol。回答下列问题:21m
(1)若把2molX和1molY充入该容器时,处于状态I,达到平衡时处于状态II(如图1),则该反应的△H
0;熵变△S 0 ( 填:“< ,> ,= ”)。该反应在 (填:高温或低温)条件下能自发进行。

(2)该反应的v-t图像如图2中左图所示。若其他条件不变,仅在反应前加入合适的催化剂,则其v-t图像如图2中右图所示。以下说法正确的是
① a1>a2 ②b1<b2 ③ t1>t2 ④ 右图中阴影部分面积更大 ⑤两图中阴影部分面积相等
(3)若该反应在容积可变的密闭容器中发生,在温度为T1、T2时,平衡体系中X的体积分数随压强变化曲线如图所示。下列说法正确的是 。

A.A、C两点的反应速率:A>C
B.A、C两点的气体密度:A<C
C.B、C两点的气体的平均相对分子质量:B<C
D.由状态B到状态A,可以用加热的方法
E.A、C两点X的浓度:A>C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着能源危机的加剧,我国也在大力推广新一代乙醇燃料,广西是我国甘蔗产量主产区之一,乙醇可以从甘蔗中提炼加工出来,乙醇除用作燃料外,还可以用它合成其他有机物。下面是以乙醇为起始原料的转化关系,请回答相关问题。
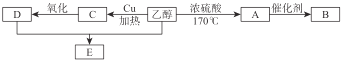
①B在日常生活中常用来作食品包装袋,但往往会带来环境问题。
写出A→B的化学方程式: 。
②写出乙醇→A的化学方程式: 。
③写出乙醇→C的化学方程式: 。
④写出E的方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四氯化锡用作媒染剂和有机合成上的氯化催化剂,甲、乙为实验室制备四氯化锡的反应装置示意图,有关信息数据如下:

有关信息数据:①实验室制备四氯化锡的操作是将金属锡熔融,然后泼入冷水,制成锡花,将干燥的锡花加入反应器中,再向反应器中缓缓通入干燥氯气;②无水四氯化锡是无色易流动的液体,熔点-33℃,沸点114.1℃,③无水四氯化锡暴露于空气中与空气中的水分反应生成白色烟雾,有强烈的刺激性。请回答下列问题:
Ⅰ、图甲是实验室制备干燥氯气的实验装置(夹持装置已略)
(1)A的仪器名称为__________,该装置制备氯气选用的药品为漂粉精固体[主要成分Ca(ClO)2]和浓盐酸,B中发生反应的化学方程式为__________。
(2)装置C中饱和食盐水的作用是__________,同时装置C亦是安全瓶,能检测实验进行时是否发生堵塞,请写出发生堵塞时C中的现象:__________。
(3)试剂X可能为__________(填序号)
A无水氯化钙 B浓硫酸 C.碱石灰 D五氧化二磷
(4)用锡花代替锡粒的目的是__________。
Ⅱ.图乙是蒸馏SnCl4的装置
(1)图中,收集到的SnCl4中可能存在的副产物的化学式为__________。
(2)该装置尚有两处不当之处,它们分别是__________,__________;
(3)若实验中用去锡粉5,95g,反应后,Ⅱ中锥形瓶里收集到12.0gSnCl4。则SnCl4的产率为__________。(结果保留3位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[选修 2—化学与技术]Ⅰ下列说法不正确的是
A.明矾、漂白粉、臭氧的净水原理相同
B.“血液透析”的原理利用了胶体的性质
C.食品包装中常放入有硅胶和铁粉的小袋,只能防止食物受潮
D.煤炭燃烧、机动车尾气、建筑扬尘等可加重雾霾
Ⅱ水是一种重要的自然资源,是人类赖以生存不可或缺的物质。 水质优劣直接影响人体健康。 海水是人类资源宝库,若把海水淡化和化工生产结合起来,既可解决淡水资源缺乏的问题,又可充分利用海洋资源。 据此,回答下列问题:
(1)天然水灾净化处理过程中需要加入的混凝剂,我们常用的混凝剂有明矾、硫酸铝、硫酸铁,其净水作用的原理是 。
(2)水的净化与软化的区别是水的净化是用混凝剂(如明矾等)将 。
(3)目前,国际上实用的“海水淡化”主要技术之一是蒸馏法。 蒸馏法是将海水变成蒸汽,蒸汽经冷却而得高纯度淡水。由此可判断蒸馏法是 (选填“物理变化”或“化学变化”)。
(4)海水除了可以得到淡化水外,还可提取多种化工原料。由海水制备无水氯化镁,主要有以下步骤:
①在一定条件下脱水干燥;②加熟石灰;③加盐酸;④过滤;⑤浓缩结晶。其先后顺序正确的是
A.②④⑤③①
B.③②④①⑤
C.③④②⑤①
D.②④③⑤①
(5)海水电解制得的氢气用于合成氨,某合成氨厂生产流程图如下

①第(1)个设备中先把N2和H2压缩的目的是 。
②在第(3)个设备中用冷却的方法分离出 ,其目的是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通常氢氧燃料电池有酸式和碱式两种,试回答下列问题:
(1)在酸式介质中,酸式电池的电极反应:负极: ,
正极: 。电解质溶液的pH (填“变大”、“变小”或“不变”)。
(2)在碱式介质中,碱式电池的电极反应:
负极: ,正极: 。
电解质溶液的pH (填“变大”、“变小”或“不变”)。
(3)氢氧燃料电池汽车作为上海世博园中的交通工具之一,下列有关说法不正确的是________。
A.太阳光催化分解水制氢气比电解水制氢气更为科学
B.氢氧燃料电池作为汽车动力更能保护环境
C.以稀H2SO4、KOH为介质的氢氧燃料电池的负极电极反应式相同
D.以稀H2SO4、KOH为介质的氢氧燃料电池的总反应式相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com