
(14分)实验室用密度为1.19g/mL,质量分数为36.5% 浓盐酸配制250mL0.1mol/L的盐酸溶液,填空并请回答下列问题:
(1)配制250mL0.1mol/L的盐酸溶液
| 应量取盐酸体积/mL | 应选用容量瓶的规格/mL | 除容量瓶外还需要的其它仪器 |
| | | |
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案 期末好成绩系列答案
期末好成绩系列答案科目:高中化学 来源: 题型:实验题
(10分)某同学帮助水质检测站配制480 mL 0.5 mol·L-1 NaOH溶液以备使用。
(1)该同学应选择________mL的容量瓶。
(2)其操作步骤如下图所示,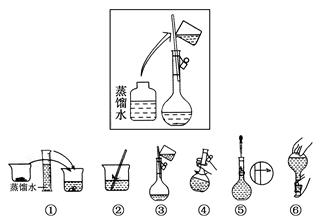
则如图操作应在下图中的________(填选项字母)之间。
A.②与③ B.①与② C.④与⑤
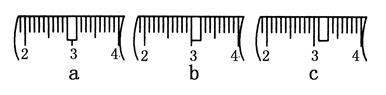
(3)该同学应称取NaOH固体________g,用质量为23.1 g的烧杯放在托盘天平上称取所需NaOH固体时,请在附表中选取所需的砝码大小________(填字母),并在下图中选出能正确表示游码位置的选项________(填字母)。
附表 砝码规格
| | a | b | c | d | e |
| 砝码大小/g | 100 | 50 | 20 | 10 | 5 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(8分)下图是我校实验室化学试剂浓硫酸标签上的部分内容。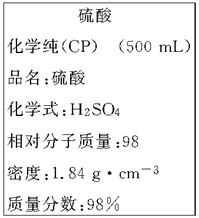
现需要480 mL 1 mol·L-1的稀硫酸。用该浓硫酸和蒸馏水配制,可供选用的仪器有:
①胶头滴管;②玻璃棒;③烧杯;④量筒。
请回答下列问题:
(1)配制稀硫酸时,还缺少的仪器有_________________(写仪器名称)。
(2)经计算,所需浓硫酸的体积约为________mL;若将该浓硫酸与等体积的水混合,所得溶液中溶质的质量分数____49%(填“>” 、“<” 或“=”)。
(3)对所配制的稀硫酸进行测定,发现其浓度大于1 mol·L-1,配制过程中下列各项操作可能引起该误差的原因是________。
①用量筒量取浓硫酸时,仰视刻度线
②容量瓶用蒸馏水洗涤后未经干燥
③用量筒量取浓硫酸后,用蒸馏水将量筒洗涤干净,洗涤液转移到烧杯中
④转移溶液时,不慎有少量溶液洒出
⑤定容时,俯视容量瓶刻度线
⑥定容后,把容量瓶倒置摇匀,正放后发现液面低于刻度线,再加蒸馏水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(每空2分,共12分)
用质量分数为37.5%的浓盐酸(密度为1.16g/cm3)配制成1mol/L的稀盐酸。现实验室仅需要这种盐酸220mL。试回答下列问题:
(1)配制稀盐酸时,应选用容量为 mL的容量瓶;
(2)经计算需要量取 mL浓盐酸,在量取时宜选用下列量筒中的 。
| A.5 mL | B.10 mL | C.25 mL | D.50 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
用Na2CO3·10H2O晶体,配制0.2 mol·L-1的Na2CO3溶液480 mL。
(1)应称取Na2CO3·10H2O晶体的质量为 。
(2)根据下列操作对所配溶液的浓度产生的影响,完成下列要求:
①Na2CO3·10H2O晶体失去了部分结晶水
②碳酸钠晶体不纯,其中混有氯化钠
③称量碳酸钠晶体时所用砝码生锈
④容量瓶未经干燥使用
其中引起所配溶液浓度偏高的有 (填序号,下同),偏低的有 ,无影响的有 。
(3)某同学改用固体Na2CO3配制上述Na2CO3溶液的过程如图所示: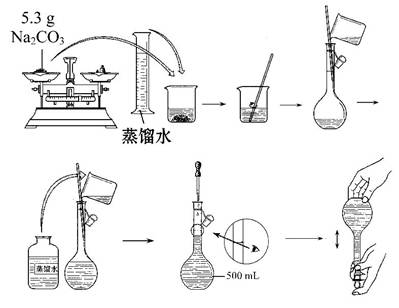
你认为该同学的错误步骤有 (填序号)。
| A.1处 | B.2处 | C.3处 | D.4处 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(18分,每小题2分)用质量分数为98%,密度为1.84g/cm3的浓硫酸来配置500ml,0.2mol/L的稀硫酸。可供选择①玻璃棒 ②烧瓶 ③烧杯 ④胶头滴管 ⑤量筒 ⑥容量瓶 ⑦托盘天平 ⑧药匙.请回答下列问题:
(1)上述仪器中,在配制稀硫酸时用不到的有 (填代号) .
(2)经计算,需浓硫酸的体积为 mL(保留一位小数); 。
(3)将浓硫酸加适量蒸馏水稀释后,冷却片刻,随后全部转移到 mL的容量瓶中,转移时应用 玻璃棒 .转移完毕,用少量蒸馏水洗涤 2~3次,并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,振荡容量瓶,使溶液混合均匀.然后缓缓地把蒸馏水直接注入容量瓶直到液面接近瓶颈刻度 cm处,改用 滴加蒸馏水,使 .塞上瓶塞、摇匀后,把溶液倒入试剂瓶、贴上标签.
(4)定容时,俯视刻度线,所配溶液的物质的量浓度将 (选填“偏高”、“偏低”或“不变”)
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
化学与社会、生活密切相关,下列说法不正确的是
| A.在食品袋中放入盛有CaO和硫酸亚铁的透气小袋,可防止食物受潮、氧化变质 |
| B.MgO、Al2O3的熔点很高,工业上用于制作耐高温材料,也用与冶炼铝和镁 |
| C.发酵粉中主要含有碳酸氢钠,能使焙制出的糕点疏松多孔 |
| D.利用ClO2对自来水消毒主要是因为ClO2具有强氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列各组中的两物质相互反应时,若改变反应条件(温度、反应物用量比),化学反应的产物并不改变的是( )
A.Na和O2 B.NaOH和CO2
C.Na2O2和CO2 D.木炭(C)和O2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com