
| A. | 固体2是氧化铁 | |
| B. | X的化学式可以表示为Fe3C2 | |
| C. | 溶液甲中可能含有Fe3+ | |
| D. | X与足量的热浓硝酸反应有NO2和CO2生成 |
分析 铁碳化合物X,在足量空气中煅烧得固体1为铁的氧化物,可以有+2价或+3价的铁,溶于盐酸所得溶液中可能Fe2+和Fe3+,再能入足量的氯气,溶液中都为+3价的铁,加热蒸发,铁离子水解,生成氢氧化铁,灼烧后氢氧化铁分解得固体2为氧化铁,24g氧化铁中含有铁元素的质量为$\frac{112}{160}×24g$=16.8g,利用元素守恒,可计算得化合物X中铁元素的质量也是16.8g,进而求得X中碳元素的质量为18g-16.8g=1.2g,所以在X中铁、碳原子的物质的量之比为$\frac{16.8}{56}:\frac{1.2}{12}$=3:1,所以X的化学式为Fe3C,Fe3C与热的浓硝酸发生氧化还原反应,碳元素可被氧化成二氧化碳,硝酸中的氮可被还原成二氧化氮,据此答题.
解答 解:铁碳化合物X,在足量空气中煅烧得固体1为铁的氧化物,可以有+2价或+3价的铁,溶于盐酸所得溶液中可能Fe2+和Fe3+,再能入足量的氯气,溶液中都为+3价的铁,加热蒸发,铁离子水解,生成氢氧化铁,灼烧后氢氧化铁分解得固体2为氧化铁,24g氧化铁中含有铁元素的质量为$\frac{112}{160}×24g$=16.8g,利用元素守恒,可计算得化合物X中铁元素的质量也是16.8g,进而求得X中碳元素的质量为18g-16.8g=1.2g,所以在X中铁、碳原子的物质的量之比为$\frac{16.8}{56}:\frac{1.2}{12}$=3:1,所以X的化学式为Fe3C,Fe3C与热的浓硝酸发生氧化还原反应,碳元素可被氧化成二氧化碳,硝酸中的氮可被还原成二氧化氮.
A、固体2是氧化铁,故A正确;
B、X的化学式可以表示为Fe3C,故B错误;
C、溶液甲中可能含有Fe3+,故C正确;
D、X与足量的热浓硝酸反应有NO2和CO2生成,故D正确;
故选B.
点评 本题主要考查了铁的相关知识,结合实验过程利用元素守恒分析和计算,中等难度,答题时注意元素化合物知识的灵活运用.


科目:高中化学 来源: 题型:选择题
| A. | Na2O2在反应中作氧化剂,又作还原剂 | |
| B. | 高铁酸钾在该温度下的溶解度比高铁酸钠的溶解度小 | |
| C. | K2FeO4能消毒杀菌,其还原产物水解生成的Fe(OH)3胶体能吸附水中的悬浮物 | |
| D. | 制取高铁酸钠时,每生成1mol Na2FeO4反应中共有4mol电子转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 配制0.1 mol•L-1 NaCl溶液时,其中一步是将已准确称量的NaCl放入烧杯中并加适量的水搅拌溶解 | |
| B. | 配制1 mol•L-1 NaOH溶液时,将溶解后的NaOH溶液立即注入容量瓶 | |
| C. | 配制0.1 mol•L-1的H2SO4溶液时,将量取的浓H2SO4放入容量瓶中加水稀释 | |
| D. | 配制1 mol•L-1 Na2CO3溶液500 mL,将Na2CO3放在托盘天平右盘称量 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
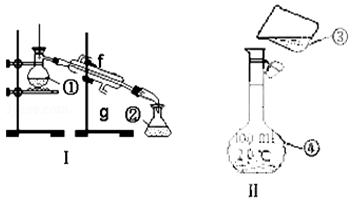
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
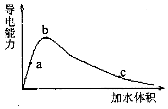 一定温度下,将一定量的冰醋酸加水稀释,稀释过程中溶液的导电性变化如图所示.则下列说法错误的是( )
一定温度下,将一定量的冰醋酸加水稀释,稀释过程中溶液的导电性变化如图所示.则下列说法错误的是( )| A. | 醋酸的电离度:c<b<a | |
| B. | 溶液的PH值:b<a<c | |
| C. | 蘸取a点溶液滴在湿润的PH试纸上,测得PH值一定偏大 | |
| D. | 若分别取a、b、c三点的溶液各10mL,各用同浓度的氢氧化钠溶液中和,消耗NaOH溶液的体积a=b=c |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6).
北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6).查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com