
【题目】(加试题)(有机物G(C26H26O2N4)是一种塑料添加剂,可以提高塑料的使用寿命,其合成有关路线如图:

已知:①F的1H-NMR谱中只有一个峰
②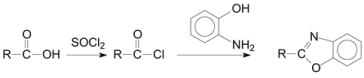
请回答:
(1)下列说法不正确的是___
A.A→B的反应需控制在较低温度,因为酚容易被氧化
B.B→C是发生了加成反应
C.D物质既具有酸性,也具有碱性
D.E在工业上的主要来源是石油工业中的催化重整
(2)G的结构简式______
(3)写出C→D的反应方程式____
(4)请设计以E为原料合成F的合成路线(用流程图表示,可使用n≤2的有机物,无机试剂任选)____
(5)写出化合物C可能的同分异构体的结构简式___。
须同时符合:①能与FeCl3溶液显色 ②苯环上的氢只有2种且苯环上只有2个取代基
【答案】B 
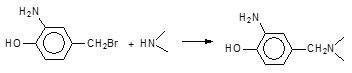 +HBr
+HBr 
 、
、![]() 、
、![]() 、
、![]()
【解析】
A为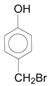 ,在浓硫酸催化作用下与浓硝酸发生消化反应生成B(
,在浓硫酸催化作用下与浓硝酸发生消化反应生成B(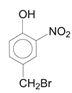 ),根据D中羟基的邻位为氨基,利用逆合成分析法可知,B到C发生了硝基的还原反应生成转化为氨基,故推出C为
),根据D中羟基的邻位为氨基,利用逆合成分析法可知,B到C发生了硝基的还原反应生成转化为氨基,故推出C为 ,C再发生取代反应生成D;根据F的分子式及给定信息“F的1H-NMR谱中只有一个峰”可知,F为对称结构,其结构简式为:
,C再发生取代反应生成D;根据F的分子式及给定信息“F的1H-NMR谱中只有一个峰”可知,F为对称结构,其结构简式为: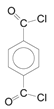 ;结合给定信息②可知,E先经过氧化反应生成对苯二甲酸,然后在SOCl2的作用下生成F,F再与D结合生成分子式为C26H26O2N4的G,则G为
;结合给定信息②可知,E先经过氧化反应生成对苯二甲酸,然后在SOCl2的作用下生成F,F再与D结合生成分子式为C26H26O2N4的G,则G为 ,据此分析作答。
,据此分析作答。
(1)A.因酚容易被氧化,故A→B的反应需控制在较低温度,A项正确;
B.B→C是发生了还原反应,硝基转化为氨基,故不属于加成反应,B项错误;
C.D分子内含有具有酸性的酚羟基,也含具有碱性的氨基,C项正确;
D.苯乙烷来自于石油工业中的催化重整,D项正确;
答案选B;
(2)根据上述分析可知,G的结构简式为: ;
;
(3)C→D的反应方程式为
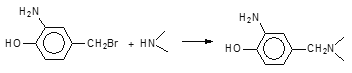 +HBr;
+HBr;
(4)根据上述分析可知,E先经过氧化反应生成对苯二甲酸,然后在SOCl2的作用下生成F,故可设计合成路线如下: ;
;
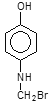
(5)化合物C为 ,其分子式为C7H9NOBr,不饱和度为4,①能与FeCl3溶液显色,说明含有酚羟基; ②苯环上的氢只有2种且苯环上只有2个取代基,则说明取代基的位置为对位,那么满足上述条件的C的同分异构体可以是:
,其分子式为C7H9NOBr,不饱和度为4,①能与FeCl3溶液显色,说明含有酚羟基; ②苯环上的氢只有2种且苯环上只有2个取代基,则说明取代基的位置为对位,那么满足上述条件的C的同分异构体可以是: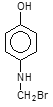 、
、![]() 、
、![]() 、
、![]() 。
。


科目:高中化学 来源: 题型:
【题目】某同学通过如下流程制备氧化亚铜:

已知CuCl难溶于水和稀硫酸:Cu2O+2H+==Cu2++Cu+H2O
下列说法不正确的是
A. 步骤②SO2可用Na2SO3替换
B. 步骤③中为防止CuCl被氧化,可用SO2水溶液洗涤
C. 步骤④发生反应的离子方程式为2CuCl+2OH-=Cu2O+2Cl-+H2O
D. 如果Cu2O试样中混有CuCl和CuO杂质,用足量稀硫酸与Cu2O试样充分反应,根据反应前、后固体质量可计算试样纯度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答问题
(1)用一种试剂除去下列物质中的杂质(括号内物质为杂质,所用试剂均为适量),写出所加的试剂及有关反应的离子方程式。
①FeSO4溶液(CuSO4):试剂___离子方程式___。
②Cu(Mg):试剂___,离子方程式___。
(2)写出下列反应的离子方程式
①氯化铁溶液与氢氧化钠溶液的反应___;
②常用澄清石灰水检验CO2气体___;
③用小苏打片(NaHCO3)治疗胃酸过多___。
(3)用双线桥标出下列反应中电子转移的方向和数目。___
Cl2+SO2+2H2O=H2SO4+2HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeCl3是中学实验室常用的试剂,可以用来制备氢氧化铁胶体。
(1)下列制备氢氧化铁胶体的操作方法正确的是____________(填字母);
a.向饱和氯化铁溶液中滴加少量的氢氧化钠稀溶液
b.加热煮沸氯化铁饱和溶液
c.![]() 氨水中滴加氯化铁浓溶液
氨水中滴加氯化铁浓溶液
d.在沸水中滴加饱和氯化铁溶液,煮沸至液体呈红褐色
(2)写出制备氢氧化铁胶体的离子方程式__________________________;
(3)下列与胶体性质无关的是_____________(填字母);
a.河流入海口处形成沙洲
b.使用微波手术刀进行外科手术,可使开刀处的血液迅速凝固而减少失血
c.肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗
d.在饱和氯化铁溶液中滴加NaOH溶液,产生红褐色沉淀
e.冶金厂常用高压电除去烟尘
(4)从溶液中分离提纯Fe(OH)3胶体的方法叫_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用质量分数为36.5%的盐酸(密度为1.20g/㎝3)配制480mL1.0mol/LHCl。回答下列问题:
(1)此浓盐酸的物质的量浓度是________________
(2)配制时,必要的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管、____________________。该试验中两次用到玻璃棒,其作用分别是 ___________________,________________________。
(3)若实验遇下列情况,溶液的浓度偏高的是 __________________________________________
A.量取浓盐酸时仰视量筒刻度
B.摇匀后发现液面低于刻度线,滴加蒸馏水至刻度线再摇匀
C.定容时俯视容量瓶的刻度线
D.容量瓶内壁附有水珠而未干燥处理
E.未冷却到室温就定容
(4)若取50.0mL上述已配好的溶液,与另一150mL0.2mol/L的HCl溶液混合,最后得到的溶液的物质的量浓度为_________________(设溶液的体积变化可忽略)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲乙丙三种物质间通过一步反应能实现如图转化,下列选项中符合转化关系的是( )
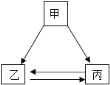
A.甲为NaOH,乙为NaCl,丙为NaNO3
B.甲为CuO,乙为CuCl2,丙为Cu(OH)2
C.甲为Na2CO3,乙为CO2,丙为CaCO3
D.甲为H2SO4,乙为BaSO4,丙为Na2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水蒸气通过的灼热的焦炭后,流出气体的主要成分是 CO 和 H2,还有 CO2和水蒸气等。现利用下图中提供实验装置,证明上述混合气体中有CO 和 H2。(A中加热装置在图中略去)回答下列问题:
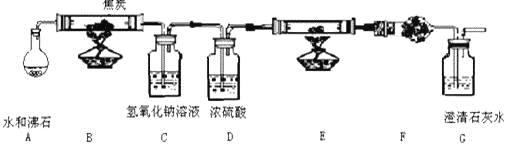
(1) C装置的用途是____________
(2)仪器 E 中需加入的试剂是_____________
(3)仪器 F 中需加入的试剂是:______,其目的是_________________
(4)装置F和G的位置能否颠倒_____,(填“能”或“否”)理由是____________________
(5)能证明混合气中含有 CO 的实验现象是________________________
(6)有人认为该实验装置存在一个缺陷,你认为这个缺陷是___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某次实验需用0.4 mol/LNaOH溶液480mL。配制方法如下:
(1)配制该溶液应选用________mL容量瓶;
(2)用托盘天平准确称量________g固体NaOH,应放在________(仪器)中称量。
(3)将称量好的NaOH固体放在500mL大烧杯中,倒入约100mL蒸馏水,用玻璃棒搅拌,使固体全部溶解,待______________后,将烧杯中的溶液注入容量瓶中;
(4)用少量蒸馏水洗涤烧杯________次,洗涤后的溶液_______________,轻轻晃动容量瓶,使溶液混合均匀;
(5)向容量瓶中加入蒸馏水,到液面接近刻度线__________时,改用_________加蒸馏水至液面最低点与刻度线相切。盖好瓶塞,上下颠倒混合均匀;
(6)若在配制过程中出现下列情况,将使所配制的NaOH溶液的浓度偏高的是________,偏低的是________,对实验结果没有影响的是____________(填各选项的序号)。
A.所用的NaOH中混有少量Na2CO3
B.用带有生锈砝码的托盘天平称量一定质量固体NaOH
C.配制溶液所用的容量瓶洗净后没有烘干
D.固体NaOH在烧杯中溶解后立即将溶液转移到容量瓶内并接着进行后续操作
E.转移溶液后,未洗涤烧杯和玻璃棒就直接定容
F.最后确定NaOH溶液体积(定容)时,俯视观察液面与容量瓶刻度线
G.定容摇匀后静止,发现液面低于刻度线,再加蒸馏水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为探究Cl2、Br2、Fe3+的氧化性强弱,设计了如下实验:

(1)①装置A中发生反应的离子方程式是____。
②整套实验装置存在一处明显的不足,请指出____。
B装置的作用:_____。
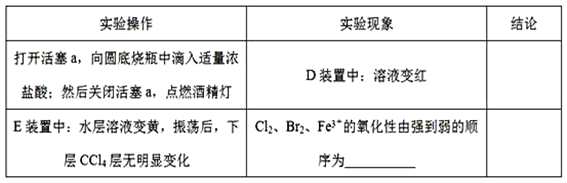
(2)用改正后的装置进行实验,实验过程如下:
①请填写Cl2、Br2、Fe3+氧化性由强到弱的顺序:_____。
②E装置中溶液变黄的原因(请用离子方程式解释)_____。
(3)因忙于观察和记录,没有及时停止反应,D、E中均发生了新的变化。
D装置中:红色慢慢褪去。
E装置中:CCl4层先由无色变为橙色,后颜色逐渐加深,直至变成红色。
为探究上述实验现象的本质,小组同学查得资料如下:

①用平衡移动原理(结合上述资料)解释Cl2过量时D中溶液红色褪去的原因____,现设计简单实验证明上述解释:取少量褪色后的溶液,滴加___溶液,若溶液颜色___,则上述解释是合理的。
②探究E中颜色变化的原因,设计实验如下:
用分液漏斗分离出E的下层溶液,蒸馏、收集红色物质,取少量,加入AgNO3溶液,结果观察到仅有白色沉淀产生。请结合上述资料用两步方程式(离子或化学方程式不限定)解释仅产生白色沉淀原因_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com