
| A. | 非自发进行的反应一定不能发生 | |
| B. | 在一定条件下,非自发进行的反应也能进行 | |
| C. | 自发进行的反应一定迅速 | |
| D. | 凡是熵增加的过程都是自发过程 |
分析 反应自发进行的判断依据是△H-T△S<0;有反应的焓变,熵变,温度共同决定;自发进行只能说明反应进行的方向,不能说明反应发生的难易和快慢,有些非自发进行的反应在一定条件下也可以发生.
解答 解:A、反应是否自发进行,由熵变、焓变、温度共同决定,非自发反应在改变条件下可以发生,故A错误;
B、自发进行只能说明反应进行的方向,不能说明反应发生的难易和快慢,有些非自发进行的反应在一定条件下也可以发生,故B正确;
C、自发进行只能说明反应进行的方向,不能说明反应发生的难易和快慢,故C错误;
D、凡是熵增加的反应不一定能自发进行,如碳酸盐的分解,故D错误.
故选B.
点评 本题考查了化学反应自发进行的判断依据,反应是否自发进行,由熵变、焓变、温度共同决定,题目较简单.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢离子浓度相同 | |
| B. | 导电能力相同 | |
| C. | 相同体积时,中和NaOH的能力相同 | |
| D. | 加水稀释10倍后,溶液的pH值均上升1个单位 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
| Ksp | 2.2×10-20 | 2.6×10-39 | 1.7×10-7 | 1.3×10-12 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L | B. | 0.5L | C. | 0.3L | D. | 0.6L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | 相关信息 |
| A | 原子核外L层电子数是K层的2倍 |
| B | 其一种单质被称为地球生物的“保护伞” |
| C | 元素的第一电离能是第3周期所有元素中最小的 |
| D | 基态原子最外层电子排布为(n+1)sn(n+1)p(n+2) |
| E | 可形成多种氧化物,其中一种为具有磁性的黑色晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图所示装置为在直流电的作用下电解200molNaCl溶液图,其中A、B为石墨电极,a、b为电源的两极,当接通电源,通电一段时间后,B电极产生能使湿润的淀粉碘化钾试纸变蓝的气体224mL(标准状况),则:
如图所示装置为在直流电的作用下电解200molNaCl溶液图,其中A、B为石墨电极,a、b为电源的两极,当接通电源,通电一段时间后,B电极产生能使湿润的淀粉碘化钾试纸变蓝的气体224mL(标准状况),则:查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 锌电极发生还原反应:铜电极发生氧化反应 | |
| B. | 铜电极做正极发生的电极反应为:2H++2e-═H2↑ | |
| C. | 当有13g Zn溶解时,电路中就有0.5mol电子通过 | |
| D. | 电子从锌电极通过电流表流向铜电极 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
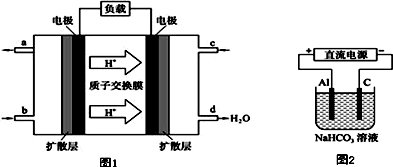
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com