
�л���PAS-Na��һ�����Ʒν��ҩ�����Ч�ɷ֣��л���G��һ��ʳ�����ϣ��Լױ�Ϊԭ�Ϻϳ����������ʵ�·�����£�
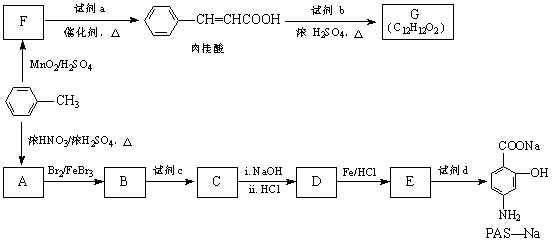

�ش��������⣺
��1��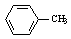 ����A�ķ�Ӧ������ ��
����A�ķ�Ӧ������ ��
��2��F�к��������ŵ������� ���Լ�a�Ľṹ��ʽΪ ��
��3��д����A����B�Ļ�ѧ����ʽ�� ��
��4������ͼ��ʾ�Լ�b����Է�������Ϊ58�������в���������Ϊ��״�ṹ��д����������Լ�b����G�Ļ�ѧ����ʽ�� ��
��5�����Լ�d����ʱ������ѡ�õ��Լ�d�� ������ĸ��ţ���
a��NaHCO3 b��NaOH c��Na2CO3
��6��д��C��NaOH��Ӧ�Ļ�ѧ����ʽ ��
��7��������ж���ͬ���칹�壬���������������� �֡�
a��������������ȡ������
b���ܷ���������Ӧ����1 mol���л����������4 mol Ag��
����������������ͬ���칹���У�д�������������ֲ�ͬ��ѧ������ԭ�ӵ��л���Ľṹ��ʽ����дһ�ּ��ɣ� ��
 �ŵ������ϵ�д�
�ŵ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ʵ�鲻����Ϊ�ж����ݵ���(����)
A���ƺ�þ�ֱ�����ˮ��Ӧ���ж��ƺ�þ������ǿ��
B����MgCl2��AlCl3��Һ�зֱ���������NaOH��Һ���ж�þ�����Ľ�����ǿ��
C������������Һ��ͨ��CO2������ɫ�������ж�̼������������ǿ��
D������HF��HCl��ˮ��Һ������ǿ���жϷ����ȵķǽ����Ե�ǿ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���½������ʱȽϵ�ʵ�飬���������ǣ�������
| �� | A�� | �Ƚ�Cu��Fe2+�Ļ�ԭ�ԣ�����������ͭ��Һ�� |
| �� | B�� | �Ƚ��ȡ��嵥�ʵ������ԣ��廯����Һ��ͨ������ |
| �� | C�� | �Ƚ�þ���������ԣ��Ȼ�þ���Ȼ�����Һ�зֱ���������NaOH��Һ |
| �� | D�� | �Ƚ�̼����ǽ����ԣ��ⶨͬ����ͬ���ʵ���Ũ�ȵ�Na2CO3��Na2SO4��Һ��pH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������ʵ��Ӧ�Ļ�ѧ������ȷ����
A�������Ƽ�����з�̪��ˮ�У���Һ��죺Na + 2H2O === Na+ + 2OH- + H2��
B����NaOH��Һ���ն����������Cl2 + 2OH- === Cl- + ClO-+ H2O
C����NaHCO3��Һ����Ca(OH)2��Һ����а�ɫ������
2HCO3- + Ca2+ + 2OH- === CaCO3�� + 2H2O + CO32-
D����������Һ�ε�����ʯ�������ݲ�����2H+ + CaCO3 === CO2��+ Ca2+ + H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ҵ�ϳ������������������裨CN-����ˮ��һ�������£�������CN-��Ӧ���������塣����˵������ȷ����
A��CN-��̼Ԫ�صĻ��ϼ�Ϊ+2
B���÷�Ӧ�IJ���֮һ������N2
C����1 mol CN-���뷴Ӧʱ��ת��3 mol e-
D��������0.1 mol CN-�ķ�ˮ����������Ҫ���ı�״����Cl2�����Ϊ5.6 L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���и�������ȫ����������ʵ���
A��H2SiO3 H2S CO2 B��MgSO4 CH3COOH CH3CH2OH
C��H2SO3 BaSO4 CH4 D��H2O NH3•H2O H3PO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��������3���Ȼ�ѧ����ʽ��
2H2S��g��+3O2��g����2SO2��g��+2H2O��l�� ��H��Q1 kJ/mol
2H2S��g��+O2��g����2S ��s��+2H2O��l�� ��H��Q2 kJ/mol
2H2S��g��+O2��g����2S ��s��+2H2O��g�� ��H��Q3 kJ/mol
�ж�Q1��Q2��Q3���߹�ϵ��ȷ����
A��Q1>Q2>Q3 B��Q1>Q3>Q2 C��Q3>Q2>Q1 D��Q2>Q1>Q3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
2SO2��g��+O2��g��=2SO3��g����Ӧ���̵������仯��ͼ��ʾ����֪1mol SO2��g������Ϊ1mol SO3��g���Ħ�H= ��99kJ��mol-1����ش��������⣺
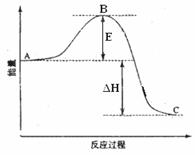
��1��ͼ��A��ʾ ��E�Ĵ�С�Ը÷�Ӧ�ķ�Ӧ�� ����С����ޡ���Ӱ�졣�÷�Ӧͨ����V2O5����������V2O5��ʹͼ��B�� ������ߡ����ǡ����͡�������H ����������С�����䡱���������� ��
��2����֪�������ȼ����Ϊ296 KJ��mol-1�������� S��s������3 molSO3��g���ġ�H��Ҫ�������̣���
S��s������3 molSO3��g���ġ�H��Ҫ�������̣���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ṹ��ʽ��ͼ�����������е�һ����ԭ�ӱ���ԭ��ȡ�������γɵ�һ�ȴ����������(����)

A��1�� B��2��
C��3�� D��4��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com