
| A�� | 0.1 mol/L Na2CO3��Һ��c��OH-��=c��HCO3-��+c��H+��+c��H2CO3�� | |
| B�� | �����£�NH4Cl��NH3•H2O�����Һ��PH=7��c��NH4+ ��=c��Cl-�� | |
| C�� | �������Һ�м������������ƣ��õ��ļ��Ի����Һ��c��Na+����c��CH3COO-����c��H+����c��OH-�� | |
| D�� | �����£����������Һ�еμ�ϡ����õ���pH=5�Ļ����Һ��c��K+����c��NO3-�� |
���� A���κε������Һ�ж����������غ㣬���������غ��жϣ�
B��������pH=7����Һ�д���c��H+��=c��OH-�������ݵ���غ��жϣ�
C����Һ�ʼ��ԣ������c��H+����c��OH-������ϵ���غ��жϣ�
D���κε������Һ�ж����������غ㣬���������غ��жϣ�
��� �⣺A���κε������Һ�ж����������غ㣬���������غ��c��OH-��=c��HCO3-��+c��H+��+2c��H2CO3������A����
B��������pH=7����Һ�д���c��H+��=c��OH-�������ݵ���غ�c��NH4+ ��+c��H+��=c��OH-��+c��Cl-����c��NH4+ ��=c��Cl-������B��ȷ��
C����Һ�ʼ��ԣ������c��H+����c��OH-������ϵ���غ��c��Na+����c��CH3COO-������C����
D���κε������Һ�ж����������غ㣬���������غ�ã�c��K+��=c��NO3-������D����
��ѡB��
���� ���⿼������Ũ�ȴ�С�Ƚϣ�Ϊ��Ƶ���㣬��ȷ��Һ�����ʼ��������ǽⱾ��ؼ���ע���غ��Ӧ�ã��״�ѡ����D���ܶ�ͬѧ����Һ�����Ӱ������´�����Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
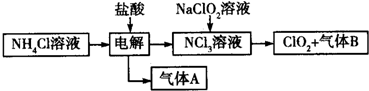
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | H2 | CO | CH4 | CH3COOH |
| ȼ���ȣ�kJ/mol�� | 286 | 283 | 890 | 874 |
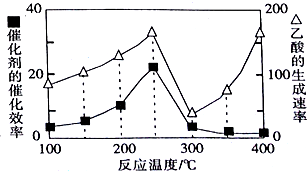
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
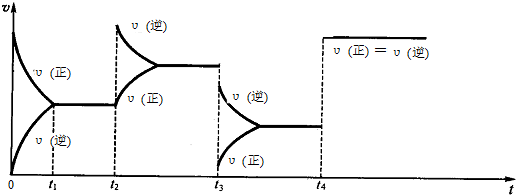
| ʱ�䣨s�� C��mol/L�� | 0 | 20 | 40 | 60 | 80 | 100 |
| C��N2O4�� | 0.20 | a | 0.10 | c | d | e |
| C��NO2�� | 0.00 | 0.12 | b | 0.22 | 0.22 | 0.22 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 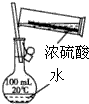 ϡ��Ũ���� | |
| B�� | 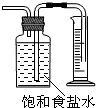 ����Cl2����� | |
| C�� | 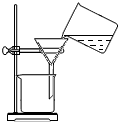 ���� | |
| D�� | 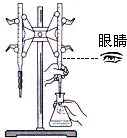 ��NaOH����Һ�ζ���ƿ�е����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
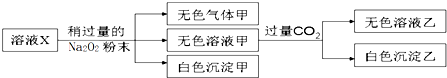
| A�� | Fe3+�϶������� | |
| B�� | ��ɫ����ײ�һ���Ǵ����� | |
| C�� | K+��Mg2+��Al3+��SO42-һ����������ҺX�� | |
| D�� | ��ɫ�����ҿ϶�����Al��OH��3��H2SiO3�Ļ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na2CO3��NaHCO3���嶼�����ȷ����ֽ� | |
| B�� | H2��SO2��CO2�������嶼����Ũ������� | |
| C�� | Fe��OH��3������ɫ�������ܲ������������ | |
| D�� | SiO2���ܺ�����������Һ��Ӧ���ܺ�����ᷴӦ������������������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �� ���� | ��A | ��A | ��A | ��A | ��A | ��A | ����A | 0 |
| 2 | C | O | F | |||||
| 3 | Na | Mg | P | S | Cl |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com