
【题目】根据价层电子对互斥理论,判断下列分子或者离子的空间构型是平面三角形的是( )
A.CO2B.H3O+C.BF3D.PO43﹣
【答案】C
【解析】
根据价层电子对互斥理论确定其空间构型,价层电子对数=σ 键个数+![]() (a-xb),a指中心原子价电子个数,x指配原子个数,b指配原子形成稳定结构需要的电子个数,据此分析解答。
(a-xb),a指中心原子价电子个数,x指配原子个数,b指配原子形成稳定结构需要的电子个数,据此分析解答。
A、二氧化碳分子中,价层电子对个数=σ键个数+孤电子对个数=2+![]() (4-2×2)=2,所以碳原子采取sp杂化,故空间结构为直线形,故A错误;
(4-2×2)=2,所以碳原子采取sp杂化,故空间结构为直线形,故A错误;
B、H2O中O原子有两对孤对电子,H3O+中O原子有一对孤对电子,价层电子对个数=σ键个数+孤电子对个数=3+![]() (6-1-3×1)=4,所以H3O+中氧原子采取sp3杂化。空间构型为三角锥形,故B错误;
(6-1-3×1)=4,所以H3O+中氧原子采取sp3杂化。空间构型为三角锥形,故B错误;
C、BF3分子中,中心B原子成3个σ键、没有孤对电子,价层电子对个数=3+![]() ×(3-3×1)=3,故杂化轨道数为3,采取sp2杂化,空间结构为平面正三角形,故C正确;
×(3-3×1)=3,故杂化轨道数为3,采取sp2杂化,空间结构为平面正三角形,故C正确;
D、PO43-中价层电子对个数=σ键个数+孤电子对个数=4+![]() (5+3-4×2)=4,所以PO43-中磷原子采取sp3杂化,空间构型为四面体,故D错误。
(5+3-4×2)=4,所以PO43-中磷原子采取sp3杂化,空间构型为四面体,故D错误。
答案选C。


科目:高中化学 来源: 题型:
【题目】在一密闭容器中,反应![]() 达到平衡时,测得
达到平衡时,测得![]() 为
为![]() 在温度不变的情况下,将容积增大一倍,当达到新的平衡时,测得
在温度不变的情况下,将容积增大一倍,当达到新的平衡时,测得![]() 为
为![]() 下列判断中不正确的是
下列判断中不正确的是
A.物质B的质量分数减小B.平衡时逆反应速率减小
C.化学计量数:![]() D.物质C的体积分数不变
D.物质C的体积分数不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中能大量共存的是( )
A.pH=1的溶液中:Fe2+、NO3-、SO42-、Na+
B.由水电离的c(H+)=1×10-14mol·L-1的溶液中:Ca2+、K+、Cl-、HCO3-
C.![]() =1012的溶液中:NH4+、Al3+、NO3-、Cl-
=1012的溶液中:NH4+、Al3+、NO3-、Cl-
D.NaHS溶液中:K+、S2-、SO42-、Al3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在给定条件下能大量共存的是 ( )
A.在c(HCO![]() )="0.1" mol·L-1的溶液中:NH
)="0.1" mol·L-1的溶液中:NH![]() 、Al3+、Cl-、NO
、Al3+、Cl-、NO![]()
B.有大量![]() 存在的溶液中:Na+、Mg2+、Ca2+、I-
存在的溶液中:Na+、Mg2+、Ca2+、I-
C.有大量![]() 存在的强酸性溶液中:NH
存在的强酸性溶液中:NH![]() 、Ba2+、Fe2+、Br-
、Ba2+、Fe2+、Br-
D.能使红色石蕊试纸变蓝的溶液中:SO![]() 、S2-、Na+、K+
、S2-、Na+、K+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于化学反应中的能量变化,下列说法中不正确的是( )
A. 燃烧反应都是放热反应
B. 对于可逆反应:aA(g)+bB(g)![]() bC(g)+dD(g),如果正反应放热,逆反应一定吸热
bC(g)+dD(g),如果正反应放热,逆反应一定吸热
C. 氢气燃烧生成水是一个放热的化学反应,说明1 mol H2的能量高于1 mol H2O的能量
D. 只有放热的氧化还原反应才可以设计为原电池
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N4分子结构为正四面体(如图所示)。己知:断裂N4(g)中1molN-N键吸收193kJ能量,形成N2(g)中1 molN≡N放出941 kJ能量。下列说法正确的是

A. 形成1 molN4(g)中的化学键放出193kJ的能量
B. N4(g)比N2(g)更稳定
C. lmolN2(g)完全转化为N4(g),体系的能量增加362kJ
D. N4(g) =2N2(g) △H=724kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组利用下面的装置进行实验,②、③中溶液均足量,操作和现象如下表。
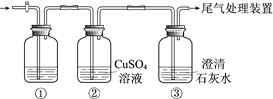
实验 | 操作 | 现象 |
Ⅰ | 向盛有Na2S溶液的①中持续通入CO2至过量 | ②中产生黑色沉淀,溶液的pH降低; ③中产生白色浑浊,该浑浊遇酸冒气泡 |
Ⅱ | 向盛有NaHCO3溶液的①中持续通入H2S气体至过量 | 现象同实验Ⅰ |
资料:CaS遇水完全水解
由上述实验得出的结论不正确的是
A.③中白色浑浊是CaCO3
B.②中溶液pH降低的原因是:H2S+Cu2+ == CuS↓+2H+
C.实验Ⅰ①中发生的反应是:CO2+H2O+ S2== CO32+ H2S
D.由实验Ⅰ和Ⅱ不能比较H2CO3和H2S酸性的强弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向 100 mL0.01 mol·L-1HA 溶液中逐滴加入0.02 mol·L-1MOH 溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题:

(1)由图中信息可知HA为 酸(填“强”或“弱”),理由是 。
(2)常温下一定浓度的MA稀溶液的pH = a,则a_________7(填“ > ”、“< ”或“=”),用离子方程式表示其原因:_____________________,此时,溶液中由水电离出的c(OH-)= 。
(3)请写出K点所对应的溶液中离子浓度的大小关系:____________________。
(4)K点对应的溶液中,c(M+) +c(MOH)__________2c (A-)(填“>”“<”或“=”);若此时溶液的 pH = 10,则 c(MOH) +c(OH-) =_____________mol· L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用化学链燃烧技术有利于提高燃料利用率。化学链燃烧技术的基本原理是借助载氧剂(如Fe2O3,FeO等)将燃料与空气直接接触的传统燃烧反应分解为几个气固反应,燃料与空气无须接触,由载氧剂将空气中的氧气传递给燃料。回答下列问题:
Ⅰ.以Fe2O3作载氧剂的化学链燃烧循环转化反应的部分热化学方程式如下,循环转化的原理如图所示:
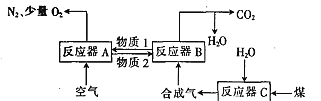
①C(s) +H2O(g) = CO(g)+ H2(g) ΔH = akJmol-1
②CO(g)+ H2(g) + O2(g) = CO2(g) +H2O(g) ΔH = bkJmol-1
(1)写出图中总反应的热化学方程式:_____________________________
(2)空气经反应器A后得到的尾气___________(填“能”或“不能”)直接用作工业合成氨的原料气,原因是_____________________。
Ⅱ.用FeO作载氧剂,部分反应的lgKp [K是用平衡分压(平衡分压=总压×物质的量分数)代替平衡浓度]与温度的关系如图所示。
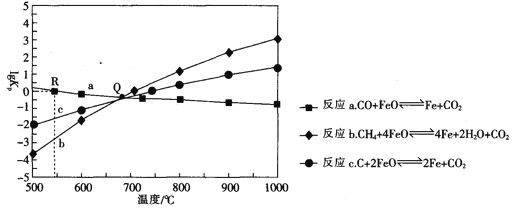
(3)图中涉及的反应中,属于吸热反应的是反应_________________(填字母)。
(4)R点对应温度下,向某恒容密闭容器中通入1molCO,并加入足量的FeO,只发生反应CO(g)+ FeO(s) ![]() CO2(g) +Fe(s),则CO的平衡转化率为______________.
CO2(g) +Fe(s),则CO的平衡转化率为______________.
Ⅲ.在T℃下,向某恒容密闭容器中加入1molCH4(g)和4mol FeO(s)进行反应:CH4(g) + 4FeO(s) ![]() 4Fe(s) +2H2O(g) +CO2(g)。反应起始时压强为P0,反应进行至10min时达到平衡状态,测得此时容器的气体压强是起始压强的2倍。
4Fe(s) +2H2O(g) +CO2(g)。反应起始时压强为P0,反应进行至10min时达到平衡状态,测得此时容器的气体压强是起始压强的2倍。
(5)T℃下,该反应的Kp = _____________________.
(6)若起始时向该容器中加入1molCH4(g),4molFeO(s),1mol H2O(g),0.5molCO2(g),此时反应向__________________(填“正反应”或“逆反应”)方向进行。
(7)其他条件不变,若将该容器改为恒压密闭容器,则此时CH4的平衡转化率___________(填“增大”“减小”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com