
分析 根据n=$\frac{m}{M}$计算出硫酸钠的物质的量,然后根据c=$\frac{n}{V}$计算出所得硫酸钠溶液的物质的量浓度;根据硫酸钠的化学式计算出钠离子的浓度;根据n(SO42-)=n(Na2SO4)、N=nNA计算出含有的硫酸根离子的数目.
解答 解:14.2g Na2SO4的物质的量为:$\frac{14.2g}{142g/mol}$=0.1mol,所得硫酸钠溶液的浓度为:c(Na2SO4)=$\frac{0.1mol}{1L}$=0.1mol/L;
所得溶液中含有钠离子的浓度为:c(Na+)=2c(Na2SO4)=0.1mol/L×2=0.2mol/L;
该溶液中含有硫酸根离子的物质的量为:n(SO42-)=n(Na2SO4)=0.1mol,则含有硫酸根离子的数目为0.1NA,
故答案为:0.1mol/L;0.2mol/L;0.1NA.
点评 本题考查了物质的量浓度的计算,题目难度不大,明确物质的量浓度的概念及表达式为解答关键,注意掌握物质的量与摩尔质量、阿伏伽德罗常数、物质的量浓度之间的关系,试题培养了学生的化学计算能力.


科目:高中化学 来源: 题型:选择题
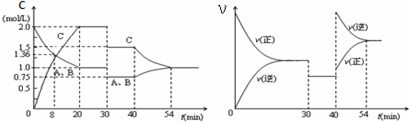
| A. | 8min时表示正反应速率等于逆反应速率 | |
| B. | 在0-54分钟的反应过程中该可逆反应的平衡常数始终为4 | |
| C. | 40min时改变的条件是升高温度,且正反应为放热反应 | |
| D. | 反应方程式中的x=1,30min时改变的条件是降低温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
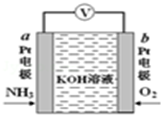 电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图所示,NH3被氧化为常见无毒物质.下列说法错误的是( )
电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图所示,NH3被氧化为常见无毒物质.下列说法错误的是( )| A. | 溶液中K+向电极b移动 | |
| B. | 反应消耗的NH3与O2的物质的量之比为4:5 | |
| C. | 氨气在电极a上发生氧化反应 | |
| D. | 正极的电极反应式为:O2+4e-+2H20=4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3→Na++H++CO32- | B. | HClO→H++ClO- | ||
| C. | H2S?2H++S2- | D. | NH4++OH-→NH3•H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 茶是我国的传统饮品,茶叶中含有的茶多酚可以替代食品添加剂中对人体有害的合成抗氧化剂,用于多种食品保鲜等,如图1所示是茶多酚中含量最高的一种儿茶素A的结构简式,关于这种儿茶素A的有关叙述正确的是( )
茶是我国的传统饮品,茶叶中含有的茶多酚可以替代食品添加剂中对人体有害的合成抗氧化剂,用于多种食品保鲜等,如图1所示是茶多酚中含量最高的一种儿茶素A的结构简式,关于这种儿茶素A的有关叙述正确的是( )| A. | ①② | B. | ①④ | C. | ②③ | D. | ③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com