
| A. | 将氯化铁饱和溶液逐滴滴入氢氧化钠稀溶液中,边滴边搅拌,可获得氢氧化铁胶体 | |
| B. | 不能用乙醇萃取碘水中的碘是因为碘在水中溶解度比在乙醇中大 | |
| C. | 实验室可通过蒸馏的方法除去自来水中含有的氯离子等杂质制蒸馏水 | |
| D. | 定容时俯视容量瓶的刻度线会导致所配制的溶液浓度偏低 |
分析 A.FeCl3+3NaOH=Fe(OH)3↓+3NaCl,生成氢氧化铁沉淀;
B.萃取剂的选择原则是:与水互不相溶,被萃取的物质在该溶剂中的溶解度比在水中的溶解度大,且跟萃取物不发生化学反应;
C.氯离子难挥发,自来水加热蒸发,冷却后可得蒸馏水;
D.定容时俯视容量瓶体积偏小.
解答 解:A.FeCl3+3NaOH=Fe(OH)3↓+3NaCl,生成氢氧化铁沉淀,得不到氢氧化铁胶体,故A错误;
B.不能用乙醇萃取碘水中的碘是因为乙醇和水互溶,故B错误;
C.自来水中含有的Cl-等杂质,蒸馏时,可将水和杂质分离,可得到纯净的水,故C正确;
D.定容时俯视容量瓶体积偏小,浓度偏大,故D错误.
故选C.
点评 本题考查化学实验方案的评价,为高频考点,涉及胶体制备及分离与提纯、溶液配制等,侧重实验基本操作和实验原理的考查,注意装置的作用及实验的操作性、评价性分析,题目难度不大.


 互动英语系列答案
互动英语系列答案科目:高中化学 来源: 题型:选择题
| A. | 3:2:2 | B. | 2:3:2 | C. | 2:2:3 | D. | 3:2:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
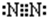 ,其中的化学键属于共价键(填“离子”或“共价”).
,其中的化学键属于共价键(填“离子”或“共价”).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (NH4)2Fe(SO4)2溶液中:Ba2+、K+、OH-、Br- | |
| B. | 通入过量SO2气体的溶液中:Fe3+、NO3-、Ba2+、H+ | |
| C. | $\frac{c(O{H}^{-})}{c({H}^{+})}$=10-12的溶液中:NH4+、Cu2+、NO3-、Cl- | |
| D. | c(I-)=0.1 mol•L-1的溶液中:Na+、Fe3+、ClO-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| a/g | 起始读数/mL | b/mL | c/mL |
| 0.1970 | 0.00 | 31.30 | 42.40 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 定量检验C2H5Cl时,将C2H5Cl和NaOH溶液混合共热后,加盐酸酸化 | |
| B. | 为提高KMnO4溶液的氧化能力,用盐酸将KMnO4溶液酸化 | |
| C. | 鉴定检测液中是否有Fe2+时,用硝酸酸化,再加KSCN溶液 | |
| D. | 鉴别溶液中是否含有SO42-可用盐酸酸化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com