
【题目】硅酸(H2SiO3)是一种难溶于水的弱酸,从溶液中析出时常形成凝胶状沉淀。实验室常用 Na2SiO3 溶液制备硅酸。某小组同学进行了如下实验:
编号 | Ⅰ | Ⅱ |
实验 |
|
|
现象 | a 中产生凝胶状沉淀 | b 中凝胶状沉淀溶解,c 中无明显变化 |
下列结论不正确的是
A.Na2SiO3 溶液一定显碱性
B.由 Ⅰ 不 能 说 明 酸 性 H2CO3>H2SiO3
C.由Ⅱ可知,同浓度时 Na2CO3 溶液的碱性强于 NaHCO3 溶液
D.向 Na2SiO3 溶液中通入过量 CO2,发生反应:SiO32-+CO2+H2O=CO32-+H2SiO3↓
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源: 题型:
【题目】根据如图所示转化关系判断下列说法正确的是( )
![]()
A.(C6H10O5)n可以是淀粉或纤维素,二者均属于多糖,互为同分异构体
B.可以利用与新制Cu(OH)2悬浊液反应生成砖红色沉淀证明反应①的最终产物为葡萄糖
C.酸性高锰酸钾溶液可将乙醇氧化为乙酸,将烧黑的铜丝趁热插入乙醇中也可得到乙酸
D.向反应②得到的混合物中倒入饱和氢氧化钠溶液并分液可得到纯净的乙酸乙酯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,将0.1mo/L的NaOH溶液滴入盛有50mLpH=2的HA溶液的绝热容器中(忽略热胀冷缩和分子空隙对体积的影响),加入NaOH溶液的体积V与溶液温度T的关系如图,下列说法不正确的是( )

A.25℃时,该pH=2的HA溶液电离度为10%
B.b点溶液显碱性
C.b到c的过程中,温度下降的主要原因是NaOH溶液的加入
D.c点溶液中,c(Na+)<c(A-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】观察下列模型并结合有关信息,判断下列说法不正确的是( )
HCN | S8 | SF6 | B12结构单元 | |
结构模型 示意图 |
|
|
|
|
备注 | — | 易溶于CS2 | — | 熔点1 873 K |
A. HCN的结构式为H—C≡N,分子中含有2个σ键和2个π键
B. 固态硫S8属于原子晶体
C. SF6是由极性键构成的非极性分子
D. 单质硼属原子晶体,结构单元中含有30个B—B键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,Na2S溶液中存在水解平衡:S2-+H2O![]() HS-+OH,在溶液中加入少量CuSO4固体,HS-浓度减小。下列说法正确的是
HS-+OH,在溶液中加入少量CuSO4固体,HS-浓度减小。下列说法正确的是
A. 稀释溶液,水解平衡常数增大
B. Ksp(CuS)<Ksp[Cu(OH)2]
C. 升高温度![]() 增大
增大
D. 加入MgCl2固体,HS-浓度减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生物浸出是用细菌等微生物从固体中浸出金属离子,有速率快、浸出率高等特点。氧化亚铁硫杆菌是一类在酸性环境中加速 Fe2+氧化的细菌,培养后能提供 Fe3+, 控制反应条件可达细菌的最大活性,其生物浸矿机理如下图。
![]()
反应1 反应2
(1)氧化亚铁硫杆菌生物浸出 ZnS 矿。
①反应 2 中有 S 单质生成,离子方程式是__。
② 实验表明温度较高或酸性过强时金属离子的浸出率均偏低,原因可能是__。
(2)氧化亚铁硫杆菌生物浸出废旧锂离子电池中钴酸锂(LiCoO2)与上述浸出机理相似,发生反应1 和反应3:LiCoO2 +3Fe3+=Li++ Co2++3Fe2++O2↑
①在酸性环境中,LiCoO2 浸出 Co2+的总反应的离子方程式是__。
②研究表明氧化亚铁硫杆菌存在时,Ag+对钴浸出率有影响,实验研究 Ag+的作用。取 LiCoO2 粉末和氧化亚铁硫杆菌溶液于锥形瓶中,分别加入不同浓度 Ag+的溶液,钴浸出率(图 1)和溶液 pH(图 2)随时间变化曲线如下:
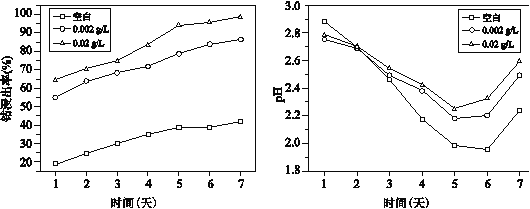
图1 不同浓度Ag+作用下钴浸出率变化曲线 图2 不同浓度Ag+作用下溶液中pH变化曲线
Ⅰ.由图 1 和其他实验可知,Ag+能催化浸出 Co2+,图 1 中的证据是__。
Ⅱ.Ag+是反应 3 的催化剂,催化过程可表示为: 反应 4:Ag++LiCoO2=AgCoO2+Li+
反应 5:……
反应 5 的离子方程式是__。
Ⅲ.由图 2 可知,第 3 天至第 7 天,加入 Ag+后的 pH 均比未加时大,结合反应解释其原因:__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用少量的溴和足量的乙醇制备1,2一二溴乙烷的装置如图所示:

有关数据列表如下:
乙醇 | 1.2二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g/cm﹣3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | ﹣130 | 9 | ﹣116 |
请按要求回答下列问题:
(1)写出A装置中的化学反应方程式_____;
(2)装置C中盛有氢氧化钠溶液,其作用是_____
(3)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是_____
(4)判断该制备反应已经结束的最简单方法是_____;
(5)若产物中有少量未反应的Br2,最好用_____洗涤除去;(填正确选项前的字母)
a 水 b 亚硫酸氢钠 c 碘化钠溶液 d 乙醇
(6)反应过程中应用冷水冷却装置D,其主要目的是_____;但又不能过度冷却(如用冰水),其原因是_____.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国化学家研究的一种新型复合光催化剂[碳纳米点(CQDs)/氮化碳(C3N4)纳米复合物]可以利用太阳光实现高效分解水,其原理如图所示。下列说法正确的是
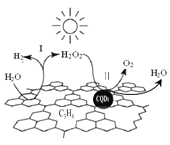
A. C3N4中C的化合价为 -4
B. 反应的两个阶段均为吸热过程
C. 阶段Ⅱ中,H2O2既是氧化剂,又是还原剂
D. 通过该反应,实现了化学能向太阳能的转化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环境监察局常用“定电位NOx传感器来监测化工厂的氮氧化物气体是否达到排放标准,其工作原理如图所示。下列说法不正确的是( )
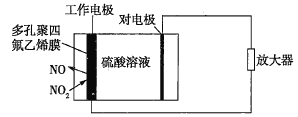
A.“对电极”是负极
B.“工作电极”上发生的电极反应为NO2+2e-+2H+=NO+H2O
C.传感器工作时H+移向“对电极”
D.“对电极”的材料可能为活泼金属锌
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com